ബോറിയം
അണുസംഖ്യ 105 ആയ മൂലകമാണ് ബോറിയം.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| വിവരണം | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| പേര്, പ്രതീകം, അണുസംഖ്യ | ബോറിയം, Bh, 107 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| കുടുംബം | സംക്രമണ ലോഹങ്ങൾ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ഗ്രൂപ്പ്, പിരീഡ്, ബ്ലോക്ക് | 7, 7, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| സാധാരണ ആറ്റോമിക ഭാരം | [270] g·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ഇലക്ട്രോൺ വിന്യാസം | [Rn] 5f14 6d5 7s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ഓരോ ഷെല്ലിലേയും ഇലക്ട്രോണുകൾ | 2, 8, 18, 32, 32, 13, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ഭൗതികസ്വഭാവങ്ങൾ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase | ഖരം എന്ന് കരുതുന്നു | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ക്രിസ്റ്റൽ ഘടന | unknown | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ഓക്സീകരണാവസ്ഥകൾ | 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellaneous | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS registry number | 54037-14-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selected isotopes | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| അവലംബങ്ങൾ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Bh ആണ് ആവർത്തനപ്പട്ടികയിലെ ഇതിന്റെ പ്രതീകം. ഇത് ഒരു കൃത്രിമ മൂലകമാണ്.
Bh-270 ആണ് ഇതിന്റെ ഏറ്റവും സ്ഥിരതയുള്ള ഐസോട്ടോപ്പ്. 61 സെക്കന്റ് ആണ് അതിന്റെ അർദ്ധായുസ്. ആവർത്തനപ്പട്ടികയിലെ ഏഴാം ഗ്രൂപ്പിൽ ഇതിനെ ഉൾപ്പെടുത്താമെന്ന് പരീക്ഷണങ്ങളിലൂടെ സ്ഥിരീകരിച്ചിട്ടുണ്ട്.
ഔദ്യോഗിക കണ്ടെത്തൽ
പീറ്റർ ആംബ്രസ്റ്റർ, ഗോട്ട്ഫ്രൈഡ് മ്യുൻസെൻബെർഗ് എന്നിവരുടെ നേതൃത്വത്തിലുള്ള ജർമൻ ശാസ്ത്രജ്ഞരുടെ സംഘമാണ് ആദ്യമായി ബോറിയം നിർമിച്ചത്. 1981ൽ ഡാംസ്റ്റാഡ്റ്റിലെ ഗെസെൽഷഫ്റ്റ് ഫർ ഷ്വെറിയോണെൻഫോർഷുങ് (ഇന്റിറ്റ്യൂട്ട് ഫോർ ഹെവി അയോൺ റിസേർച്ച്)ൽ വച്ചായിരുന്നു അത്. ഡബ്ന പ്രവർത്തനമായിരുന്നു അവർ അതിനായി ഉപയോഗിച്ചത്.
1989ൽ ജിഎസ്ഐ സംഘം ഈ പരീക്ഷണം വിജയകരമായി ആവർത്തിച്ചു. 261Bhനെ പരീക്ഷണത്തിൽ തിരിച്ചറിഞ്ഞു. 262Bh രണ്ട് ഐസോമെറുകൾ ആയാണ് കാണപ്പെടുന്നതെന്നും സ്ഥിരീകരിച്ചു.
ഐയുപിഎസി/ഐയുപിഎസി ട്രാൻസ്ഫെർമിയം വർക്കിങ് ഗ്രൂപ്പ് (ടി.ഡബ്ലി.യുജി) 1992ൽ ജിഎസ്ഐ സംഘത്തെ മൂലകം 107ന്റെ ഉപജ്ഞാതാക്കളായി പ്രഖ്യാപിച്ചു.
നിർദ്ദേശിത നാമങ്ങൾ
ആദ്യകാലങ്ങളിൽ മൂലകം 107 ഏക റെനിയം എന്ന പേരിലാണ് അറിയപ്പെട്ടിരുന്നത്.
ഡാനിഷ് ഊർജതന്ത്രജ്ഞനായ നീൽസ് ബോറിന്റെ ബഹുമാനാർത്ഥം Ns എന്ന പ്രതീകത്തോടെ നീൽസ്ബോറിയം എന്ന പേരാണ് ജർമൻകാർ നിർദ്ദേശിച്ചത്. സോവിയറ്റുകാർ ഈ പേര് മൂലകം 105ന് (ഡബ്നിയം) നൽകണമെന്ന് മുമ്പ് നിർദ്ദേശിച്ചിരുന്നു.
101 മുതൽ 109 വരെയുള്ള മൂലകങ്ങളുടെ നാമകരണത്തേച്ചൊല്ലി പല വിവാദങ്ങളമുണ്ടായി. അതിനാൽ ഐയുപിഎസി മൂലകം 107ന് അൺനിൽസെപ്റ്റിയം എന്ന താൽകാലിക നാമം സ്വീകരിച്ചു. ശാസ്ത്രജ്ഞരുടെ മുഴുവൻ പേര് മൂലകങ്ങൾക്ക് നൽകുന്ന ഒരു രീതി നിലവിലില്ലായിരുന്നതിനാൽ 1994ൽ നീൽബോറിയം എന്ന പേര് ഐയുപിഎസി തിരസ്കരിച്ചു. ബോറിയം എന്ന പേരാണ് അവർ നിർദ്ദേശിച്ചത്. മൂലകത്തിന്റെ ഉപജ്ഞാതാക്കൾ ഈ നിർദ്ദേശത്തെ എതിർക്കുകയും തങ്ങൾക്കാണ് മൂലകത്തിന് പേര് നൽകാനുള്ള അവകാശം എന്ന് വാദിക്കുകയും ചെയ്തു. ഈ പ്രശ്നം ഐയുപിഎസിയുടെ ഡാനിഷ് ശാഖയിലേക്ക് വിടുകയും അവർ ബോറിയം എന്ന പേരിനെ അനുകൂലിക്കുകയും ചെയ്തു. എന്നാൽ ബോറീയവും ബോറോണും തമ്മിലുള്ള സാമ്യം ആശയക്കുഴപ്പമുണ്ടാക്കുമോ എന്നൊരു പ്രശ്നമുണ്ടായി. പ്രത്യേകിച്ച് അവയുടെ ഓക്സോ-അയോണുകളായ ബോറേറ്റും (bohrate) ബോറേറ്റും (borate0 തമ്മിൽ . എന്നാൽ 1997ൽ ലോകവ്യാപകമായി മൂലകം 107ന് ബോറിയം എന്ന പേര് സ്വീകരിക്കപ്പെട്ടു. ബോറിയത്തിന്റെ ലവണങ്ങളെ ബോറിയേറ്റ്സ് എന്ന് വിളിക്കാൻ ഐയുപിഎസി പിന്നീട് തീരുമാനിച്ചു.
ഇലക്ട്രോണിക് ഘടന
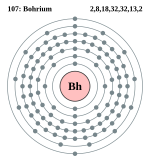
ആവർത്തനപ്പട്ടികയിലെ 107ആം മൂലകമാണ് ബോറിയം. അതിന്റെ രണ്ട് രീതിയിലുള്ള ഇലക്ട്രോൺ വിന്യാസങ്ങൾ:
ബോർ മാതൃക: 2, 8, 18, 32, 32, 13, 2
ക്വാണ്ടം മെക്കാനിക്കൽ മാതൃക: 1s22s22p63s23p64s23d10 4p65s24d105p66s24f145d10 6p67s25f146d5
ഐസോട്ടോപ്പുകളും കണ്ടുപിടിച്ച വർഷവും
| ഐസോട്ടോപ്പ് | കണ്ട്പിടിച്ച വർഷം | പ്രവർത്തനം |
|---|---|---|
| 260Bh | 2007 | 209Bi(52Cr,n) |
| 261Bh | 1989 | 209Bi(54Cr,2n) |
| 262Bhg,m | 1981 | 209Bh(54Cr,n) |
| 263Bh | unknown | |
| 264Bh | 1994 | 209Bi(64Ni,n) |
| 265Bh | 2004 | 243Am(26Mg,4n) |
| 266Bh | 2004 | 209Bi(70Zn,n) |
| 267Bh | 2000 | 249Bk(22Ne,5n) |
| 268Bh | unknown | |
| 269Bh | unknown | |
| 270Bh | 2006 | 237Np(48Ca,3n) |
| 271Bh | unknown | |
| 272Bh | 2003 | 243Am(48Ca,3n) |
ആധാരങ്ങൾ
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ക്ഷാര ലോഹങ്ങൾ | ആൽക്കലൈൻ ലോഹങ്ങൾ | ലാന്തനൈഡുകൾ | ആക്റ്റിനൈഡുകൾ | സംക്രമണ ലോഹങ്ങൾ | മറ്റു ലോഹങ്ങൾ | അർദ്ധലോഹങ്ങൾ | അലോഹങ്ങൾ | ഹാലൊജനുകൾ | ഉൽകൃഷ്ട വാതകങ്ങൾ | രാസസ്വഭാവം കൃത്യമായി മനസ്സിലാക്കാൻ പറ്റിയിട്ടില്ലാത്ത മൂലകങ്ങൾ |
This article uses material from the Wikipedia മലയാളം article ബോറിയം, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). പ്രത്യേകം പറയാത്ത പക്ഷം ഉള്ളടക്കം CC BY-SA 4.0 പ്രകാരം ലഭ്യം. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki മലയാളം (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.


