நைட்ரசு ஆக்சைடு: வேதிச் சேர்மம்
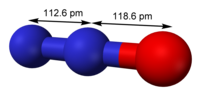
நைட்ரஸ் ஆக்சைடு (nitrous oxide), அல்லது பொதுவாக சிரிப்பூட்டும் வாயு, நைட்ரசு, நைட்ரோ, NOS என அழைக்கப்படுவது N2O என்ற வாய்பாட்டைக் கொண்ட ஒரு வேதிச் சேர்மம் ஆகும்.
இது நைதரசனின் ஓர் ஆக்சைடு ஆகும். அறை வெப்பநிலையில் இது நிறமற்ற, நறுமணச் சுவையுடன், எளிதில் தீப்பற்றாத ஒரு வளிமம். இவ்வாயுவின் மயக்க மற்றும் வலிநிவாரண விளைவுகள் காரணமாக அறுவைச் சிகிச்சை மற்றும் பல் மருத்துவத்தில் பயன்படுத்தப்படுகிறது. சுவாசிக்கும்போது இவ்வாயு உண்டாக்கும் தற்காலிக மயக்கம் மற்றும் பரவச பொழுதுபோக்கு நன்னிலை காரணமாக இதனைச் சிரிப்பூட்டும் வாயு என்று அழைக்கின்றனர். தானுந்துப் பந்தய இயந்திரங்கள் மற்றும் ஏவூர்தித் தொழில்நுட்பத்தில் ஆற்றல் வெளியீட்டை அதிகரிக்கும் ஆக்சிசனேற்றியாக நைட்ரஸ் ஆக்சைடு பயன்படுத்தப்படுகிறது. உயர்த்தப்பட்ட வெப்பநிலையில், மூலக்கூறு ஆக்சிசன் போன்ற ஒரு சக்தி வாய்ந்த ஆக்சிசனூக்கியாகவும் இந்த ஆக்சைடு திகழ்கிறது.
 | |
 | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர் டைநைட்ரசன் மோனாக்சைடு | |
| வேறு பெயர்கள் சிரிப்பூட்டும் வாயு, இனிமையான வளி, Protoxide of nitrogen, Hyponitrous oxide | |
| இனங்காட்டிகள் | |
| 10024-97-2 | |
| ATC code | N01AX13 |
| ChEBI | CHEBI:17045 |
| ChEMBL | ChEMBL1234579 |
| ChemSpider | 923 |
| யேமல் -3D படிமங்கள் | Image |
| KEGG | D00102 |
| பப்கெம் | 948 |
| வே.ந.வி.ப எண் | QX1350000 |
SMILES
| |
| UNII | K50XQU1029 |
| UN number | 1070 (compressed) 2201 (liquid) |
| பண்புகள் | |
| N 2O | |
| வாய்ப்பாட்டு எடை | 44.013 கி/மோல் |
| தோற்றம் | நிறமற்ற வாயு |
| அடர்த்தி | 1.977 கி/லி (வாயு) |
| உருகுநிலை | −90.86 °C (182.29 K) |
| கொதிநிலை | −88.48 °C (184.67 K) |
| 1.5 கி/லி (15 °C) | |
| கரைதிறன் | ஆல்ககோல், ஈதர், கந்தகக் காடி ஆகியவற்றில் கரையக்கூடியது |
| மட. P | 0.35 |
| ஆவியமுக்கம் | 5150 kPa (20 °C) |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.330 |
| கட்டமைப்பு | |
| மூலக்கூறு வடிவம் | |
| இருமுனைத் திருப்புமை (Dipole moment) | 0.166 D |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH | +82.05 கிஜூ mol−1 |
| நியம மோலார் எந்திரோப்பி S | 219.96 ஜூ K−1 mol−1 |
| மருந்தியல் | |
| Routes of administration | உள்மூச்சு |
| வளர்சிதைமாற்றம் | 0.004% |
| உயிரியல் அரை-வாழ்வு | 5 நிமி. |
| கழிப்பு | மூச்சுத் தொகுதி |
| கருத்தரிப்பு வகைப்பாடு | |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | Ilo.org, ICSC 0067 |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாதது |
| தொடர்புடைய சேர்மங்கள் | |
| நைட்ரசன் ஆக்சைடுகள் தொடர்புடையவை | நைட்ரிக் ஆக்சைடு டைநைதரசன் ட்ரைஆக்சைடு நைதரசனீரொட்சைடு டைநைதரசன் டெட்ராஆக்சைடு டைநைதரசன் பென்டாக்சைடு |
| தொடர்புடைய சேர்மங்கள் | அமோனியம் நைதரேட்டு Azide |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
நைட்ரஸ் ஆக்சைடு ஆக்சிசன் அணுக்களுடன் வினை புரிந்து நைட்ரிக் ஆக்சைடைத் தருகிறது. இயற்கையாகத் தோன்றும் இந்த நைட்ரிக் ஆக்சைடு ஓசோனுடன் வினைபுரிவதன் விளைவாக, அடுக்கு மண்டல ஓசோனின் சமநிலையைப் பாதிக்கிறது. இது வளி மாசடைதல், மற்றும் பைங்குடில் வளிமங்களிலும் அதிகமான அளவிலும் அங்கம் வகிக்கிறது. உலக வெப்பமயமாதலில் கடந்த நூறாண்டுகளில் காபனீரொக்சைட்டைக் காட்டிலும் 298 பங்குகள் அதிகமாக இவ்வாயு பங்கு வகித்துள்ளது.
உலக சுகாதார அமைப்பு பட்டியலிட்டுள்ள உடலுக்கு மிக அவசியமான மருந்துகளின் பட்டியலில் இதுவும் இடம்பிடித்துள்ளது.
நச்சுத்தன்மை இல்லாமல் இருப்பது, அறை வெப்பநிலையில் நிலைப்புத் தன்மையுடன் காணப்படுவது, பாதுகாப்பாக விமானத்தில் எடுத்துச் செல்ல முடிவது மற்றும் சேமித்து வைக்க எளிமையானது போன்ற பல சாதகமான அம்சங்கள் மற்ற ஆக்சைடுகளை விட நைட்ரஸ் ஆக்சைடுக்குக் கூடுதலாக இருப்பதால் ஏவூர்தி இயந்திரங்களில் இதை ஆக்சிசனேற்றியாக உபயோகிக்கிறார்கள். உடனடியாக சிதைந்து சுவாசிக்கும் காற்றாக இவ்வாயு மாறவியலும் என்பது மற்றுமொரு காரணமாகும். இதனுடைய அதிக அடர்த்தி மற்றும் குறைவான வெப்பநிலையில் உள்ள குறைந்த அழுத்தம் ஆகிய சிறப்புகள் மற்ற அதிக அழுத்த வாயுக்களுக்கு சவாலாக விளங்குகிறது
1914 ஆம் ஆண்டில், அமெரிக்க ராக்கெட் முன்னோடியான இராபர்ட் கோடார்ட் நைட்ரஸ் ஆக்சைடு மற்றும் பெட்ரோல் ஆகியவற்றை ஏவூர்திகளை உந்தி செலுத்துவதற்குச் சாத்தியமான திரவ எரிபொருள்களாக பரிந்துரைத்து காப்புரிமை பெற்றார். திட எரிபொருளுடன் திரவ அல்லது வாயு ஆக்சிசனேற்றிகளைப் பயன்படுத்திய பல்வேறு விதமாக வடிவமைக்கப்பட்ட கலப்பின ஏவூர்திகளில் நைட்ரஸ் ஆக்சைடு ஆக்சிசனேற்றியாக தேர்வு செய்யப்பட்டு வந்தது. ஐதராக்சைல் நீக்கப்பட்ட பலவணு பியூட்டாடையீன் உடன் நைட்ரஸ் ஆக்சைடு இணைந்த எரிபொருள் ஸ்பேஸ்சிப்வன் மற்றும் பல விண்கப்பல்களில் பயன்படுத்தப்பட்டு வந்தது. தொழில்சார்ந்த மற்றும் அதிக சக்திவாய்ந்த ஏவூர்திகளில் பல்வேறு வகையான நெகிழிகள் எரிபொருளாகப் பயன்படுத்தப்பட்டது என்பதும் கவனிக்கத்தக்கது.
நைட்ரஸ் ஆக்சைடு ஒற்றை உந்துபொருள் ஏவூர்திகளிலும்
பயன்கள்
ஏவூர்தி இயந்திரங்களில்
நச்சுத்தன்மை இல்லாமல் இருப்பது, அறை வெப்பநிலையில் நிலைப்புத் தன்மையுடன் காணப்படுவது, பாதுகாப்பாக விமானத்தில் எடுத்துச் செல்ல முடிவது மற்றும் சேமித்து வைக்க எளிமையானது போன்ற பல சாதகமான அம்சங்கள் மற்ற ஆக்சைடுகளை விட நைட்ரஸ் ஆக்சைடுக்குக் கூடுதலாக இருப்பதால் ஏவூர்தி இயந்திரங்களில் இதை ஆக்சிசனேற்றியாக உபயோகிக்கிறார்கள். உடனடியாக சிதைந்து சுவாசிக்கும் காற்றாக இவ்வாயு மாறவியலும் என்பது மற்றுமொரு காரணமாகும். இதனுடைய அதிக அடர்த்தி மற்றும் குறைவான வெப்பநிலையில் உள்ள குறைந்த அழுத்தம் ஆகிய சிறப்புகள் மற்ற அதிக அழுத்த வாயுக்களுக்கு சவாலாக விளங்குகிறது
1914 ஆம் ஆண்டில், அமெரிக்க ராக்கெட் முன்னோடியான இராபர்ட் கோடார்ட் நைட்ரஸ் ஆக்சைடு மற்றும் பெட்ரோல் ஆகியவற்றை ஏவூர்திகளை உந்தி செலுத்துவதற்குச் சாத்தியமான திரவ எரிபொருள்களாக பரிந்துரைத்து காப்புரிமை பெற்றார். திட எரிபொருளுடன் திரவ அல்லது வாயு ஆக்சிசனேற்றிகளைப் பயன்படுத்திய பல்வேறு விதமாக வடிவமைக்கப்பட்ட கலப்பின ஏவூர்திகளில் நைட்ரஸ் ஆக்சைடு ஆக்சிசனேற்றியாக தேர்வு செய்யப்பட்டு வந்தது. ஐதராக்சைல் நீக்கப்பட்ட பலவணு பியூட்டாடையீன் உடன் நைட்ரஸ் ஆக்சைடு இணைந்த எரிபொருள் ஸ்பேஸ்சிப்வன் மற்றும் பல விண்கப்பல்களில் பயன்படுத்தப்பட்டு வந்தது. தொழில்சார்ந்த மற்றும் அதிக சக்திவாய்ந்த ஏவூர்திகளில் பல்வேறு வகையான நெகிழிகள் எரிபொருளாகப் பயன்படுத்தப்பட்டது என்பதும் கவனிக்கத்தக்கது.
நைட்ரஸ் ஆக்சைடு ஒற்றை உந்துபொருள் ஏவூர்திகளிலும் எரிபொருளாகப் பயன்படுத்தப்படுகிறது. சூடாக்கப்பட்ட வினையூக்கி முன்னிலையில் N
2O சுமார் 1300 °C வெப்பநிலையில், நைதரசன் மற்றும் ஆக்சிசனாக சிதைவடைந்து வெப்பத்தை உமிழ்கிறது. வினையில் அதிக அளவிளான வெப்பம் வெளிவிடப்படுவதால் நைட்ரஸ் ஆக்சைடின் தன்னிச்சையான சிதைவு மேலோங்கி வினையூக்கியின் நடவடிக்கை விரைவில் இரண்டாம் பட்சமாகிறது. வெற்றிடப் பொறியியல் அமுக்கியில் இவ்வாறு வெளிப்படும் வெப்பவாற்றல் வழங்கும் ஒற்றை உந்துபொருள் உந்துவிசை எண் (Isp) 180s. அதேவேளையில் நைதரசன் டெட்ராக்சைடுடன் ஒற்றை உந்து பொருளாகவோ அல்லது இரட்டை உந்துபொருளாகவோ பயன்படுத்தப்படும் ஐதரசீன் வழங்கும் உந்துவிசை நைட்ரஸ் ஆக்சைடுடன் ஒப்பிடுகையில் Isp குறைவான மதிப்பையே கொண்டுளளது. இத்தகைய சிறப்புத் தன்மையினால் நைட்ரஸ் ஆக்சைடு ஏவூர்திகளில் எந்தவிதமான விசாரணைக்கும் இடமின்றி உந்துபொருளாக பயன்படுத்தப்படுகிறது.
நைட்ரஸ் ஆக்சைடு 21 வளிமண்டல அழுத்த சூழ்நிலையில் கிட்டத்தட்ட 600 °C (1,112 °F) குறை வெப்பநிலையில் வெடித்து எரிகிறது. உதாரணமாக 600 psi அழுத்த வீச்சில் இவ்விரு வாயுக்களை இணைத்து எளிதாக பற்றவைக்க முடியும், இப்பற்றவைப்புக்கு சுமார் 6 ஜூல் ஆற்றல் மட்டுமே தேவைப்படுகிறது. அதேசமயம், 130 psi அழுத்த வீச்சில் 2500 ஜூல் ஆற்றலை உள்ளிட்டாலும் N
2O வினைபுரியாமல் இருக்கிறது.
ஒரு ஐதரோ கார்பன் எரிபொருளை நைட்ரஸ் ஆக்சைடு சேமிக்கப்பட்டுள்ள அதே தொட்டியில் கலப்பதன் மூலம் குறிப்பிடத்தக்க அளவுக்கு உந்துவிசையை (Isp) மேம்படுத் இயலும். இக்கலவை நைட்ரஸ் ஆக்சைடு எரிபொருள் கலவை (NOFB) ஒற்றை உந்துபொருள் எனப்படுகிறது. நைட்ரஸ் ஆக்சைடு நிலைப்புத்தன்மை மிக்கது என்பதால் சேமிப்பு கலவையான நைட்ரஸ் ஆக்சைடு எரிபொருள் கலவையால் தன்னிச்சையாகப் பற்றிக்கொள்ளும் அபாயம் நேர்வதில்லை. நைட்ரஸ் ஆக்சைடு சூடாக்கப்பட்ட வினையூக்கி மூலமாக சிதைவடையும் போது , உயர் வெப்பநிலை ஆக்சிசன் வெளியிடப்பட்டு உடனடியாக ஹைட்ரோகார்பன் எரிபொருள் கலவை எரியூட்டப்படுகிறது. நைட்ரஸ் ஆக்சைடு எரிபொருள் கலவை ஒற்றை உந்துபொருள் அதிகபட்சமாக 300 வினாடிகள் Isp உந்துவிசையை அளிக்கவல்லது. தொட்டவுடன் தீப்பற்றும் உந்துவிசை அமைப்புகளைப் பயன்படுத்தலால் உண்டாகும் நச்சு விளைவுகள் இந்த ஹைட்ரோகார்பன் எரிபொருள் கலவையால் தவிர்க்கப்படுகின்றன. ஐதரசீன் மற்றும் டைநைதரசன் டெட்ராக்சைடுடன் ஒப்பிடுகையில் குறைந்த உறைநிலை கொண்ட நைட்ரஸ் ஆக்சைடு எரிபொருள் கலவையின் வெப்ப மேலாண்மை சிறப்பானது. இப்பண்பு விண்வெளியில் சேமித்து வைப்பதற்கு உகந்த உந்துபொருள்க்ளுக்குத் தேவையான சிறப்புப் பண்பாகும்.
மேற்கோள்கள்
வெளி இணைப்புகள்
This article uses material from the Wikipedia தமிழ் article நைட்ரசு ஆக்சைடு, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). வேறுவகையாகக் குறிப்பிடப்பட்டிருந்தாலன்றி இவ்வுள்ளடக்கம் CC BY-SA 4.0 இல் கீழ் கிடைக்கும். Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki தமிழ் (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.
