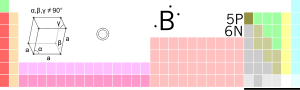
Grunnstoffet Bor: Grunnstoff med kjemisk symbol B og atomnummer 5
Bor er eit grunnstoff med atomnummer 5 og kjemisk symbol B.
| ||||||||||||||||||||
| Generelle eigenskapar | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Namn, kjemisk symbol, atomnummer | Bor, B, 5 | |||||||||||||||||||
| Kjemisk serie | Halvmetall | |||||||||||||||||||
| Gruppe, periode, blokk | 13, 2, p | |||||||||||||||||||
| Tettleik, hardleik | 2460 kg/m3, 9,3 (ikkje SI) | |||||||||||||||||||
| Utsjånad | Svart  | |||||||||||||||||||
| Atomeigenskapar | ||||||||||||||||||||
| Atommasse | 10,811 u (ikkje SI) | |||||||||||||||||||
| Atomradius (berekna) | 85 (87) pm | |||||||||||||||||||
| Kovalent radius | 82 pm | |||||||||||||||||||
| Ioneradius | 20 pm (ladning: +3) | |||||||||||||||||||
| van der Waals radius | (?) pm | |||||||||||||||||||
| Elektronkonfigurasjon | [He]2s22p1 | |||||||||||||||||||
| Elektron per energinivå | 2, 3 | |||||||||||||||||||
| Oksidasjonstrinn (oksid) | +3 (svak syre) | |||||||||||||||||||
| Krystallstruktur | Rombisk | |||||||||||||||||||
| Fysiske eigenskapar | ||||||||||||||||||||
| Tilstandsform | Fast stoff | |||||||||||||||||||
| Smeltepunkt | 2349 K (2076°C) | |||||||||||||||||||
| Kokepunkt | 4200 K (3927°C) | |||||||||||||||||||
| Molart volum | 4,39 cm3/mol | |||||||||||||||||||
| Fordampingsvarme | 507,8 kJ/mol | |||||||||||||||||||
| Smeltevarme | 50,2 kJ/mol | |||||||||||||||||||
| Damptrykk | 0,348 Pa ved 2300 °C | |||||||||||||||||||
| Ljodfart | 16200 m/s ved 20 °C | |||||||||||||||||||
| Diverse eigenskapar | ||||||||||||||||||||
| Elektronegativitet | 2,04 (Paulings skala) | |||||||||||||||||||
| Spesifikk varmekapasitet | 1026 J/(kg·K) | |||||||||||||||||||
| Elektrisk konduktivitet | 10−10 MS/m | |||||||||||||||||||
| Termisk konduktivitet | 27,4 W/(m·K) | |||||||||||||||||||
| Ioniseringspotensial | 800,6 kJ/mol 2427,1 kJ/mol 3659,7 kJ/mol 25026 kJ/mol 32827 kJ/mol | |||||||||||||||||||
| Mest stabile isotopar | ||||||||||||||||||||
| ||||||||||||||||||||
| SI-einingar og STP er brukt unntatt der det er avmerkt | ||||||||||||||||||||
Det er eit halvmetall i gruppe 13 i periodesystemet.
Særskilde kjenneteikn
Fleire allotrope former av bor, både amorfe og krystallinske er kjende.
Ein del borsambindingar, særleg hydrid har elektronunderskot. Det vil seia at det er færre elektron i bindinga enn det som må til for å oppfylla oktettregelen. Dette er mogleg fordi eit hydrogenatom kan danna ei bru mellom to boratom.
Bruk
Borsambindingar vert brukt i organisk syntese.
Historie
Bor vart oppdaga av Sir Humphrey Davy og Joseph-Louis Gay-Lussac i 1808, men borsambindingar har vore kjend lenge.
Kjemi
Boraks (Na2B4O7) er ein viktig sambinding av bor.
Biologisk rolle
Bor kan vera nødvendig for plantar.
Tryggleik
Bor og borat er ikkje giftige, så spesiell handsaming er unødvendig. Nokre andre borsambindingar er giftige.
Sjå også
Bakgrunnsstoff
This article uses material from the Wikipedia Nynorsk article Grunnstoffet bor, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Teksten er tilgjengeleg under CC BY-SA 4.0 om ikkje anna er oppgjeve. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Nynorsk (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.