Молибден
Молибден — хемиски елемент со симбол Мо и атомски број 42.
Името е од нео-латински molybdaenum , од старогрчки Μόλυβδος molybdos , што значи олово , бидејќи рудите на молибден биле помешани со оловни руди. Минералите на молибден се познати низ историјата, но елементот е откриен (во смисла на диференцијација како нов ентитет од минералните соли на други метали) во 1778 година од Карл Вилхелм Шеле . Металот првпат бил изолиран во 1781 година од Петар Јакоб Хелм .
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Општи својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Име и симбол | молибден (Mo) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изглед | металик сива | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молибденот во периодниот систем | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски број | 42 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандардна атомска тежина (±) (Ar) | 95,95(1) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Категорија | преоден метал | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Група и блок | група 6, d-блок | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Периода | V периода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електронска конфигурација | [Kr] 4d5 5s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
по обвивка | 2, 8, 18, 13, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физички својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза | цврста | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка на топење | 2.896 K (2.623 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка на вриење | 4.912 K (4.639 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Густина близу с.т. | 10,28 г/см3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| кога е течен, при т.т. | 9,33 г/см3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлина на топење | 37,48 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлина на испарување | 598 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Моларен топлински капацитет | 24,06 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
парен притисок
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Оксидациони степени | 6, 5, 4, 3, 2, 1, −1, −2, −4 (силен киселински оксид) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електронегативност | Полингова скала: 2,16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Енергии на јонизација | I: 684,3 kJ/mol II: 1.560 kJ/mol II: 2.618 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски полупречник | емпириски: 139 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентен полупречник | 154±5 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Разни податоци | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристална структура | телоцентрирана коцкеста (тцк) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Брзина на звукот тенка прачка | 5.400 м/с (при с.т.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинско ширење | 4,8 µм/(m·K) (при 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинска спроводливост | 138 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинска распространливост | 54,3 mm2/s (при 300 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електрична отпорност | 53,4 nΩ·m (при 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнетно подредување | парамагнетно | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модул на растегливост | 329 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модул на смолкнување | 126 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модул на збивливост | 230 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поасонов сооднос | 0,31 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мосова тврдост | 5,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Викерсова тврдост | 1.400–2.740 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Бринелова тврдост | 1.370–2.500 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-број | 7439-98-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Историја | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Откриен | Карл Вилхелм Шиле (1778) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Првпат издвоен | Петер Јакоб Јелм (1781) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Најстабилни изотопи | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Режимите на распад во загради се предвидени, но сè уште не се забележани | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Молибден не се јавува природно како слободен метал ; се наоѓа само во различни оксидациски состојби во минералите. Слободниот елемент, сребрен метал со сива боја, ја има шестата највисока точка на топење од секој елемент. Таа лесно формира цврсти, стабилни карбиди во легури , и затоа најголем дел од светското производство на молибденот (околу 80%) се користи во челични легури, вклучувајќи легури со висока јачина и суперлегури .
Повеќето соединенија на молибден имаат ниска растворливост во вода, но кога минералите што содржат молибден се во допир со кислород и вода, добиениот молибдат- јон MoO2−
4 е доста растворлив. Индустриски, соединенија на молибден (околу 14% од светското производство на елементот) се користат под висок притисок и на висока температура како пигменти и катализатори .
Ензимите кои содржат молибден се далеку најчестите бактериски катализатори за кинење на хемиската врска во атмосферскиот молекуларен азот во процесот на биолошко врзување на азот . Најмалку 50 молибденови ензими се познати кај бактериите, растенијата и животните, иако само бактериски и цианобактериски ензими се вклучени во врзување на азот. Овие нитрогенази содржат молибден во форма различна од другите ензими на молибден, кои сите содржат целосно оксидиран молибден во кофaктор на молибден . Овие различни ензими на молибден-кофактор се од витално значење за организмите, а молибденот е суштински елемент за живот во сите повисоки организми на еукариоти , иако не кај сите бактерии.
Особености
Физички својства
Во чиста форма, молибденот е сребрено-сив метал со цврстина на Мос од 5.5, и стандардна атомска тежина од 95.95 g / mol. Тој има точка на топење од 2,623 °C (4,753 °F) од природните елементи, само тантал , осмиум , рениум , волфрам и јаглерод имаат повисоки точки на топење. Mолибденот го има еден од најниските коефициенти на топлинско ширење кај комерцијално користените метали. Јачината на истегнување на молибденските жици се зголемува околу 3 пати, од околу 10 до 30 GPa , кога нивниот пречник се намалува од ~ 50-100 nm до 10 nm.
Хемиски својства
Молибден е преоден метал со електронегативност од 2.16 на скалата на Полинг. Тој на собна температура реагира не визуелно со кислород или вода. Слаба оксидација на молибден започнува на 300 °C (572 °F) ; масовна оксидација се јавува на температура над 600 °C, што резултира со молибден триоксид. Како и многу потешки преодни метали, молибденот покажува мала склоност да формира катјон во воден раствор, иако кадарот Mo 3+ е познат под внимателно контролирани услови.
Изотопи
Постојат 35 познати изотопи на молибден, кои се движат од 83 до 117 по атомска маса, како и четири метастабилни јадрени изомери. Седум изотопи се јавуваат природно, со атомски маси од 92, 94, 95, 96, 97, 98 и 100. Од овие природни изотопи, само молибден-100 е нестабилен.
Молибден-98 е најзастапен изотоп, кој содржи 24,14% од целиот молибден. Молибден-100 има период на полураспад од околу 10 19 години и подложува двојно бета распаѓање во рутениум -100. Молибденските изотопи со атомски броеви од 111 до 117 сите имаат период на полураствор од приближно 150ns. Сите нестабилни изотопи на молибден се распаѓаат во изотопи на ниобиум , технециум и рутениум.
Како што е наведено подолу, најчестата примена на изотопски молибден вклучува молибден-99 , кој е производ на цепење. Тоа е матичен радиоизотоп на краткотрајниот гама-јонски радиоизотоп технециум-99м , јадрен изомер кој се користи во разни примени во медицината. Во 2008 година, Технолошкиот универзитет Делфт аплицирал за патент за производство на молибден-99 на молибден-98.
Соединенија
Молибден формира хемиски соединенија во оксидациски состојби од -II до + VI. Повисоките оксидациски состојби се порелевантни за нејзината Земјина појава и нејзините биолошки улоги, состојбите на оксидација на средно ниво често се асоцирани со метални кластери , а многу ниските оксидни состојби обично се асоцирани со органомолибденски соединенија . Хемијата на Mo и W покажува силни сличности. Релативната реткост на молибденот (III), на пример, е во контраст со продорноста на хром (III) соединенијата. Највисоката состојба на оксидација се гледа во молибден (VI) оксид (MoO 3 ), додека нормалното сулфурно соединение е молибден дисулфид MoS 2 .
| Оксидациска состојба | Пример |
|---|---|
| -2 | Na2[Mo2(CO)10] |
| 0 | Mo(CO)6 |
| +1 | Na[C6H6Mo] |
| +2 | MoCl2 |
| +3 | Na3[Mo(CN)]6 |
| +4 | MoS2 |
| +5 | MoCl5 |
| +6 | MoF6 |

Од аспект на трговијата, најважните соединенија се молибден дисулфид ( MoS2 ) и молибден триоксид ( MoO3 ). Црниот дисулфид е главниот минерал. Се пече во воздух за да се даде триоксид:
- 2 MoS2 + 7 O2 → 2 MoO3 + 4 SO2
Трикоксидот, кој е испарлив на високи температури, е претходник на речиси сите други Mo соединенија, како и легури. Молибденот има неколку состојби на оксидација , најстариот стабилен е +4 и +6 (со задебелени букви во табелата лево).
Молибден (VI) оксид е растворлив во силна Базна вода, формирајќи молибдат (MoO 4 2- ). Молибдатите се послаби оксиданси отколку хроматите. Тие имаат тенденција да формираат структурно сложени оксианјони со кондензација со пониски вредности на pH , како што се [Mo 7 O 24 ] 6- и [Mo 8 O 26 ] 4- . Полимолибдат може да внесе други јони, формирајќи полиоксиметалати . Темно-синиот фосфор- хетерополимолибдат P [Mo 12 O 40 ] 3- се користи за спектроскопска детекција на фосфор. Широкиот опсег на оксидациски состојби на молибден се рефлектира во различни молибден хлориди:
- Молибден (II) хлорид MoCl 2 , кој постои како хексамер Mo 6 Cl 12 и поврзаниот dianion [Mo 6 Cl 14 ] 2- .
- Молибден (III) хлорид MoCl 3, темноцрвени цврсти, кој се претвора во анјонот trianionic комплекс [MoCl 6] 3-.
- Молибден (IV) хлорид MoCl 4 , црна цврста, која прифаќа полимерна структура.
- Молибден (V) хлорид MoCl 5 темнозелена цврста материја која прифаќа димерична структура.
Молибден (VI) хлорид MoCl 6 не е познат, иако молибденот хексафлуорид е добро карактеризиран.
Како и хромот и некои други транзициони метали, молибденот формира четиривалентни врски , како што се Mo 2 (CH 3 COO) 4 и [Mo 2 Cl 8 ] 4- , кој исто така има и четиривалентна врска.
Оксидациската состојба 0 е возможна со јаглерод моноксид како лиганд, како што е во молибден хексакарбонил , Mo (CO) 6 .
Историја
Молибденитот - главната руда од која сега се извлекува молибден - претходно беше познат како молибдена. Молибдена била помешана и често користена како да е графит . Како и графитот, молибденитот може да се користи за да се оцрни површина или како цврсто мазиво. Дури и кога молибдената се разликувала од графитот, таа сè уште била помешана со заедничката руда на олово PbS (сега се нарекува галена ); името доаѓа од старогрчки Μόλυβδος molybdos , што значи олово . (Грчкиот збор сам по себе е предложен како залог од анадолски лувиски и лидиски јазици).
Иако (наводно) молибден бил намерно легиран со челик во еден јапонски меч од 14 век ( Околу 1330 г.), таа уметност никогаш не била широко работена и подоцна била изгубена. На Западот во 1754 година, Бенгт Андерсон Кувист испитувал примерок од молибденит и утврдил дека не содржи олово и затоа не бил гален.
До 1778 година шведскиот хемичар Карл Вилхелм Шеле цврсто тврдел дека молибденот не е ниту гален ниту графит. Наместо тоа, Шиле предложил дека молибденот е руда од посебен нов елемент, именуван како молибден за минералот во кој живеел и од кој може да биде изолиран. Петар Џејкоб Хелм успешно го изолирал молибденот со користење на јаглеродно и ленено масло во 1781 година.
Следниот век, молибденот немал индустриска употреба. Релативно редок, чистиот метал бил тежок да се изолира, а неопходните техники на металургијата биле незрели. Раните челични легури направени од молибден покажале големо ветување за зголемена цврстина, но напорите за производство на легурите во голем обем биле попречени со неконстантни резултати, со тенденција кон кршливост и рекристализација. Во 1906 година, Вилијам Д. Кулиге поднесол патент за рендерирање на молибденски нодули , што довело до примена како елемент за греење за високотемпературни печки и како поддршка за светилки со волфрамово влакно; формирањето и деградацијата на оксиди бараат молибденот да биде физички запечатен или затворен во инертен гас. Во 1913 година, Френк Е. Елмор развил процес со флотација на пена за да изолира молибденит од руди; флотацијата останува главен процес на изолација.
За време на Првата светска војна , побарувачката за молибден се ширела; молибденот бил користен и во обложување на оклоп и како замена за волфрам во челици со голема брзина . Некои британски тенкови биле заштитени со 75 мм манган челик , но ова се покажало како неефективно. Манган челичните плочи биле заменети со многу полесни 25 милеметарски молибденски челични плочи што овозможуваат поголема брзина, поголема контрола и подобра заштита. Германците, исто така, користеле молибденски челик за тешка артилерија, како во супер-тешката хаубица Биг Берта бидејќи традиционалниот челик се топела на температурите произведени исфрлањето на едно тонскиот куршум. По војната, побарувачката опаднала сè додека металуршките достигнувања не дозволиле производство и во време на мир. Во Втората светска војна , молибден повторно станал од стратешко значење како замена за волфрам во челични легури.
Појавување и производство

Молибден е 54-от најважен елемент во Земјината кора и 25-от најзастапен елемент во океаните, со просек од 10 делчиња на милијарда; тоа е 42-тиот најважен елемент во Универзумот. Руската мисија Луна 24 открила зрно со лого на молибден (1 × 0,6 μm) во фрагмент од пироксен земен од Маре Кризиум на Месечината . Компаративната реткост на молибденот во Земјината кора е неутрализирана од нејзината концентрација во голем број на руди нерастворливи во вода, често комбинирани со сулфур на ист начин како бакар, со кој често се наоѓа. Иако молибден се наоѓа во вакви минерали како вулфенит (PbMoO 4 ) и пауелит (CaMoO 4 ), главниот комерцијален извор е молибдеитот (Mo S 2 ). Молибден е копан како главна руда и исто така се обновува како нуспроизвод од бакарското и волфрамското рударство. Производството на молибден во светот изнесувало 250.000 тони во 2011 година, а најголемите производители се Кина (94.000 т), САД (64.000 т), Чиле (38.000 т), Перу (18.000 т) и Мексико (12.000 t). Вкупните резерви се проценуваат на 10 милиони тони, и главно се концентрирани во Кина (4.3 МТ), САД (2.7 МТ) и Чиле (1.2 Mt). Застапеност по континент, 93% од светското производство на молибден е подеднакво споделено меѓу Северна Америка, Јужна Америка (главно во Чиле) и Кина. Европа и остатокот од Азија (главно Ерменија, Русија, Иран и Монголија) го произведуваат остатокот.
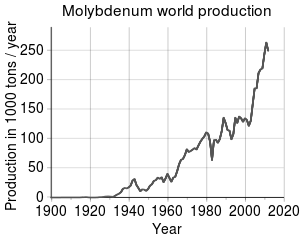
Во обработката на молибден, рудата прво се пече во воздух на температура од 700 °C (1,292 °F) . Процесот дава гасен сулфурдиоксид и молибден (VI) оксид :
- 2 MoS 2 + 7 O 2 → 2 MoO 3 + 4 SO 2
Оксидираната руда потоа обично се вади со воден амонијак за да се добие амониум молибдат:
- Moo 3 + 2 NH 3 + H 2 O → (NH 4) 2 (Moo 4)
Бакар, нечистотија во молибденот, е помалку растворлив во амонијакот. За целосно да се отстрани од растворот, тој се преципитира со сулфурводород . Амониум молибдат се претвора во амониум димолибдат , кој е изолиран како цврст материјал. Греењето на овој цврст материјал дава молибден триоксид:
- (NH 4 ) 2 Mo 2 O 7 → 2 MoO 3 + 2 NH 3 + H 2 O
Суровиот триоксид може понатаму да се прочисти со сублимација на 1,100 °C (2,010 °F) .
Металниот молибден се добива со редукција на оксидот со водород:
- Moo 3 + 3 H 2 → Mo + 3 H 2 O
Молибденот за производство на челик се намалува со алуминиумска реакција со додавање на железо за производство на феромолибден . Честата форма на феромолибден содржи 60% молибден.
Молибден има вредност од околу 30.000 долари по тон од август 2009 година. Одржувал цена од околу 10.000 долари за тон од 1997 до 2003 година и достигна врв од 103.000 долари за тон во јуни 2005 година. Во 2008 година Лондонската берза за метал најавила дека молибденот ќе се тргува како стока.
Историја на рударството со молибден
Историски, рудникот на Кнабен во јужна Норвешка, отворен во 1885 година, бил првиот рудник посветен за копање на молибден. Бил затворен во 1973 година, но повторно е отворен во 2007 година и сега произведува 100,000 килограми од молибден дисулфид годишно. Големи рудници во Колорадо (како што се рудникот Хендерсон и рудникот Климакс ) и во Британска Колумбија даваат молибден како нивниот примарен производ, додека многу порфирни бакарни наноси, како што се рудникот Кањон Бингам во Јута и рудникот Чукикамата во северниот дел на Чиле даваат молибден како нуспроизвод на рударството на бакар.
Примена
Легури

Околу 86% од произведениот молибден се користи во металургијата , а остатокот се користи во хемијата. Проценетата глобална употреба е структурен челик 35%, не’рѓосувачки челик 25%, хемикалии 14%, алати и брзи челици 9%, леано железо 6%, молибден елементарен метал 6% и суперлегури 5%.
Молибденот може да издржи екстремни температури без значително проширување или омекнување, што го прави корисен во средини со високи температури, вклучувајќи воени оклопи, делови од воздушни летала, електрични контакти, индустриски мотори и филаменти.
Повеќето челични легури со висока јачина (на пример, 41xx челици ) содржат од 0,25% до 8% молибден. Дури и во овие мали делови, секоја година се користат повеќе од 43.000 тони молибден во не’рѓосувачки челици , челици за алат , леани желези и високотемпературни суперлегури .
Молибден, исто така, е вреднуван во челичните легури за високата отпорност кон корозија и лесноста за заварување . Молибденот придонесува за отпорноста од корозија на не’рѓосувачки челици тип-300 (посебно тип-316), а особено во таканаречените супер аустентни не’рѓосувачки челици (како легури AL-6XN , 254SMO и 1925hMo). Молибденот го зголемува напонот на решетката , со што се зголемува енергијата потребна за распуштање на атомите на железо од површината. Молибден исто така се користи за подобрување на отпорноста од корозија на феритни (на пример, тип 444) и мартензитни (на пример 1.4122 и 1.4418) не’рѓосувачки челици.
Поради својата помала густина и постабилна цена, понекогаш се користи молибден наместо волфрам. Еден пример е М серијата од брзи челици, како што се М2, М4 и М42 како замена за челичната серија Т, кои содржат волфрам. Молибден, исто така, може да се користи како огно-отпорен слој за други метали. Иако неговата точка на топење е 2,623 °C (4,753 °F) , молибден брзо оксидира на температура над 760 °C (1,400 °F) што го прави подобар за употреба во вакуумски средини.
TZM (Mo (~ 99%), Ti (~ 0.5%), Zr (~ 0.08%) и некои C) е молибденска суперлегура отпорна на корозија која се спротивставува на стопените соли на флуорид на температура над 1,300 °C (2,370 °F). Таа има двапати поголема јачина во споредба со чистиот Мо, и е повеќе
нодуларна и повеќе заварувачка, но сепак во тестовите се спротивставува на корозијата на стандардна евтектичка сол ( FLiBe ) и солените пареи кои се користат во реакторите за солена вода за 1100 часа со толку мала корозија која е тешко да се измери.
Други легури засновани на молибден кои не содржат железо имаат само ограничени примени. На пример, поради неговата отпорност на стопен цинк,воедно чист молибден и молибден-волфрам легурите (70% / 30%) се користат за цевки кои доаѓаат во контакт со стопен цинк.
Други примени како чист елемент
- Молибденскиот прав се користи како ѓубриво за некои растенија, како што е карфиолот
- Елементарниот молибден се користи во NO, NO 2 , NO x анализаторите во електраните за контрола на загадувањето. На 350 °C (662 °F) , елементот делува како катализатор за NO 2 / NO x за да формираат NO молекули за детекција со инфрацрвена светлина.
- Молибденските аноди го заменуваат волфрамот во одредени нисконапонски извори на Х-зраци за специјализирани употреби, како што е мамографијата
- Радиоактивниот изотоп молибден-99 се користи за генерирање на технециум-99м , кој се користи за медицинско снимање . Изотопот се ракува и се чува како молибдат.
Соединенија (14% од глобалната употреба)
- Молибден дисулфид (MoS 2 ) се користи како цврсто мазиво и (HPHT) агент со висок притисок и вискоа температура против истрошување. Формира силни мембрани на метални површини и е чест додаток на HPHT масти - во случај на катастрофална загуба на мастите, тенок слој од молибден спречува контакт меѓу подмачкуваните делови. Исто така има полупроводнички својства со посебни предности над традиционалниот силициум или графен во електронските примени. MoS 2 исто така се користи како катализатор за хидрокрекирање на нафтени фракции кои содржат азот, сулфур и кислород.
- Молибенден дисилицид (MoSi 2 ) е електрично-проводна керамика со примарна употреба во елементи кои работат на температури над 1500 °C во воздух.
- Молибден триоксид (MoO 3 ) се користи како лепило помеѓу емајли и метали. Водечкиот молибдат (вулфенит) ко-преципитиран со оловни хромати и оловни сулфати е светло-портокалов пигмент кој се користи со керамика и пластика.
- Мешаните оксиди врз основа на молибден се разновидни катализатори во хемиската индустрија. Некои примери се катализатори за селективна оксидација на пропилен во акролеин и акрилна киселина, амоксидација на пропилен во акрилонитрил. Се испитуваат соодветни катализатори и процеси за директна селективна оксидација на пропан во акрилна киселина.
- Амониум хептамолибдат се користи при биолошко боење.
- Сончевото варово стакло обложено со молибден се користи во БИГС ( бакар индиум галиум селенид ) сончеви ќелии , наречени БИГС сончеви ќелии .
- Фосфомолибдичната киселина е дамка употребена во хроматографија со тенок слој .
Биолошка улога
Ензими кои содржат Молибден
Молибден е суштински елемент кај повеќето организми. Всушност, недостатокот на молибден во раните океани на Земјата може имало силно влијание врз еволуцијата на еукариотите(кој ги вклучува сите растенија и животни).
Најмалку 50 ензими кои содржат молибден се идентификувани, најчесто кај бактерии. овие ензими вклучуваат алдехид оксидаза , сулфит оксидаза и ксантин оксидаза. Со еден исклучок, Mo во белковините е обврзан со молибдопертерин да го даде кофакторот на молибден .
Во однос на функцијата, молибдоензимите ја катализираат оксидацијата, а понекогаш и редукција на одредени мали молекули во процесот на регулирање на азот , сулфур и јаглерод . Кај некои животни и кај луѓето, оксидацијата на ксантин во мочната киселина , процес на пурински катаболизам , е катализирана од ксантин оксидаза , ензим што содржи молибден. Активноста на ксантин оксидазата е правопропорционална на количината на молибден во телото. Сепак, екстремно високата концентрација на молибден го менува трендот и може да дејствува како инхибитор и кај пуринскиот катаболизам и во други процеси. Концентрацијата на молибден, исто така, влијае врз синтезата на белковини , метаболизмот и растот.
Молибденот е како составен дел во повеќето нитрогенази . Меѓу молибдеензимите, нитрогеназите се уникатни во недостаток на молибдопертерин. Нитрогеназите го катализираат производство на амонијак од атмосферскиот азот:
Биосинтезата на активното место FeMoco е многу комплексна.


Молибдат се транспортира во телото како MoO 4 2- .
Човечки метаболизам и дефицит
Молибден е суштински додаток во исхраната . Познати се четири ензими неопходни за цицачи, кои содржат кофактор на молибден (Моко) заснован на птерин : сулфитна оксидаза , ксантин оксидоредуктаза , алдехид оксидаза и митохондриска амидоксим редуктаза. Луѓето со силен дефицит на молибден имаат слабо функционална сулфитна оксидаза и се склони кон токсични реакции на сулфитите во храната. Човечкото тело содржи околу 0.07 mg молибден на килограм телесна тежина, со повисоки концентрации во црниот дроб и бубрезите и пониски во пршлените. Молибден исто така е присутен во човечкиот глеѓ и може да помогне да се спречи неговото распаѓање.
Акутната токсичност не е забележана кај луѓето, а токсичноста зависи од хемиската состојба. Студиите врз стаорци покажуваат средна смртоносна доза (ЛД 50 ) на најниско 180 mg / kg за некои Молибденски соединенија. Иако податоците за токсичноста кај не се достапни, испитувањата на животни покажаа дека хроничното внесување од 10 мг на ден молибден може да предизвика дијареа, попречување кај растот, неплодност, ниска родилна тежина и гихт ; исто така може да влијае на белите дробови, бубрезите и црниот дроб. Натриум волфрам е конкурентен инхибитор на молибден. Диететски волфрам ја намалува концентрацијата на молибден во ткивата.
Ниската концентрација на молибден во почвата во географски опсег од северна Кина до Иран резултира со дефицит на диететски молибден и е поврзана со зголемени стапки на рак на езофагусот . Во споредба со САД, кои имаат поголема понуда на молибден во почвата, луѓето кои живеат во овие области имаат околу 16 пати поголем ризик за езофагеален сквамозен карцином .
Дефицитот на молибден, исто така, е пријавен како последица на храна која не содржи молибден, кој ја надополнува вкупната парентерална исхрана (целосна интравенозна исхрана) за долги периоди на време. Тоа резултира со високи нивоа на сулфит и мочна киселина во крвта, на истиот начин како и недостатокот на молибденски кофактор . Сепак (веројатно затоа што дефицитот на чист молибден од оваа причина се јавува првенствено кај возрасните), невролошките последици не се толку значајни како кај случаите на вроден дефицит на кофактор.
Поврзани болести
Вродена болест на дефицит на молибденски кофактор , забележана кај доенчиња, е неможноста да се синтетизира кофикторот на молибден , хетероцикличната молекула дискутирана погоре, која го врзува молибденот на активната локација кај сите познати човечки ензими кои користат молибден. Резултирачкиот дефицит резултира со високи нивоа на сулфит и мочна киселина и невролошко оштетување.
Бакар-молибден антагонизам
Високите нивоа на молибден може да го попречат внесувањето на бакар во телото, предизвикувајќи дефицит на бакар . Молибден ги спречува плазма белковините да се врзуваат за бакар, а исто така ја зголемува количината на бакар што се екскретира во урината. Преживарите кои консумираат високо ниво на молибден страдаат од дијареа , заостанување на растот, анемија и ахромотрихија (губење на пигмент во кожата). Овие симптоми може да се ублажат со додатоци од бакар, или диететски инјекции. Делотворниот дефицит на бакар може да се влоши со вишокот на сулфур .
Редукција или дефицит на бакар, исто така, може да биде намерно индуцирана за терапевтски цели од страна на соединетиот амониум тетратиомолибдат , во кој светлоцрвениот анјон тетратиомолибдат е средство за хелатирање на бакар. Тетратиомолибдат прво се користел терапевтски во третманот на бектериска токсикоза кај животните. Таа потоа е воведена како третман во Вилсоновата болест ,кај луѓето со наследно нарушување на метаболизмот поради дефицит на бакар делува и со натпреварување со бакарна апсорпција во дебелото црево и со зголемување на екскрецијата. Исто така, е откриено дека има инхибиторен ефект врз ангиогенезата , потенцијално преку инхибиција на процесот на транслокација на мембраната кој зависи од јони на бакар. Ова е ветувачки начин за истражување на третманите за рак , макуларна дегенерација поврзана со возраста и други болести кои вклучуваат патолошка пролиферација на крвните садови.
Диететски препораки
Во 2000 година, тогашниот американски институт за медицина (сега Националната академија за медицина , NAM) ги ажурираше Проценетите просечни барања (EARs) и препорачаната исхрана (RDAs) за молибден. Доколку нема доволно информации за да се воспостават ЕАР и РДА, наместо тоа, се користи проценет назначен адекватен внес (АИ).
АИ од 2 микрограми (μg) од молибден дневно е утврдено за доенчиња до 6 месеци на , и 3 μg / ден од 7 до 12 месеци, како за мажи, така и за жени. За постари деца и возрасни, следните дневни RDAs се воспоставени за молибден: 17 μg од 1 до 3, 22 μg од 4 до 8 години, 34 μg од 9 до 13 години, 43 μg од 14 до 18 години и 45 μg за лица на возраст од 19 години и постари. Сите овие RDAs се валидни за двата пола. Бремени или лактивни жени од 14 до 50 години имаат повисока дневна RDA од 50 μg од молибден.
Што се однесува до безбедноста, NAM ги поставува толерантните вредности за внесување (ULs) за витамини и минерали кога има доволно докази. Во случај на молибден, UL е 2000 μg / ден. Колективно, EARs, RDAs, AIs и ULs се нарекуваат диететски референтни вредности (DRIs).
Европскиот орган за безбедност на храната (EFSA) се однесува на колективниот сет на информации како референтни вредности за исхраната, со референтниот внес на население (PRI) наместо RDA, и просечниот услов, наместо EAR. АИ и UL дефинирани како и во САД. За жените и мажите на возраст од 15 и повеќе години, АИ е поставена на 65 μg / ден. Бремените и доилки имаат ист АИ. За деца на возраст од 1-14 години , АИ се зголемуваат со годините од 15 на 45 μg / ден. Возрасни AIs се повисоки од американските RDAs, но од друга страна, Европската агенција за безбедност на храната го разгледа истото прашање на безбедност и го постави својот UL на 600 μg / ден, што е многу пониско од вредноста на САД.
За целите на обележување на храна во САД и на исхраната, износот во една порција се изразува како процент од дневна вредност (% ДВ). За цели на етикетирање на молибден 100% од дневната вредност беше 75 μg, но од 27 мај 2016 година беше ревидиран на 45 μg. Табела на старите и новите возрасни дневни вредности е дадена на референтното дневно внесување. Првичниот рок што требаше да се почитува беше 28 јули 2018 година, но на 29 септември 2017 година, Управата за храна и лекови (ФДА) објави предложено правило кое го продолжи крајниот рок до 1 јануари 2020 година за големите компании и 1 јануари 2021 година за мали компании.
Храна која содржи молибден
Просечниот дневен внес варира помеѓу 120 и 240 μg / ден, што е повисоко од диеталните препораки. Свинско, јагнешко и црн дроб има околу 1,5 делчиња на милион од молибден. Други значајни диететски извори вклучуваат боранија, јајца, семки од сончоглед, пченично брашно, леќа, краставици и житни зрна.
Мерки на претпазливост
Молибденските прашини и гасови, генерирани од рударството или обработката на метали, можат да бидат токсични, особено ако се внесат (вклучувајќи прашина заглавена во синусите и подоцна проголтана). Ниските нивоа на продолжено изложување може да предизвикаат иритација на очите и кожата. Треба да се избегнува директна инхалација или внесување на молибден и неговите оксиди. Прописите на OSHA ја одредуваат максималната дозволена изложеност на молибден во 8-часовен ден како 5 mg / m 3 . Хронична изложеност на 60 до 600 mg / m 3 може да предизвика симптоми, вклучувајќи замор, главоболки и болки во зглобовите. На ниво од 5000 mg / m 3 , молибденот е веднаш опасен за животот и здравјето .
Поврзано
- Список на рудници на молибден
- Рударство на молибден во САД
Наводи
Надворешни врски
| „Молибден“ на Ризницата ? |
- Молибден на Периодниот систем на видеа (Универзитет во Нотингем)
- Минерални и истражувања - Мапа на производители на светски молибден 2009
- Популарна механика "Рударство на планина", јули 1935, стр. 63-64
- Мапа за глобални информации за молибден
- CDC - NIOSH Pocket Водич за хемиски опасности
This article uses material from the Wikipedia Македонски article Молибден, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Содржината е достапна под CC BY-SA 4.0 освен ако не е поинаку наведено. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Македонски (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.

