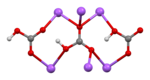
Натриум Бикарбонат: хемиско соединение
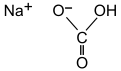
Натриум бикарбонат (име IUPAC : натриум хидрогенкарбонат), попознат како сода бикарбона или сода бикарбонат — хемиско соединение со формулата NaHCO3.
Тоа е сол составена од натриум катјон (Na+) и бикарбонат анјон (HCO3−). Натриум бикарбонат е бела цврста материја која е кристална, но често се појавува како фин прав. Има малку солен, алкален вкус кој наликува на сода за перење (натриум карбонат). Природната минерална форма е наколит. Тој е составен дел на минералот натрон и се наоѓа растворен во многу минерални извори.
 | |||
| |||
 | |||
| |||
Назив според МСЧПХ натриум хидрогенкарбонат | |||
Други називи Сода бикарбона, бикарбона (лабораториски сленг), сода бикарбона, наколит, натриум хидроген карбонат, натрон | |||
| Назнаки | |||
|---|---|---|---|
| 144-55-8 | |||
| Бајлштајн | 4153970 | ||
| ChEBI | CHEBI:32139 | ||
| ChEMBL | ChEMBL1353 | ||
| ChemSpider | 8609 | ||
| DrugBank | DB01390 | ||
| EC-број | 205-633-8 | ||
IUPHAR/BPS | 4507 | ||
| 3Д-модел (Jmol) | Слика | ||
| KEGG | C12603 | ||
| MeSH | + бикарбонат Натриум + бикарбонат | ||
| PubChem | 516892 | ||
| RTECS-бр. | VZ0950000 | ||
| |||
| UNII | 8MDF5V39QO | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Изглед | Бели кристали | ||
| Мирис | Без мирис | ||
| Густина |
| ||
| Точка на топење | |||
| |||
| Растворливост | 0.02 wt% ацетон, 2.13 wt% метанол @22 °C. нерастворлив во етанол | ||
| log P | −0.82 | ||
| Киселост (pKa) |
| ||
| Показател на прекршување (nD) | nα = 1.377 nβ = 1.501 nγ = 1.583 | ||
| Структура | |||
| Кристална структура | Monoclinic | ||
| Термохемија | |||
| Ст. енталпија на формирање ΔfH | −950.8 kJ/mol | ||
| Стандардна моларна ентропија S | 101.7 J/mol K | ||
| Специфичен топлински капацитет, C | 87.6 J/mol K | ||
| Pharmacology | |||
| ATC код | B05CB04 B05, QG04 | ||
Фармацевтски дозирани форми | Интравенозно, орално | ||
| Опасност | |||
| Безбедност при работа: | |||
Главни опасности | Предизвикува сериозна иритација на очите | ||
| NFPA 704 | |||
| Температура на запалување | {{{value}}} | ||
| Смртоносна доза или концентрација: | |||
LD50 (средна доза) | 4220 mg/kg (стаорец, орално) | ||
| Безбедносен лист | External MSDS | ||
| Слични супстанци | |||
| Други анјони | Натриум карбонат | ||
| Други катјони |
| ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||

Номенклатура
Бидејќи одамна е позната и широко користена, солта има многу различни имиња како сода бикарбона, сода за готвење или сода и често може да се најде во близина на прашокот за пециво во продавниците. Терминот сода бикарбона е почест во САД, додека бикарбона е почест во Австралија, Обединетото Кралство и Ирска а во многу северни/средноевропски земји се нарекува Натрон. Скратените разговорни форми како што се натриум бикарбона, бикарбона сода, бикарбонат се вообичаени.
Зборот saleratus, од латински sal æratus (што значи „газирана сол“), бил широко користен во 19 век и за натриум бикарбонат и за калиум бикарбонат.
Неговиот број Е за адитиви за храна е E500.
Префиксот bi во бикарбонат доаѓа од застарен систем за именување што му претходи на молекуларното знаење во однос на двата моларни еквиваленти на јаглерод диоксид (познат како јаглеродна киселина во античкиот хемиски јазик) кој калиум хидрокарбонат/бикарбонат го ослободува при распаѓање во (ди)калиум карбонат и до калиум оксид (поташа).. Современите хемиски формули на овие соединенија сега ги изразуваат нивните прецизни хемиски состави кои биле непознати кога е измислено името би-карбонат на поташа (види исто така: бикарбонат).
Употреба
Готвење
Квасец
Во готвењето, сода бикарбона првенствено се користи во печењето како квасец. Кога реагира со киселина, се ослободува јаглерод диоксид, што предизвикува проширување на тестото и ја формира карактеристичната текстура и зрно во колачи, брзи лебови, сода леб и друга печена и пржена храна. Киселинско-базната реакција може генерички да се претстави на следниов начин:
- NaHCO 3 + H + → Na + + CO 2 + H 2 O
Киселите материјали кои ја поттикнуваат оваа реакција вклучуваат водород фосфати, крем од забен камен, сок од лимон, јогурт, матеница, какао и оцет. Сода бикарбона може да се користи заедно со кисело тесто, кое е кисело, со што се добива полесен производ со помалку кисел вкус.
Топлината, исто така, може сама по себе да предизвика натриум бикарбонат да дејствува како средство за подигање при печењето поради термичко распаѓање, ослободувајќи јаглерод диоксид на температури над 80 °C (180 °F), како што следува:
- 2 NaHCO 3 → Na 2 CO 3 + H 2 O + CO 2
Кога се користи на овој начин самостојно, без присуство на кисела компонента (без разлика дали во тестото или со употреба на прашок за печиво што содржи киселина), се ослободува само половина од достапниот CO2 (се формира една молекула CO2 на секои две еквиваленти на NaHCO3). Дополнително, во отсуство на киселина, со термичко распаѓање на натриум бикарбонат се добива и натриум карбонат, кој е силно алкален и на печениот производ му дава горчлив, „сапунски“ вкус и жолта боја. Бидејќи реакцијата се случува бавно на собна температура, смесите (тестото за колачи и сл.) може да се остави да отстојат без да нараснат додека не се загреат во рерната.
Прашок за печиво
Прашокот за пециво, кој се продава и за готвење, содржи околу 30% бикарбонат и разни кисели состојки кои се активираат со додавање вода, без потреба од дополнителни киселини во медиумот за готвење. Многу форми на прашок за печиво содржат натриум бикарбонат во комбинација со калциум киселина фосфат, натриум алуминиум фосфат или крем од забен камен. Сода бикарбона е алкална; киселината што се користи во прашокот за пециво го избегнува металниот вкус кога хемиската промена за време на печењето создава натриум карбонат.
Пиротехника
Натриум бикарбонат е една од главните компоненти на обичниот огномет „црна змија“. Ефектот е предизвикан од термичкото распаѓање, кое произведува гас на јаглерод диоксид за да произведе долга змиска пепел како производ на согорување на другата главна компонента, сахарозата. Натриум бикарбонат исто така се користи за одложување на реакциите на согорување со ослободување на CO2 и H2O при загревање, од кои и двете се забавувачи на пламен.
Лесно средство за дезинфекција
Има слаби својства за дезинфекција, и може да биде ефикасен фунгицид против некои организми. Бидејќи сода бикарбона ги апсорбира мирисите на мувлосана, таа стана сигурен метод за продавачите на користени книги кога ги прават книгите помалку непријатни.
Противпожарен апарат
Натриум бикарбонат може да се користи за гаснење на мали маснотии или електрични пожари со фрлање над огнот, бидејќи загревањето на натриум бикарбонат ослободува јаглерод диоксид. Сепак, не треба да се применува на оган во фритези; ненадејното ослободување на гас може да предизвика прскање на маснотиите. Натриум бикарбонат се користи во суви хемиски противпожарни апарати BC како алтернатива на покорозивниот моноамониум фосфат во ABC апаратите за гаснење пожар. Алкалната природа на натриум бикарбонат го прави единствениот сув хемиски агенс, покрај Purple-K, кој се користел во големи системи за сузбивање пожар инсталирани во комерцијални кујни. Бидејќи може да делува како алкали, агенсот има благ сапонифицирачки ефект врз топлата маст, што формира задушувачка, сапунска пена.
Неутрализација на киселини
Натриум бикарбонат спонтано реагира со киселини, ослободувајќи CO2 гас како производ на реакција . Најчесто се користи за неутрализирање на несакани киселински раствори или излевање на киселина во хемиски лаборатории. Не е соодветно да се користи натриум бикарбонат за неутрализирање на базата иако е амфотерична, реагирајќи и со киселини и со бази.
Земјоделство
Натриум бикарбонат кога се нанесува на листовите може да го спречи растот на габите; сепак, не ја убива габата. Прекумерната количина на натриум бикарбонат може да предизвика обезбојување на овошјето (два проценти раствор) и хлороза (еден процентен раствор).
Медицинска употреба и здравје
Натриум бикарбонат измешан со вода може да се користи како антацид за лекување на киселинско варење и горушица. Неговата реакција со стомачната киселина произведува сол, вода и јаглерод диоксид:
- NaHCO 3 + HCl → NaCl + H 2 O + CO 2 (g)
Мешавина од натриум бикарбонат и полиетилен гликол, како што е PegLyte, растворена во вода и земена орално, е ефикасен препарат за гастроинтестинална лаважа и лаксатив пред операција на гастроинтестиналниот тракт, гастроскопија итн.
Интравенска администрација на натриум бикарбонат во воден раствор понекогаш се користи за случаи на ацидоза, или кога нема доволно натриум или бикарбонат јони во крвта. Во случаи на респираторна ацидоза, инфузираниот бикарбонат јон го придвижува пуферот на јаглеродна киселина/бикарбонат на плазмата налево, и на тој начин ја зголемува pH вредноста. Поради оваа причина, натриум бикарбонат се користи во кардиопулмонална реанимација под медицински надзор. Инфузија на бикарбонат е индицирана само кога pH на крвта е значително ниска ( < 7,1-7,0).
HCO3- се користи за третман на хиперкалемија, бидејќи ќе го врати K+ во клетките за време на периоди на ацидоза. Бидејќи натриум бикарбонат може да предизвика алкалоза, понекогаш се користи за лекување на предозирање со аспирин. Аспиринот бара кисела средина за правилна апсорпција, а основната средина ќе ја намали апсорпцијата на аспирин во случаи на предозирање. Натриум бикарбонат исто така се користи во третман на предозирање со трициклични антидепресиви. Може да се нанесува и локално како паста, со три дела сода бикарбона во еден дел вода, за да се ублажат некои видови каснувања и убоди од инсекти (како и придружниот оток).
Некои алтернативни практичари, како што е Тулио Симончини, ја промовирале сода бикарбоната како лек за рак, на што предупредило Американското здружение за рак поради нејзината недокажана ефикасност и потенцијална опасност при употреба. Еџард Ернст ја нарекол промоцијата на натриум бикарбонат како лек за рак „една од поболните алтернативни измами за рак што сум ги видел долго време“.
Натриум бикарбонат може да се додаде во локалните анестетици, за да се забрза почетокот на нивните ефекти и да се направи нивното инјектирање помалку болно. Тоа е, исто така, компонента на Мофетовиот раствор, кој се користи во назална хирургија.
Предложено е дека киселите диети ги ослабуваат коските. Една систематска мета-анализа на истражувањето не покажува таков ефект. Друг, исто така, открива дека нема докази дека алкалните диети го подобруваат здравјето на коските, но сугерира дека „можеби има одредена вредност“ на алкалните диети поради други причини.
Растворите за антациди (како сода бикарбона) се подготвени и користени од демонстрантите за да се ублажат ефектите од изложеноста на солзавец за време на протестите.
Слично на неговата употреба во печењето, натриум бикарбонат се користи заедно со блага киселина како што е винската киселина како помошна супстанција во шумливи таблети: кога таквата таблета ќе се падне во чаша вода, карбонатот го остава медиумот за реакција како гас јаглерод диоксид (HCO3− + H+ → H2O + CO2 ↑ или, поточно, HCO3− + H3O + → 2H2O + CO2 ↑). Ова го прави таблетот да се распадне, оставајќи го лекот суспендиран и/или растворен во водата заедно со добиената сол (во овој пример, натриум тартарат).
Лична хигиена
Натриум бикарбонат исто така се користи како состојка во некои плакнења за уста. Има антикариозни и абразивни својства. Работи како механичко чистење на забите и непцата, го неутрализира производството на киселина во устата, а делува и како антисептик за спречување на инфекции. Натриум бикарбонат во комбинација со други состојки може да се користи за да се направи сув или влажен дезодоранс. Натриум бикарбонат може да се користи како пуферско средство, во комбинација со кујнска сол.
Се користи во хигиената на очите за лекување на блефаритис . Ова се прави со додавање на лажичка натриум бикарбонат во изладената вода што неодамна е зовриена, проследено со нежно чистење на основата на трепките со памучно стапче натопено во растворот.
Ветеринарна употреба
Натриум бикарбонат се користи како додаток за добиточна храна, особено како пуферски агенс за бурагот.
Средство за чистење
Натриум бикарбонат се користи во процес за отстранување на боја и корозија наречен содабластирање. Како медиум за минирање, натриум бикарбонат се користи за отстранување на површинската контаминација од помеки и помалку еластични подлоги како што се алуминиум, бакар или дрва кои можат да бидат оштетени од абразивни медиуми од силика песок.
Производителот препорачува паста направена од сода бикарбона со минимална вода како нежен прашок за чистење, и е корисна за отстранување на површинската 'рѓа, бидејќи 'рѓата формира соединение растворливо во вода кога е во концентриран алкален раствор; Треба да се користи ладна вода, бидејќи растворите за топла вода може да го кородираат челикот. Натриум бикарбонат го напаѓа тенкиот заштитен оксиден слој што се формира на алуминиум, што го прави несоодветен за чистење на овој метал. Растворот во топла вода ќе го отстрани оцрнувањето од среброто кога среброто е во контакт со парче алуминиумска фолија . Сода бикарбона најчесто се додава во машините за перење како замена за омекнувач на вода и за отстранување на мирисите од облеката. Исто така е речиси исто толку ефикасен во отстранувањето на тешките дамки од чај и кафе од шолјите како натриум хидроксид, кога се разредува со топла вода.
За време на проектот Менхетен за развој на јадрена бомба во раните 1940-ти, хемиската токсичност на ураниумот претставувала проблем. Утврдено е дека оксидите на ураниум многу добро се лепат на памучна ткаенина и не се мијат со сапун или детергент за перење. Сепак, ураниумот ќе се измие со 2% раствор на натриум бикарбонат. Облеката може да се контаминира со токсична прашина од осиромашен ураниум (DU), која е многу густа, па затоа се користи за противтегови во цивилен контекст и во проектили кои пробиваат оклоп. DU не се отстранува со нормално перење; миењето со околу 6 унци (170 g) сода бикарбона во 2 литри (7,5 L) вода ќе помогне да се измие.
Контрола на мирис
Често се тврди дека сода бикарбона е ефикасен отстранувач на мирис, и често се препорачува да се чува отворена кутија во фрижидер за да се апсорбира мирис. Оваа идеја била промовирана од водечкиот американски бренд на сода бикарбона, Arm & Hammer, во рекламна кампања која започна во 1972 година Иако оваа кампања се смета за класика на маркетингот, што води во рок од една година повеќе од половина од американските фрижидери да содржат кутија сода бикарбона, има малку докази дека е всушност ефикасна во оваа апликација.
Производство на водороден гас
Натриум бикарбонат може да се користи како катализатор во производството на гас. Неговите перформанси се „добри“, но вообичаено не се користат. Водородниот гас се произведува преку електролиза на вода, процес во кој се применува електрична струја низ волумен на вода, што предизвикува атомите на водород да се одвојат од атомите на кислород. Оваа демонстрација обично се прави на часовите по хемија во средно училиште за да се покаже електролиза .
Хемија
Натриум бикарбонат е амфотерно соединение. Водните раствори се благо алкални поради формирање на јаглеродна киселина и хидроксид јон:
HCO−
3 + H2O → H2CO3 + OH−
Натриум бикарбонат често може да се користи како побезбедна алтернатива на натриум хидроксид, и како таков може да се користи како миење за да се отстранат сите киселински нечистотии од „сурова“ течност, со што се добива почист примерок. Од реакцијата на натриум бикарбонат и киселина се добива сол и јаглеродна киселина, која лесно се распаѓа на јаглерод диоксид и вода:
- NaHCO 3 + HCl → NaCl + H 2 O + CO 2
- H 2 CO 3 → H 2 O + CO 2 (g)
Натриум бикарбонат реагира со оцетна киселина (се наоѓа во оцетот), произведувајќи натриум ацетат, вода и јаглерод диоксид:
- NaHCO 3 + CH 3 COOH → CH 3 COONa + H 2 O + CO 2 (g)
Натриум бикарбонат реагира со бази како натриум хидроксид за да формира карбонати:
- NaHCO 3 + NaOH → Na 2 CO 3 + H 2 O
Термичко распаѓање
На температури од 80-100 °C (176–212 °F), натриум бикарбонат постепено се распаѓа на натриум карбонат, вода и јаглерод диоксид. Конверзијата е побрза на 200 °C (392 °F) :
- 2 NaHCO 3 → Na 2 CO 3 + H 2 O + CO 2
Повеќето бикарбонати се подложени на оваа реакција на дехидрација . Понатамошното загревање го претвора карбонатот во оксид (над 850 С/1,560 F ):
- Na 2 CO 3 → Na 2 O + CO 2
Овие конверзии се релевантни за употребата на NaHCO 3 како средство за сузбивање пожар („BC прав“) во некои противпожарни апарати со сув прав.[се бара извор]
Стабилност и рок на траење
Доколку се чува ладен (собна температура) и сув (се препорачува херметички сад за да не излегува влажен воздух), натриум бикарбонат може да се чува без значителна количина на распаѓање најмалку две или три години.
Историја
Зборот натрон бил во употреба во многу јазици во текот на современото време (во формите на анатрон, натрум и натрон) и настанал (како шпански, француски и англиски natron како и „ натриум“) преку арапскиот naṭrūn (или anatrūn; сп. долноегипетскиот „Натронтал“ Вади Ел Натрун, каде што се користела мешавина од натриум карбонат и натриум хидроген карбонат за дехидрација на мумиите ) од грчки нитрон (νίτρον) (Херодот; тавански lítron (λίτρον) ), што може да се потекнува од древниот египетски ntr . Грчкиот нитрон (сода, шалитра) се користел и во латинскиот (sal) nitrum и во германскиот Salniter (изворот на азот, нитрат итн. ).
Во 1791 година, францускиот хемичар Николас Лебланк произвел натриум карбонат, исто така познат како сода пепел. Фармацевтот Валентин Роуз Помладиот е заслужен за откривањето на натриум бикарбонат во 1801 година во Берлин. Во 1846 година, двајца американски пекари, Џон Двајт и Остин Черч, ја основале првата фабрика во САД за производство на сода бикарбона од натриум карбонат и јаглерод диоксид.
Салератус, калиум или натриум бикарбонат, се споменува во романот „Капетани храбри“ од Радјард Киплинг како интензивно користен во 1800-тите во комерцијален риболов за да се спречи расипување на свежо уловената риба.
Во 1919 година, американскиот сенатор Ли Оверман изјавил дека сода бикарбона може да го излечи шпанскиот грип. Во средината на дебатата на 26 јануари 1919 година, тој ја прекинал дискусијата за да го објави откривањето на лекот. „Сакам да кажам, во корист на оние кои ја водат оваа истрага“, изјавил тој, „дека судијата на надреден суд во планинската земја Северна Каролина ми кажа дека откриле лек за оваа болест“. Наводниот лек подразбира критика на модерната наука и благодарност за едноставната мудрост на едноставните луѓе. „Велат дека обичната сода бикарбона ќе ја излечи болеста“, продолжил тој, „дека ја излечиле со неа, дека воопшто немаат смртни случаи таму горе; користат обична сода бикарбона, која ја лекува болеста“.
Производство
Натриум бикарбонат се произведува индустриски од натриум карбонат:
- Na 2 CO 3 + CO 2 + H 2 O → 2 NaHCO 3
Се произведува на скала од околу 100.000 тони годишно (од 2001 година) со светски производствен капацитет од 2,4 милиони тони годишно (од 2002 година). Со сличен метод се произведуваат и комерцијални количини сода бикарбона: сода пепел, ископана во форма на руда трона, се раствора во вода и се третира со јаглерод диоксид. Натриум бикарбонат се таложи како цврста супстанца од овој раствор.
Што се однесува до процесот на Солвеј, натриум бикарбонат е посредник во реакцијата на натриум хлорид, амонијак и јаглерод диоксид . Сепак, производот покажува ниска чистота (75 парчиња).
Иако нема практична вредност, NaHCO 3 може да се добие со реакција на јаглерод диоксид со воден раствор на натриум хидроксид:
- CO 2 + NaOH → NaHCO 3
Рударство
Природните депозити на наколит (NaHCO3) се пронајдени во еоценската возраст (55,8-33,9 Mya) на Формација Зелена река во Колорадо. Наколитот се депонирал како корита за време на периоди на високо испарување во сливот. Комерцијално се ископува со користење на вообичаени техники на подземно ископување, како што се копани, барабан и ископување со долг ѕид на начин многу сличен на ископувањето јаглен.
Се произведува и со ископување раствор, пумпање на загреана вода низ наколитните кревети и кристализирање на растворениот наколит преку процес на кристализација на ладење.
Во популарната култура
Натриум бикарбонат, како „сода бикарбона“, бил чест извор на удари за Гручо Маркс во филмовите на Браќата Маркс. Во Duck Suup, Маркс го игра водачот на нацијата во војна. Во една сцена, тој добива порака од бојното поле дека неговиот генерал известува за напад со гас, а Гручо му кажува на својот помошник: „Кажи му да земе лажичка сода бикарбона и половина чаша вода“. Во „Ноќ во операта“, ликот на Гручо се обраќа на публиката на отворањето на операта велејќи за главниот тенор: „Сињор Ласпари потекнува од многу познато семејство. Неговата мајка беше добро позната бас пејачка. Неговиот татко бил првиот човек кој наполнил шпагети со сода бикарбона, со што во исто време предизвикувал и лекувал варење.“
Во класиката на Џозеф Ел . . Ченинг ветува дека секогаш ќе чува кутија бикарбона со името на Макс.
Наводи
Надворешни врски
| „Натриум бикарбонат“ на Ризницата ? |
| Wikibooks Cookbook has a recipe/module on |
This article uses material from the Wikipedia Македонски article Натриум бикарбонат, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Содржината е достапна под CC BY-SA 4.0 освен ако не е поинаку наведено. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Македонски (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.