Хемија На Аскорбинска Киселина
Аскорбинската киселина е органско соединение со формула C6H8O6 C6H8O6 C6H8O6 C6H8O6, првично наречена хексуронска киселина.
Тоа е бело цврсто тело, но нечистите примероци може да изгледаат жолтеникави. Добро се раствора во вода за да даде благо кисели раствори. Тоа е благо редуцирачки агенс .
Аскорбинската киселина постои како два енантиомери ( изомери со огледална слика), вообичаено означени "l " (за "лево") и "d " (за "декстро"). На l изомерот е оној што најчесто се среќава: природно се наоѓа во многу намирници и е една форма („ витамер “) на витамин Ц, суштинска хранлива материја за луѓето и многу животни. Недостатокот на витамин Ц предизвикува скорбут, порано главна болест на морнарите при долгите морски патувања. Се користи како додаток на храна и додаток во исхраната поради неговите антиоксидантни својства. Формата "d " може да се направи преку хемиска синтеза, но нема значајна биолошка улога.
Историја
Антискорбутичните својства на одредени намирници биле демонстрирани во 18 век од страна на Џејмс Линд. Во 1907 година, Аксел Холст и Теодор Фролих откриле дека антискорбутичниот фактор е хемиска супстанца растворлива во вода, различна од онаа што спречува бери-бери. Помеѓу 1928 и 1932 година, Алберт Сент-Ѓерги изолирал кандидат за оваа супстанца, која ја нарекол „хексуронска киселина“, прво од растенија, а подоцна и од животински надбубрежни жлезди. Во 1932 година , Чарлс Глен Кинг потврдил дека тоа навистина е антискорбутичен фактор.
Во 1933 година, хемичарот за шеќер Волтер Норман Хаворт, работејќи со примероци од „хексуронска киселина“ што Шент-Ѓерги ја изолирал од пиперката и му ја испратил претходната година, ја заклучил точната структура и оптичко-изомерната природа на соединението, а во 1934 година објавил неговата прва синтеза. Во врска со антискорбутните својства на соединението, Хаворт и Шент-Ѓерги предложија да се преименува во „а-скорбинска киселина“ за соединението, а подоцна конкретноl -аскорбинска киселина. Поради нивната работа, во 1937 година Нобеловите награди за хемија и медицина беа доделени на Хаворт и Шент-Ѓерги, соодветно.
Хемиски својства
Киселост
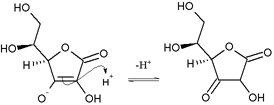
Аскорбинската киселина е лактон базиран на фуран и го формира аскорбатниот анјон кога се депротонира на еден од хидроксилите. Ова својство е карактеристично за редуктоните : ендиоли со карбонилна група во непосредна близина на групата ендиол, имено со групата −C(OH)=C(OH)−C(=O)−. Аскорбатниот анјон се стабилизира со електронска делокализација што е резултат на резонанца помеѓу две форми:
Поради оваа причина, аскорбинската киселина е многу покисел отколку што би се очекувало ако соединението содржи само изолирани хидроксилни групи.
Соли
Аскорбатниот анјон формира соли, како што се натриум аскорбат, калциум аскорбат и калиум аскорбат .
Естери
Аскорбинската киселина, исто така, може да реагира со органски киселини како естери кои формираат алкохол, како што се аскорбил палмитат и аскорбил стеарат .
Нуклеофилен напад
Нуклеофилниот напад на аскорбинска киселина врз протон резултира со 1,3-дикетон:
Оксидација


Аскорбатниот јон е доминантен вид при типични биолошки pH вредности. Тоа е благо редуцирачки агенс и антиоксиданс. Се оксидира со губење на еден електрон за да се формира радикален катјон, а потоа со губење на втор електрон за да се формира дехидроаскорбинска киселина. Обично реагира со оксиданти од реактивните видови кислород, како што е радикалот хидроксил .
Аскорбинската киселина е посебна затоа што може да пренесе еден електрон, благодарение на природата стабилизирана со резонанца на сопствениот радикален јон, наречен полудехидроаскорбат. Нето реакцијата е:
- RO • + C6H7O−
6 C6H7O−
6 C6H7O−
6 C6H7O−
6 → RO − + C 6 H 7 O • • → ROH + C 6 H 6 O 6
При изложеност на кислород, аскорбинската киселина ќе претрпи дополнително оксидативно распаѓање на различни производи, вклучувајќи ги дикетогулонска киселина, ксилонска киселина, треонска киселина и оксална киселина .
Реактивните видови кислород се штетни за животните и растенијата на молекуларно ниво поради нивната можна интеракција со нуклеинските киселини, белковините и липидите. Понекогаш овие радикали иницираат верижни реакции. Аскорбат може да ги прекине овие верижни радикални реакции со пренос на електрони. Оксидираните форми на аскорбат се релативно нереактивни и не предизвикуваат клеточно оштетување.
Како и да е, како добар донатор на електрони, вишокот аскорбат во присуство на слободни метални јони не само што може да промовира, туку и да иницира реакции на слободните радикали, што го прави потенцијално опасно прооксидативно соединение во одредени метаболички контексти.
Аскорбинската киселина и нејзините соли на натриум, калиум и калциум најчесто се користат како антиоксидантни прехранбени адитиви. Овие соединенија се растворливи во вода и затоа не можат да ги заштитат мастите од оксидација: За таа цел, естрите растворливи во масти на аскорбинска киселина со долги масни киселини (аскорбил палмитат или аскорбил стеарат) може да се користат како антиоксиданти за храна.
Други реакции
Создава испарливи соединенија кога се меша со гликоза и аминокиселини во 90 °C.
Тој е кофактор во оксидацијата на тирозин .
Користење
Додаток за храна
Главната употреба наl аскорбинска киселина и нејзините соли е како адитиви за храна, најмногу за борба против оксидацијата. Тој е одобрен за оваа намена во ЕУ со Е број E300, САД, Австралија и Нов Зеланд.
Додаток во исхраната
Друга голема употреба наl аскорбинска киселина е како додаток во исхраната .
Ниша, непрехранбени употреби
- Аскорбинската киселина лесно се оксидира и затоа се користи како редуктор во растворите за фотографирање (меѓу другите) и како конзерванс .
- Во флуоресцентната микроскопија и сродните техники засновани на флуоресценција, аскорбинската киселина може да се користи како антиоксиданс за да се зголеми флуоресцентниот сигнал и хемиски да се забави фотобелењето на бојата.
- Исто така, најчесто се користи за отстранување на растворени метални дамки, како што е железото, од површините на базените со фиберглас.
- Во производството на пластика, аскорбинската киселина може да се користи за побрзо склопување на молекуларни синџири и со помалку отпад отколку традиционалните методи на синтеза.
- Познато е дека корисниците на хероин користат аскорбинска киселина како средство за претворање на хероинската база во сол растворлива во вода за да може да се инјектира.
- Како што е оправдано со неговата реакција со јод, се користи за негирање на ефектите на јодните таблети при прочистување на водата. Тој реагира со стерилизираната вода, отстранувајќи го вкусот, бојата и мирисот на јодот. Ова е причината зошто често се продава како втор сет таблети во повеќето продавници за спортска опрема како таблети за неутрализирање на аква, заедно со таблетите на калиум јодид.
- Интравенозните високи дози на аскорбат се користат како хемотерапевтски и биолошки агенс за модифицирање на одговорот . Во моментов сè уште е во клинички испитувања.
- Понекогаш се користи како уринарен закиселувач за подобрување на антисептичното дејство на метенаминот .
Синтеза
Природната биосинтеза на витаминот Ц се јавува кај многу растенија и животни, со различни процеси.
Индустриска подготовка
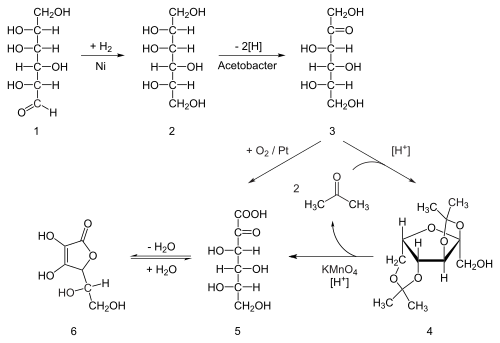
Осумдесет проценти од светската понуда на аскорбинска киселина се произведува во Кина. Аскорбинската киселина се подготвува во индустријата од гликоза на метод базиран на историскиот процес на Рајхштајн. Во првиот процес од пет чекори, гликозата каталитички се хидрогенизира до сорбитол, кој потоа се оксидира од микроорганизмот Acetobacter субоксиданс во сорбоза. Само една од шесте хидрокси групи се оксидира со оваа ензимска реакција. Од оваа точка, достапни се две правци. Третманот на производот со ацетон во присуство на киселински катализатор претвора четири од преостанатите хидроксилни групи во ацетали. Незаштитената хидроксилна група се оксидира до карбоксилна киселина со реакција со каталитичкиот оксиданс TEMPO (регенериран од натриум хипохлорит – раствор за белење ). Историски гледано, индустриската подготовка преку процесот на Рајхштајн користела калиум перманганат како раствор за белење. Киселински катализирана хидролиза на овој производ врши двојна функција на отстранување на двете ацетални групи и лактонизација со затворање на прстенот. Овој чекор дава аскорбинска киселина. Секој од петте чекори има принос поголем од 90%.
Побиотехнолошкиот процес, првпат развиен во Кина во 1960-тите, но дополнително развиен во 1990-тите, ја заобиколува употребата на групи за заштита на ацетон. Вториот генетски модифициран вид микроб, како што е мутантот Erwinia, меѓу другите, ја оксидира сорбозата во 2-кетоглуконска киселина (2-KGA), која потоа може да претрпи лактонизација со затворање на прстенот преку дехидрација. Овој метод се користи во доминантниот процес што го користи индустријата за аскорбинска киселина во Кина, која обезбедува 80% од светската аскорбинска киселина. Американските и кинеските истражувачи се натпреваруваат за инженерство на мутант кој може да изврши ферментација во едно тенџере директно од гликоза до 2-KGA, заобиколувајќи ја и потребата за втора ферментација и потребата да се намали гликозата до сорбитол.
Постои аd -аскорбинска киселина, која не се јавува во природата, но може да се синтетизира вештачки. Да бидам конкретен,lПознато е дека -аскорбат учествува во многу специфични ензимски реакции кои бараат точен енантиомер (l -аскорбат и неd -аскорбат).l -Аскорбинска киселина има специфична ротација од [α] 20 20 = +23°.
Определување
Традиционалниот начин за анализа на содржината на аскорбинска киселина е процесот на титрација со оксидирачки агенс и развиени се неколку процедури.
Популарниот пристап на јодометрија користи јод во присуство на индикатор за скроб. Јодот се намалува со аскорбинска киселина, и кога целата аскорбинска киселина реагира, тогаш јодот е во вишок, формирајќи сино-црн комплекс со индикаторот за скроб. Ова ја покажува крајната точка на титрацијата.
Како алтернатива, аскорбинската киселина може да се третира со вишок на јод, проследено со назад титрација со натриум тиосулфат користејќи скроб како индикатор.
Овој јодометриски метод е ревидиран за да се искористи реакцијата на аскорбинска киселина со јодат и јодид во киселински раствор. Со електролиза на растворот на калиум јодид се добива јод, кој реагира со аскорбинска киселина. Крајот на процесот се одредува со потенциометриска титрација на начин сличен на титрацијата на Карл Фишер. Количината на аскорбинска киселина може да се пресмета со законот на Фарадеј .
Друга алтернатива користи N -бромосуцинимид (NBS) како оксидирачки агенс, во присуство на калиум јодид и скроб. НБС прво ја оксидира аскорбинската киселина; кога вториот е исцрпен, NBS го ослободува јодот од калиум јодидот, кој потоа го формира сино-црниот комплекс со скроб.
Наводи
This article uses material from the Wikipedia Македонски article Хемија на аскорбинска киселина, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Содржината е достапна под CC BY-SA 4.0 освен ако не е поинаку наведено. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Македонски (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.