ایندیم: یکی از عنصرهای جدول تناوبی عنصرها
ایندیوم (Indium) از عنصرهای شیمیایی جدول تناوبی است.
نشانه کوتاه آن In و عدد اتمی آن ۴۹ است. ایندیوم یک فلز نرم سفید نقرهای است و در برابر آب و هوا پایدار است. این فلز شبیه قلع است. ازنظر شیمیایی مشابه آلومینیوم و گالیوم است؛ امّا از نظر ظاهری بیشتر شبیه روی میباشد. ایندیوم نرمترین فلزی است که قلیایی نیست و نقطه ذوب آن از گالیم و سدیم بیشتر است ولی از لیتیم و قلع کمتر است.
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایندیم | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| تلفظ | /ˈɪndiəm/ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ظاهر | silvery lustrous gray | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| جرم اتمی استاندارد (Ar، استاندارد) | ۱۱۴٫۸۱۸(۱) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایندیم در جدول تناوبی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اتمی (Z) | 49 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| گروه | گروه ۱۳ (گروه بور) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دوره | دوره 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| بلوک | بلوک-p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دسته | Post-transition metal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آرایش الکترونی | [Kr] 4d10 5s2 5p1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2, 8, 18, 18, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای فیزیکی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| فاز در STP | جامد | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه ذوب | 429.7485 K (156.5985 °C, 313.8773 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه جوش | 2345 K (2072 °C, 3762 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| چگالی (near r.t.) | 7.31 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| در حالت مایع (at m.p.) | 7.02 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارت همجوشی | 3.281 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آنتالپی تبخیر | 231.8 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ظرفیت حرارتی مولی | 26.74 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
فشار بخار
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای اتمی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اکسایش | −5, −2, −1, +1, +2, +3 (an amphoteric اکسید) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الکترونگاتیوی | مقیاس پائولینگ: 1.78 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انرژی یونش |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع اتمی | empirical: 167 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع کووالانسی | pm 142±5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع واندروالسی | 193 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دیگر ویژگی ها | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
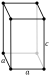
| ساختار بلوری | چهارگوشه | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سرعت صوت thin rod | 1215 m/s (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انبساط حرارتی | 32.1 µm/(m·K) (at 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانندگی گرمایی | 81.8 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش الکتریکی | 83.7 n Ω·m (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش مغناطیسی | دیامغناطیس | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول یانگ | 11 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی موس | 1.2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی برینل | 8.83 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شماره ثبت سیایاس | 7440-74-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایزوتوپهای ایندیم | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


خواص
- عدد اتمی: ۴۹ با آرایش الکترونی Kr] 4d105s25p1] که دوست دارد سه الکترون از دست بدهد و به ایندیوم(III) تبدیل شود ولی در بعضی حالتها فقط یک الکترون از دست میدهد و به ایندیوم(I) تبدیل میشود.
- جرم اتمی: ۱۱۴٫۸۲
- نقطه ذوب: C° ۱۵۶٫۶ (از همولوگ سبک خوب یعنی گالیم بیشتر و از همولوگ سنگین خوب یعنی تالیوم و قلع کمتر است.)
- نقطه جوش: C° ۲۰۷۲ (بیشتر از نقطه جوش تالیوم و کمتر از نقطه جوش گالیم است.)
- چگالی: ۷٫۳۱g/cm3 (از گالیم بیشتر و از تالیوم کمتر است)
- شعاع اتمی: ۲A
- ظرفیت: ۱و۲و۳
- حالت استاندارد: جامد
- ایزوتوپها: ۳۹ ایزوتوپ شناختهشده با عدد جرمی ۹۷ تا ۱۳۵ دارد.
ایندیم فلز سفید رنگ و بسیار نرمی است که با چاقو بریده میشود و دارای سطحی درخشان میباشد. این فلز اگر خالص باشد هنگام خم شدن تولید صدایی ممتد و زیر میکند. ایندیم را بیشتر از پسماندهایی که در طول پردازش سنگ معدن روی بجا ماندهاست، تولید میکنند، اما در سنگ معدن آهن، سرب و مس نیز یافت میشود.
ایندیوم با آب واکنش نمیدهد ولی این ماده توسط اکسیدکنندههای قویتری مانند هالوژنها اکسید میشود و ترکیبات ایندیوم (III) به دست میآید.
خاصیت ویژه و غیرمعمول آن، این است که در دمای بسیار پایین نرم و قابل کار میماند.
ایندیوم هیچ نقش بیولوژیکی شناختهشدهای ندارد. اگر بیشاز چند میلیگرم مصرف شود سمی است و میتواند روی رشد جنین تأثیر بگذارد.
تاریخچه
ایندیوم در سال ۱۸۶۳ توسط دو شیمیدان آلمانی به نامهای فردیناند رچ(ferdinand reich) و تئودور ریچر(hieronymous theodoe richter) کشف شد. ریچر در جستجوی عنصر تالیم در کانیهای روی بود، که با مشاهده یک خط نیلی رنگ براق در طیفسنجی نمونهها به وجود ایندیوم پی برد. نام ایندیوم از آبی نیلی نشأت گرفتهاست.

ایندیوم از لحاظ فراوانی همانند نقره است ولی بسیار سادهتر از نقره بازیابی میشود و معمولاً همراه کانیهای آهن، سرب و مس میباشد.
فراوانی در طبیعت
ایندیوم یکی از کمترین مواد معدنی موجود در زمین است. این ماده در طبیعت غیر ترکیبی یافت شدهاست، امّا بهطور معمول در ارتباط با مواد معدنی روی و سنگ معدن آهن، سرب و مس یافت میشود. ایندیوم به عنوان محصول جانبی تصفیهٔ روی بهصورت تجاری تولید میشود.
تولید جهانی عمدتاً از کانادا انجام میشود و حدود ۷۵ تن در سال است، ذخایر این فلز بیش از ۱۵۰۰تن تخمین زده میشود.
کاربرد
عمده کاربرد ایندیوم در ساخت لایههای نازکی است که از آنها بهعنوان لایههای روغنکاری شده استفاده میشود. بیشترین مقدار ایندیوم مصرف شده مربوط به تولید جهانی LCD است.
اولین برنامهٔ کاربردی در مقیاس بزرگ از ایندیوم، در زمان جنگ جهانی دوم بود که کارایی موتورهای هواپیمایی را بالا میبرد تا از آسیب و خوردگی محافظت کند. البته امروزه کاربرد ایندیوم به این شکل رایج نیست.
بعدها کاربردهای بیشتری برای آن در آلیاژها، لحیمها و علم الکترونیک یافت شد و تولید آن بهتدریج افزایش یافت.
در اواسط و اواخر دهه ۹۰ تولید نیمههادیهای فسفید ایندیم و لایههای نازک اکسید ایندیم – قلع برای liquid crystal displays یعنی همان LCD بیشتر مورد توجه قرار گرفت. تا پایان سال ۱۹۹۲ این لایههای نازک عمدهترین کاربرد این عنصر بود.
از دیگر کاربردهای آن میتوان به موارد زیر اشاره کرد:
- در ساخت آلیاژهای با نقطه ذوب پایین کاربرد دارد. آلیاژی که حاوی ۲۴٪ ایندیم و ۷۶٪ گالیم میباشد، در دمای اتاق به حالت مایع است.
- برای ساخت نور رسانها، ژرمانیم، ترانزیستور، دیودها و دمایابها بکار میرود.
- از آن میتوان برای روکش فلزات استفاده کرد و با بخار آن روی شیشه، تولید آیینههایی نمود که به همان خوبی آیینههای ساخته شده با نقره است، اما در مقابل فرسایش مقاومت بیشتری دارد.
- اکسید آن برای ساخت صفحات کلید (Panels) برق درخشی (electroluminescent) مورد استفاده میباشد.
- در صنعت جواهرسازی از این عنصر برای ایجاد سختی و ایجاد جلا و شفافیت استفاده میشود. البته به علت اختلاف زیاد بین دمای ذوب و دمای تبخیر و پایین بودن دمای ذوب برای جلوگیری از سوخت شدن و تغییر ندادن عیار طلا مورد استفاده قرار میگیرد.
- خاصیت غیرمعمولی دارد که در دمای بسیار پایین نرم و قابل ماشینکاری میماند. این ویژگی اجازه میدهد تا از آن در تجهیزات ویژهٔ مورد نیاز در دمای نزدیک به صفر مطلق استفاده شود. این یک انتخاب عالی برای پمپهای برودتی، سیستمهای با خلأ زیاد و سایر کاربردهای اتصال و مهر و موم منحصر به فرد است.
- یکی دیگر از موارد مهم استفاده از ایندیوم در ساخت آلیاژها است که در دستگاههای الکترونیکی و مواد مورد استفاده در دندان پزشکی استفاده میشود. ایندیم را در آلیاژها "ویتامین فلزی" مینامند، به این معنی که مقادیر بسیار کمی از ایندیم میتواند تغییرات بزرگی در آلیاژ ایجاد کند. به عنوان مثال، افزودن مقدار کمی ایندیم به آلیاژهای طلا و پلاتین، آنها را بسیار سختتر میکند.
- برخی از قطعات هواپیما از آلیاژهای حاوی ایندیوم ساخته شدهاند و از واکنش آنها با اکسیژن هوا یا فرسودگی آنها جلوگیری میکند.

استفادههای نوین از ایندیوم عبارتند از:
- در صنایع نیمه هادی
- در لحیمکاری
- در مهر و مومهای فلزی نرم
- در تولید پوششهای رسانایی شفاف از اکسید قلع ایندیوم (ITO)
- در الکترونیک
- در انواعی از لامپها
- در امالگامهای دندان
- یکی از جایگزینهای جیوه در باتریهای قلیایی
- در میلههای کنترل برای راکتورهای هستهای
اکسید قلع ایندیوم(ITO)
اکسید قلع ایندیم(ITO) یک ترکیب سه تایی از ایندیم، قلع و اکسیژن در نسبتهای مختلف است. بسته به محتوای اکسیژن، میتوان آن را به عنوان سرامیک یا آلیاژ توصیف کرد.
ITO یک رسانا است که معمولاً بهعنوان یک پوشش نازک استفاده میشود. در لایههای نازک شفاف و بیرنگ است، درحالی که به صورت جامد بسته به درجهٔ اکسیداسیون آن، معمولاً مایل به زرد تا خاکستری است.
حدود ۴۵٪ از کل ایندیم برای تولید ITO استفاده میشود و این در سلولهای خورشیدی و LCDها (نمایشگرهای کریستال مایع) کاربرد دارد. در هردو این وسایل از ITO برای ایجاد جریان الکتریکی روی دستگاه و عبور نور از آن استفاده میشود.
استفاده از ITO در موارد دیگر: پنلهای لمسی، نمایشگرهای الکتروکرومیک، الکترو لومینسانس، نمایشگرهای پلاسما، نمایشگرهای انتشار میدانی، پوششهای بازتابنده گرما، سنسورهای گاز، فتوولتائیک.
ایندیوم در پزشکی
افراد برای خستگی، پیری، تقویت سیستم ایمنی بدن و افزایش تولید هورمون از ایندیوم استفاده میکنند؛ اما هیچ مدرک علمی خوبی برای حمایت از این موارد وجود ندارد. استفاده از ایندیوم به صورت خوراکی نیز میتواند خطرناک باشد. ارائهدهندگان خدمات بهداشتی گاهی برای کمک به تشخیص انواع خاصی از سرطان، یک نسخه تأیید شده توسط FDA، به نام indium (In-111) pentetreotide به روش IV استفاده میکنند.
عوارض جانبی
ایندیوم اگر خوردهشود خطرناک است.
ایندیوم برای بسیاری از قسمتهای بدن سمی است.
هنگامی که یک محصول حاوی ایندیوم(In-111)پنتروتید توسط یک متخصص مراقبتهای بهداشتی بهصورت IV تجویز شود، به احتمال زیاد به این روش ایمن است.
هشدارها و احتیاطهای ویژه
در زمان بارداری و شیردهی مصرف ایندیم از طریق دهان یا به صورت IV خطرناک است. اثرات ایندیوم بر نوزاد متولد نشده یا شیرخوار ناشناخته است، اما سمی بودن آن محرز است.
بازیافت
از آنجا که ایندیوم بهطور گستردهای در محیط پخش نمیشود، تهدیدی برای حیات زمین و دریا نیست. اثرات زیستمحیطی این ماده بهطور کامل بررسی نشدهاست. البته بخش قابل توجهی از آن از بازیافت بدست میآید.
امروزه هر سال حدود ۴۸۰ تن ایندیوم از معدن به دست میآید و ۶۵۰ تن از طریق بازیافت به دست میآید. فناوری مورد استفاده در بازیافت ایندیوم بیشتر اختصاصی است.
ایندیوم بیشتر از بهبود یافتن اکسید قلع ایندیوم(ITO) مصرف شده از طریق مراحل زیر دست میآید:
- از نیتریک اسید استفاده میشود تا نیتریت ایندیوم به دست بیاید که با خنثی سازی همراه است که باعث تولید هیدروکسید ایندیوم میشود.
- اکسید ایندیوم از طریق تجزیه حرارتی تشکیل شده و در اسید سولفوریک حل میشود.
- ایندیوم فلزی را میتوان از محلول حاصل به صورت الکترولیتی تولید کرد.
ظرفیت پالایش برای بازیافت ITO مصرف شده، برای کاهش تقاضای اولیهٔ ایندیوم از سال ۱۹۹۶ بهطور قابل توجهی گسترش یافتهاست. برای اینکار ژاپن، چین، کرهجنوبی و بلژیک بیشترین ظرفیت را دارند.
از اضافات ITO در تولید LCD و سایر برنامهها استفاده میشود.
جستارهای وابسته
منابع
پیوند به بیرون
- https://www.rsc.org/periodic-table/element/49/indium
- https://www.lenntech.com/periodic/elements/in.htm
- https://www.rsc.org/periodic-table/video/49/Indium?videoid=4opHafNmgCw
- https://www.webmd.com/vitamins/ai/ingredientmono-1158/indium
- https://www.rsc.org/periodic-table/element/49/indium
| معنای ایندیم را در ویکیواژه، واژهنامهٔ آزاد، ببینید. |
| در ویکیانبار پروندههایی دربارهٔ ایندیم موجود است. |
This article uses material from the Wikipedia فارسی article ایندیم, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). محتوا تحت CC BY-SA 4.0 در دسترس است مگر خلافش ذکر شده باشد. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki فارسی (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.