氯
「氯」得尋 - 維基大典
君所欲求,蓋名曰"氯"者乎?此共筆臺已有之。 又羅得數條,悉列於下。
 氯者,化學元素也,符號為Cl,原子序十七,屬鹵素。色黃綠,敏於腐蝕,有毒。日本稱鹽素,蓋氯爲食鹽。 氯原子有七電子於外緣,按八隅體律,最外層電子之數不足八者,皆不固。故地球之上,氯原子難自安而易相合。以共價鍵合二為一,則成氯氣。合鈉而為氯化鈉(即俗謂食鹽),存於海水。溶於水,生鹽酸次氯酸也。……
氯者,化學元素也,符號為Cl,原子序十七,屬鹵素。色黃綠,敏於腐蝕,有毒。日本稱鹽素,蓋氯爲食鹽。 氯原子有七電子於外緣,按八隅體律,最外層電子之數不足八者,皆不固。故地球之上,氯原子難自安而易相合。以共價鍵合二為一,則成氯氣。合鈉而為氯化鈉(即俗謂食鹽),存於海水。溶於水,生鹽酸次氯酸也。…… 碳酰氯,亦稱光氣,式曰COCl2,有機化合物也。無色氣體,性活潑,其毒十倍於氯。公元一八一二年,英人約翰戴維初以氯氣共一氧化碳光照合而得之。用於造農藥、染料、塑料之類。一戰因毒氣死者十萬,光氣百之八十有五也。……
碳酰氯,亦稱光氣,式曰COCl2,有機化合物也。無色氣體,性活潑,其毒十倍於氯。公元一八一二年,英人約翰戴維初以氯氣共一氧化碳光照合而得之。用於造農藥、染料、塑料之類。一戰因毒氣死者十萬,光氣百之八十有五也。…… 二氯二乙硫醚者,式書C4H8Cl2S,含氯官品,強糜爛劑是也。味似芥末,故又名硫芥子氣。第一次世界大戰施於化學戰,受害者眾,傷亡者逾一百三十萬。 為糜爛性毒劑,具細胞毒性。萬國癌究機構列之以一類致癌物,為首察化學致變劑也。……
二氯二乙硫醚者,式書C4H8Cl2S,含氯官品,強糜爛劑是也。味似芥末,故又名硫芥子氣。第一次世界大戰施於化學戰,受害者眾,傷亡者逾一百三十萬。 為糜爛性毒劑,具細胞毒性。萬國癌究機構列之以一類致癌物,為首察化學致變劑也。…… 氯胺酮者,俗稱k粉。藥也,作麻醉,亦可濫用成毒品。色白,粉狀。私販者於中國可誅之。……
氯胺酮者,俗稱k粉。藥也,作麻醉,亦可濫用成毒品。色白,粉狀。私販者於中國可誅之。……- 鹵素,第七主族諸元素統稱也,皆非金屬。意曰「可成鹽素」,故一譯造鹽質。氟、氯、溴、碘、砹五者,俱屬之。常以化合態存於天地。 氟、氯皆為氣也。氟,色微黃,性甚烈,無可儲存,惟鎳鉻有茲護層,可貯氟也。氯,色黃綠,蝕性強,有毒,常化合鈉為食鹽,存於海中。 溴,色棕紅,液相,性亦烈,強於腐蝕。溶於水則成溴水,色橙紅。……
- 非金屬,顧名思義,不為金屬也。氫、硼、碳、氮、氧、氟、硅、磷、硫、氯、砷、硒、溴、碲、碘、砈、氦、氖、氬、氪、氙、氡廿二元素屬之。從氣者,為氣,從水者,為液,從石者,為固也。 亦作矽 亦作砹 元素週期表 譯名見異,臺譯在先,陸譯在後,香港兼從……
 金屬。出於鋯石,名實俱然。溯其字義,本波斯文金色之謂也。面有光澤,呈灰白,酷似於鉿,稍類於鈦。融鋯於物,俾能耐火、遮光、防鏽。化合者眾,無機者、有機金屬者皆有,諸如二氧化鋯、二氯二茂鋯等。同位素自然而成者有五,其三穩定。 《英文維基鋯一文簡介段》 元素週期表 譯名見異,臺譯在先,陸譯在後,香港兼從……
金屬。出於鋯石,名實俱然。溯其字義,本波斯文金色之謂也。面有光澤,呈灰白,酷似於鉿,稍類於鈦。融鋯於物,俾能耐火、遮光、防鏽。化合者眾,無機者、有機金屬者皆有,諸如二氧化鋯、二氯二茂鋯等。同位素自然而成者有五,其三穩定。 《英文維基鋯一文簡介段》 元素週期表 譯名見異,臺譯在先,陸譯在後,香港兼從…… 銫者,化學元素也,符號為Cs,原子序五十五,屬鹼金屬、第六週期。性輕軟,色銀白,遇氧而火,性似鈉、鉀。熔點甚低,僅攝氏二十八度。自然之中,不以獨存,必以化合,併氯而為氯化銫,存於大海。又性烈,亟合於水,霹靂而生氫氣、氫氧化銫,故貯於煤油。夫氫氧化銫者,當世最強鹼也。 一八六一年,德意志化學家本生及基爾霍夫以焰色試驗辨銫,始得之。……
銫者,化學元素也,符號為Cs,原子序五十五,屬鹼金屬、第六週期。性輕軟,色銀白,遇氧而火,性似鈉、鉀。熔點甚低,僅攝氏二十八度。自然之中,不以獨存,必以化合,併氯而為氯化銫,存於大海。又性烈,亟合於水,霹靂而生氫氣、氫氧化銫,故貯於煤油。夫氫氧化銫者,當世最強鹼也。 一八六一年,德意志化學家本生及基爾霍夫以焰色試驗辨銫,始得之。……- 鹵代烷者,鹵素代烷烴之氫之所成。鹵素,可為氟、氯、溴、碘之一。屬官品。 鹵代烷一文似未成。宜善之。……
 百餘元素中,常溫液態者僅二,其一為溴,另一為汞。 同位素者四十五,自溴六七至溴九七。性穩者有二,曰溴七九,曰溴八一。以溴七九為盛。 欲得之,須以氯通過含溴之鹵水。 實驗室中小量得之,則用溴化鈉並濃硫酸可得。 NaBr (s) + H2SO4 (aq) → HBr (aq) + NaHSO4 (aq)……
百餘元素中,常溫液態者僅二,其一為溴,另一為汞。 同位素者四十五,自溴六七至溴九七。性穩者有二,曰溴七九,曰溴八一。以溴七九為盛。 欲得之,須以氯通過含溴之鹵水。 實驗室中小量得之,則用溴化鈉並濃硫酸可得。 NaBr (s) + H2SO4 (aq) → HBr (aq) + NaHSO4 (aq)…… 中華產銻,甲於世,以湖南錫礦山為最。取銻之法,置輝銻礦於火,以碳焙燒一也,以鐵焙燒二也。 世多產銻,多並鉛、錫而為鉛銻板,用諸鉛酸電池。融銻於鉛、錫,以成合金,亦可進焊料、子彈、軸承之功。又,氯、溴阻燃劑,雜混銻化合物,以增其效。近世亦有用銻於微電子業者。 《英文維基》銻一文簡介段 元素週期表 譯名見異,臺譯在先,陸譯在後,香港兼從……
中華產銻,甲於世,以湖南錫礦山為最。取銻之法,置輝銻礦於火,以碳焙燒一也,以鐵焙燒二也。 世多產銻,多並鉛、錫而為鉛銻板,用諸鉛酸電池。融銻於鉛、錫,以成合金,亦可進焊料、子彈、軸承之功。又,氯、溴阻燃劑,雜混銻化合物,以增其效。近世亦有用銻於微電子業者。 《英文維基》銻一文簡介段 元素週期表 譯名見異,臺譯在先,陸譯在後,香港兼從…… 金屬。質輕且軟,新剖時銀而白,遇氧漸啞,性躁烈,遇水即沸,故貯於煤油,弗自存於世,以化合態存於坤輿,故古人未有得鈉者,今科學家以電解氯化鈉乃得之。併氯得食鹽,存於大海,兼併氫、氧,得氫氧化鈉,併氫、碳酸,得小蘇打。鈉鹽者,人所必須也。 一八零七年,英國人戴維電解熔融之氫氧化鈉,始得之並名之。……
金屬。質輕且軟,新剖時銀而白,遇氧漸啞,性躁烈,遇水即沸,故貯於煤油,弗自存於世,以化合態存於坤輿,故古人未有得鈉者,今科學家以電解氯化鈉乃得之。併氯得食鹽,存於大海,兼併氫、氧,得氫氧化鈉,併氫、碳酸,得小蘇打。鈉鹽者,人所必須也。 一八零七年,英國人戴維電解熔融之氫氧化鈉,始得之並名之。…… 而鈰之提取,易於他物。以獨其氧化態正四亦穩故,亦易辨諸鑭系元素。鑭系之中,以其最豐,其次為釹、鑭、鐠。地殼諸元素,位次第二十六,百萬而六十有六,半於氯而五於鉛。 鑭系元素,其惟先得。一八零三年,瑞典化學家白則里(Jöns Jakob Berzelius)、希辛格(Wilhelm……
而鈰之提取,易於他物。以獨其氧化態正四亦穩故,亦易辨諸鑭系元素。鑭系之中,以其最豐,其次為釹、鑭、鐠。地殼諸元素,位次第二十六,百萬而六十有六,半於氯而五於鉛。 鑭系元素,其惟先得。一八零三年,瑞典化學家白則里(Jöns Jakob Berzelius)、希辛格(Wilhelm……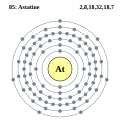 其性未知者多矣,常以推斷。以其屬鹵素,所在低於碘故,算其色澤為黑,熔點高於碘,或可作半導體。其負離子,相似於碘。惟在水中,可成正離子,類於金屬,有異鹵素中輕於其者(即氟、氯、溴、碘)。 一九四零年,加州大學柏克萊分校學者戴爾科森、羅斯麥肯齊、埃米利奧塞格雷三人,始合成之。嗣後,天然同位素相繼而得,凡四種,較諸人工合成者……
其性未知者多矣,常以推斷。以其屬鹵素,所在低於碘故,算其色澤為黑,熔點高於碘,或可作半導體。其負離子,相似於碘。惟在水中,可成正離子,類於金屬,有異鹵素中輕於其者(即氟、氯、溴、碘)。 一九四零年,加州大學柏克萊分校學者戴爾科森、羅斯麥肯齊、埃米利奧塞格雷三人,始合成之。嗣後,天然同位素相繼而得,凡四種,較諸人工合成者…… 主文:離子鍵 若並金屬、非金屬,金屬去電子而非金屬得之,兩者並合,此謂離子鍵。 金屬去電子而得正離子、非金屬得之而成負離子,正負相吸,則成。觀氯、鈉者,並之,則氯從鈉得一電子,最外達八而趨安(此謂八隅體),得氯離子、鈉離子,兩者正負相吸而並。離子鍵可延,無分子之構。 主文:共價鍵……
主文:離子鍵 若並金屬、非金屬,金屬去電子而非金屬得之,兩者並合,此謂離子鍵。 金屬去電子而得正離子、非金屬得之而成負離子,正負相吸,則成。觀氯、鈉者,並之,則氯從鈉得一電子,最外達八而趨安(此謂八隅體),得氯離子、鈉離子,兩者正負相吸而並。離子鍵可延,無分子之構。 主文:共價鍵…… 食鹽者(化學式:NaCl、化學之名:氯化鈉),離子化合物也,又曰鹽。并鈉、氯而成。無色晶體,鹹也。生之所繫,味之所依也。 凡鹽產最不一:海、池、井、土、岩、砂石,略分六種,而東夷樹葉、西戎光明不與焉。赤縣之內,海鹵居十之八,而其二為井、池、土堿。或假人力,或由天造。總之,一經舟車窮窘,則造物應付出焉。……
食鹽者(化學式:NaCl、化學之名:氯化鈉),離子化合物也,又曰鹽。并鈉、氯而成。無色晶體,鹹也。生之所繫,味之所依也。 凡鹽產最不一:海、池、井、土、岩、砂石,略分六種,而東夷樹葉、西戎光明不與焉。赤縣之內,海鹵居十之八,而其二為井、池、土堿。或假人力,或由天造。總之,一經舟車窮窘,則造物應付出焉。…… 鹽者,一譯鹺,離子化合物也,并金屬離子、非金屬離子而生,或并酸鹼得之。盈於山海,甚常見之。 夫世者,以食鹽為盛。食鹽者,氯化鈉也,并鈉、氯而成。作調味之用。產於海者,謂之海鹽;產於土者,謂之礦鹽。 色甚多,或透明如食鹽,或帶金屬光澤如黃鐵礦,各鹽之色盡列如下: 色黃者,如鉻酸鈉也 色橙者,如重鉻酸鉀也……
鹽者,一譯鹺,離子化合物也,并金屬離子、非金屬離子而生,或并酸鹼得之。盈於山海,甚常見之。 夫世者,以食鹽為盛。食鹽者,氯化鈉也,并鈉、氯而成。作調味之用。產於海者,謂之海鹽;產於土者,謂之礦鹽。 色甚多,或透明如食鹽,或帶金屬光澤如黃鐵礦,各鹽之色盡列如下: 色黃者,如鉻酸鈉也 色橙者,如重鉻酸鉀也……- 氯化氫,式HCl,無色液體也。極易溶於水,水溶液為鹽酸,性烈,為強酸。其共價鍵極性甚強,於氫,部分正電荷也;氯者,部分負電荷也。 甲、並氯氣與氫氣得之,此乃直接之法也。 乙、並氯化物與酸,得氫氯酸。如下所示: 氯化鈉+硝酸→硝酸鈉+鹽酸 顧翼東 化學詞典 :第九百二十二頁; 上海辭書出版社; ISBN……
 惰氣之類。主族諸類,如碳氧鈉鈣者,皆從此律。簡而言之,凡塵中原子之外殼有電子八,則性安不易也。若不達八,則共之、去之、取之而達八也。氯者,缺一得八,鈉者,去一得八,氯取電子而鈉去之,各八而安,得鹽也。 夫每層可納之電子有限(式乃:層級平方之兩倍),故首層電子數之極為二,次層為八,再次層十八,如此類推。……
惰氣之類。主族諸類,如碳氧鈉鈣者,皆從此律。簡而言之,凡塵中原子之外殼有電子八,則性安不易也。若不達八,則共之、去之、取之而達八也。氯者,缺一得八,鈉者,去一得八,氯取電子而鈉去之,各八而安,得鹽也。 夫每層可納之電子有限(式乃:層級平方之兩倍),故首層電子數之極為二,次層為八,再次層十八,如此類推。…… 分型也。是毒有薄膜正鏈單股核糖核酸,染之可獲二〇一九冠狀病毒病。其滅也,加以紫外線,於五十六攝氏度之高溫二刻;乙醚、醫用乙醇、含氯消毒劑、過氧乙酸、氯仿諸脂溶劑者亦可,然氯己定弗能。 初,中華人民共和國國家衛生健康委員法定其疫為乙類傳染病,以甲類治之。壬寅腊月十七,列乙類傳染病。中華民國衛生福利部定……
分型也。是毒有薄膜正鏈單股核糖核酸,染之可獲二〇一九冠狀病毒病。其滅也,加以紫外線,於五十六攝氏度之高溫二刻;乙醚、醫用乙醇、含氯消毒劑、過氧乙酸、氯仿諸脂溶劑者亦可,然氯己定弗能。 初,中華人民共和國國家衛生健康委員法定其疫為乙類傳染病,以甲類治之。壬寅腊月十七,列乙類傳染病。中華民國衛生福利部定……















