ซัลเฟอร์ไดออกไซด์
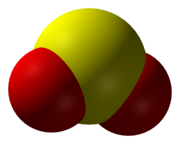
ซัลเฟอร์ไดออกไซด์ (สูตรทางเคมี SO2) เป็นออกไซด์ชนิดหนึ่งของกำมะถัน
 | |
 | |
 | |
| ชื่อ | |
|---|---|
| IUPAC name Sulfur dioxide | |
| ชื่ออื่น Sulfurous anhydride Sulfur(IV) oxide | |
| เลขทะเบียน | |
3D model (JSmol) | |
Beilstein Reference | 3535237 |
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ECHA InfoCard | 100.028.359 |
| EC Number |
|
| เลขอี | E220 (preservatives) |
Gmelin Reference | 1443 |
| KEGG | |
| MeSH | Sulfur+dioxide |
ผับเคม CID | |
| RTECS number |
|
| UNII | |
| UN number | 1079, 2037 |
CompTox Dashboard (EPA) | |
InChI
| |
SMILES
| |
| คุณสมบัติ | |
| SO 2 | |
| มวลโมเลกุล | 64.066 g mol−1 |
| ลักษณะทางกายภาพ | แก๊สไม่มีสีและฉุน |
| กลิ่น | Pungent; similar to a just-struck match |
| ความหนาแน่น | 2.6288 kg m−3[ต้องการอ้างอิง] |
| จุดหลอมเหลว | −72 องศาเซลเซียส; −98 องศาฟาเรนไฮต์; 201 เคลวิน |
| จุดเดือด | −10 องศาเซลเซียส (14 องศาฟาเรนไฮต์; 263 เคลวิน) |
| 94 g/L forms sulfurous acid | |
| ความดันไอ | 230 kPa at 10 °C; 330 kPa at 20 °C; 462 kPa at 30 °C; 630 kPa at 40 °C |
| pKa | ~1.81 |
| Basicity (pKb) | ~12.19 |
Magnetic susceptibility (χ) | −18.2·10−6 cm3/mol |
| ความหนืด | 12.82 μPa·s |
| โครงสร้าง | |
กลุ่มจุด | C2v |
Coordination geometry | Digonal |
รูปร่างโมเลกุล | Dihedral |
Dipole moment | 1.62 D |
| อุณหเคมี | |
Std molar entropy (S⦵298) | 248.223 J K−1 mol−1 |
Std enthalpy of formation (ΔfH⦵298) | −296.81 kJ mol−1 |
| ความอันตราย | |
| GHS labelling: | |
Pictograms |   |
Signal word | อันตราย |
Hazard statements | H314, H331 |
| NFPA 704 (fire diamond) | |
| ปริมาณหรือความเข้มข้น (LD, LC): | |
LC50 (median concentration) | 3000 ppm (mouse, 30 min) 2520 ppm (rat, 1 hr) |
LCLo (lowest published) | 993 ppm (rat, 20 min) 611 ppm (rat, 5 hr) 764 ppm (mouse, 20 min) 1000 ppm (human, 10 min) 3000 ppm (human, 5 min) |
| NIOSH (US health exposure limits): | |
PEL (Permissible) | TWA 5 ppm (13 mg/m3) |
REL (Recommended) | TWA 2 ppm (5 mg/m3) ST 5 ppm (13 mg/m3) |
IDLH (Immediate danger) | 100 ppm |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
| ซัลเฟอร์มอนอกไซด์ ซัลเฟอร์ไตรออกไซด์ ไดซัลเฟอร์มอนอกไซด์ | |
สารประกอบที่เกี่ยวข้อง | โอโซน ซีลีเนียมไดออกไซด์ Sulfurous acid เทลลูเรียมไดออกไซด์ |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa | |
สมบัติทางเคมี
2SO2+O2→2SO3 ซึ่งก๊าซซัลเฟอร์ไตรออกไซด์นี้สามารถละลายน้ำเกิดเป็นสารละลายกรดซัลฟิวริก
- เป็นแอซิดิกออกไซด์ (ออกไซด์ของธาตุที่ทำปฏิกิริยากับน้ำได้สารละลายกรด) เมื่อทำปฏิกิริยากับน้ำได้กรดซัลฟิวรัส
อ้างอิง
This article uses material from the Wikipedia ไทย article ซัลเฟอร์ไดออกไซด์, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). เนื้อหาอนุญาตให้เผยแพร่ภายใต้ CC BY-SA 4.0 เว้นแต่ระบุไว้เป็นอื่น Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki ไทย (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.
