Fluoor
Soekresultate vir
Daar is reeds 'n bladsy genaamd "Fluoor" op die wiki
 Fluoor (Latyn: Fluere, wat om te vloei beteken), is 'n chemiese element in die periodieke tabel met die simbool F en atoomgetal van 9. Dit is 'n giftige...
Fluoor (Latyn: Fluere, wat om te vloei beteken), is 'n chemiese element in die periodieke tabel met die simbool F en atoomgetal van 9. Dit is 'n giftige... Fluoor-19 (chemiese notasie: 199F) is 'n stabiele isotoop van die element fluoor. Dit is die enigste stabiele isotoop. 199F is saam met 11H een van die...
Fluoor-19 (chemiese notasie: 199F) is 'n stabiele isotoop van die element fluoor. Dit is die enigste stabiele isotoop. 199F is saam met 11H een van die...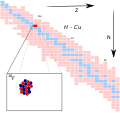 Fluoor-18 (chemiese notasie: 188F) is 'n sintetiese radioaktiewe isotoop van fluoor. Die isotoop het 'n halfleeftyd of 109 minute en sy verval stel 'n...
Fluoor-18 (chemiese notasie: 188F) is 'n sintetiese radioaktiewe isotoop van fluoor. Die isotoop het 'n halfleeftyd of 109 minute en sy verval stel 'n... Henri Moissan (afdeling Bereiding van elementêre fluoor)apteker wat die Nobelprys vir Chemie in 1906 verower het vir sy werk om fluoor van die verbindings daarvan te isoleer. Hy was die ontdekker van kalsiumkarbied...
Henri Moissan (afdeling Bereiding van elementêre fluoor)apteker wat die Nobelprys vir Chemie in 1906 verower het vir sy werk om fluoor van die verbindings daarvan te isoleer. Hy was die ontdekker van kalsiumkarbied...- kolom van die periodieke tabel voorkom. Hierdie groep omvat die elemente fluoor (F), chloor (Cl), broom (Br), jodium (I) en die minder bekende en radioaktiewe...
- aangedui); die meeste is gasse (waterstof, helium, stikstof, suurstof, fluoor, neon, chloor, argon, kripton, xenon en radon); een is ’n vloeistof (broom)...
- hierdie skaal word daar aan die mees elektronegatiewe chemiese element (Fluoor) 'n elektronegatiwiteit van 3.98 toegeken; die element met die laagste elektronegatiwiteit...
 Kalsiumfluoried (afdeling Fluoor-KMR)Kalsiumfluoried is 'n chemiese verbinding van kalsium en fluoor met 'n formule CaF2. Dit kom in die natuur as die mineraal fluoriet voor. Suiwer kalsiumfluoried...
Kalsiumfluoried (afdeling Fluoor-KMR)Kalsiumfluoried is 'n chemiese verbinding van kalsium en fluoor met 'n formule CaF2. Dit kom in die natuur as die mineraal fluoriet voor. Suiwer kalsiumfluoried...- 'n Fluoried is 'n chemiese verbinding wat die element fluoor is sy oksidasietoestand -1 bevat. Dit is essensieel alle fluoorverbindings omdat hierdie element...
- internasionale simbool vir frekwensie. F, is in die SI stelsel die internasionale simbool vir krag (vanuit het Engelse: Force). F, 'n chemiese element: Fluoor....
- elektronegatiwiteit in die diagonale rigting van tallium (links onder) na fluoor (regs bo) sterk toe. In die hoek regs bo is die elemente nie-metale, in...
- hulle kan met metale soos natrium as oksidant optree en met niemetale soos fluoor as reduksiemiddel. Hulle is vastestowwe en hul struktuur bestaan uit kovalente...
- voor as diatomiese molekules, soos waterstof H2, stikstof N2, suurstof O2, fluoor F2 en chloor Cl2, wat almal gasse is by kamertemperatuur. Broom Br2 is 'n...
- terbiumatoom in sy grondtoestand [Xe]6s25d24f8 is. Gewoonlik vorm Ln-metale met fluoor driewaardige fluoriede LnF3 omdat hulle die s- d-elektrone verloor maar...
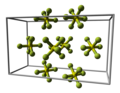 Swaelheksafluoried (kategorie Verbindings van fluoor)Swaelheksafluoried is 'n verbinding van swael in sy hoogste +6 oksidasietoestand en fluoor met die formule SF6 Dit is 'n opmerkelik inerte kleurlose en reuklose gas...
Swaelheksafluoried (kategorie Verbindings van fluoor)Swaelheksafluoried is 'n verbinding van swael in sy hoogste +6 oksidasietoestand en fluoor met die formule SF6 Dit is 'n opmerkelik inerte kleurlose en reuklose gas... 'n blok bly tot ongeveer 400 C onaangetas. Die metaal reageer ook met fluoor of chloor bo 100 C, maar dit reageer nie met sure of met koningswater nie...
'n blok bly tot ongeveer 400 C onaangetas. Die metaal reageer ook met fluoor of chloor bo 100 C, maar dit reageer nie met sure of met koningswater nie... Broompentafluoried (kategorie Fluoor)chemiese verbinding met formule BrF5 van broom in sy oksidasietoestand +5 met fluoor. Die stof is 'n baie sterk oksidator en word as fluorineringsagens gebruik...
Broompentafluoried (kategorie Fluoor)chemiese verbinding met formule BrF5 van broom in sy oksidasietoestand +5 met fluoor. Die stof is 'n baie sterk oksidator en word as fluorineringsagens gebruik... elektronegatiewe atoom en 'n Waterstof atoom wat aan Stikstof, Suurstof of Fluoor verbind is. Hierdie soort verbinding behels altyd 'n waterstofatoom en die...
elektronegatiewe atoom en 'n Waterstof atoom wat aan Stikstof, Suurstof of Fluoor verbind is. Hierdie soort verbinding behels altyd 'n waterstofatoom en die...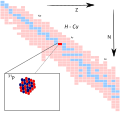 protone word gewoonlik ontkoppel, maar die koppeling met protone of met fluoor-19 kan ook bestudeer word. Hebreeuse Universiteit van Jerusalem Hierdie...
protone word gewoonlik ontkoppel, maar die koppeling met protone of met fluoor-19 kan ook bestudeer word. Hebreeuse Universiteit van Jerusalem Hierdie... is vir alle praktiese doeleindes inert maar daar is al verbindings met fluoor bekend. Kripton vorm ook klatrate met water wanneer atome daarvan in die...
is vir alle praktiese doeleindes inert maar daar is al verbindings met fluoor bekend. Kripton vorm ook klatrate met water wanneer atome daarvan in die...
- simbool F en atoomgetal 9. Fluoor is 'n giftige bleek geelgroen, univalente halogeengas. Sien Wikipedia vir meer inligting oor fluoor. Periodieke tabel










