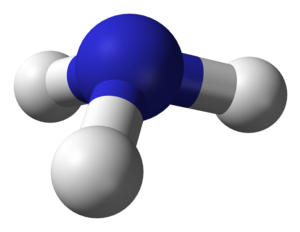
Amonyak, formülü NH3 olan; azot atomu ve hidrojen atomundan oluşan renksiz, keskin ve rahatsız edici kokulu bir bileşiktir.
OH- iyonu içermediği hâlde suda zayıf baz özelliği gösterir. Bir amonyak molekülü, bir azot ve üç hidrojen atomundan oluşur. Oda sıcaklığında gaz hâlde bulunan bileşiğin ticari formu sulu çözeltiyi içermektedir.
 | |
 | |
 | |
| Adlandırmalar | |
|---|---|
Azan | |
Diğer adlar Hidrojen nitrür Nitro-Sil | |
| Tanımlayıcılar | |
3D model (JSmol) | |
| 3DMet | |
| 3587154 | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.028.760 |
| EC Numarası |
|
| 79 | |
| KEGG | |
PubChem CID | |
| RTECS numarası |
|
| UN numarası | 1005 |
CompTox Bilgi Panosu (EPA) | |
| |
| |
| Özellikler | |
| Molekül formülü | NH3 |
| Molekül kütlesi | 17.031 g/mol |
| Görünüm | Renksiz gaz |
| Koku | Güçlü acı koku |
| Yoğunluk | 0.86 kg/m³ (kaynama noktasında 1.013 bar) 0.769 kg/m³ (Standart koşullarda) |
| Erime noktası | −77.73 °C (−107.91 °F; 195.42 K) |
| Kaynama noktası | −33.34 °C (−28.01 °F; 239.81 K) |
| Çözünürlük (su içinde) | 47% kütle/kütle (0 °C) 31% kütle/kütle (25 °C) 18% kütle/kütle (50 °C) |
| Çözünürlük | Kloroform, eter, etanol ve metanolde çözünür. |
| Buhar basıncı | 8573 h Pa |
| Asitlik (pKa) | 32.5 (−33 °C), 10.5 (DMSO) |
| Baziklik (pKb) | 4.75 |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |    |
| R-ibareleri | R10, R23, R34, R50 |
| NFPA 704 (yangın karosu) | |
| Parlama noktası | Yanıcı gaz |
Kendiliğinden tutuşma sıcaklığı | 651 °C (1,204 °F; 924 K) |
| Patlama sınırları | 15–28% |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz) | 0.015 mL/kg (insan, oral) |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | 50 ppm (25 ppm ACGIH- TLV; 35 ppm STEL) |
| AB sınıflandırması | Şablon:Hazchem T Şablon:Hazchem C Şablon:Hazchem N |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
| Bilgi kutusu kaynakları | |
Amonyak, kovalent bağlı bir bileşiktir. Molekülleri polar olduğundan su içinde yüksek oranda çözünür. Amonyak molekülleri kendi aralarında olduğu gibi su molekülleri ile de zayıf hidrojen bağı oluşturur ve suda çözünür.
İsmin kökeni Eski Mısır'a dayanır. Amon tapınağını ısıtmada kullanılan deve tezeklerinden çıkan gazlardan, tapınağın duvarlarında, tavanında sofra tuzu gibi beyaz kristaller hâlindeki amonyum klorür yani nişadır birikmiştir. Buna da o dönemde "Amon'un Tuzu" denilmiştir.
Amonyak, gübre, ilaç, boya, parfüm gibi maddelerin sentezlenmesinde ilk aşamada kullanılmaktadır. Amonyak canlılar için zehirli bir maddedir, kullanılırken dikkat edilmesi gerekir. Piyasada amonyak adı altında satılan maddeler amonyağın sulu çözeltisi olan amonyum hidroksittir.
Temizlik malzemelerinde, patlayıcı ve gübre yapımında, kimya sanayiinde, nitrik asidin, boyaların, parfümlerin, plastiklerin ve ürenin üretiminde ve endüstriyel soğutma sistemlerinde kullanılır.
This article uses material from the Wikipedia Türkçe article Amonyak, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Aksi belirtilmedikçe içeriğin kullanımı CC BY-SA 4.0 lisansı kapsamında uygundur. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Türkçe (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.