ការបង្កឡើងរបស់ កោសិកាដើម Pluripotent
Induced pluripotent stem cells (iPS cell/iPSC) ឬកោសិកាដើម pluripotent ណែនាំហ្សែនជាក់លាក់ចំនួនបួនដែលបណ្តាលឱ្យមាន pluripotency ចូលទៅក្នុងកោសិកា somatic ដូចជាកោសិកាស្បែកមនុស្សពេញវ័យ ដោយគ្មាន pluripotency ។ បន្ទាប់មកដោយការទាញយកប្រូតេអ៊ីន dedifferentiation-inducing ដែលផលិតពីកោសិកាចូលទៅក្នុងហ្សែនចំនួនបួន។ ដែលបណ្តាលឱ្យ dedifferentiation ត្រូវបានបញ្ចេញ ឬណែនាំ ហើយចាក់បញ្ចូលពួកវាទៅក្នុងកោសិកា somatic កោសិកាដើមដែលមាន pluripotency ដូចជាកោសិកាដើមអំប្រ៊ីយ៉ុងអាចបង្កើតបាន។ ទាំងនេះត្រូវបានគេហៅថាដើម pluripotent ដែលជម្រុញ។ ពួកវាត្រូវបានគេហៅថាកោសិកាដើម pluripotent ឬកោសិកាដើម pluripotent ។
ក្នុងឆ្នាំ 2006 ក្រុមរបស់សាស្រ្តាចារ្យ Shinya Yamanaka នៅសាកលវិទ្យាល័យ Kyoto ក្នុងប្រទេសជប៉ុនបានទទួលជោគជ័យក្នុងការបង្កើតកោសិកាដើមដែលមានភាពសម្បូរបែបដូចជាកោសិកាដើមអំប្រ៊ីយ៉ុង ដោយបញ្ចូលហ្សែនជាច្រើនចូលទៅក្នុង កោសិកា ស្បែកកណ្ដុរ។ នៅឆ្នាំបន្ទាប់ ក្នុងឆ្នាំ 2007 ក្រុមរបស់សាស្រ្តាចារ្យ Yamanaka បានទទួលជោគជ័យក្នុងការបង្កើតកោសិកាដើម pluripotent ដោយបញ្ចូលហ្សែនទៅក្នុងកោសិកាស្បែកមនុស្សពេញវ័យ។ ក្នុងការទទួលស្គាល់ការរួមចំណែករបស់គាត់ក្នុងការរកឃើញ និងបង្ហាញថាកោសិកាចាស់ទុំ និងខុសគ្នាអាចត្រូវបានបែងចែកទៅជាកោសិកាដែលមិនទាន់ពេញវ័យ និងត្រូវបានអភិវឌ្ឍទៅជាជាលិកាទាំងអស់ម្តងទៀត សាស្ត្រាចារ្យ Shinya Yamanaka រួមជាមួយសាស្រ្តាចារ្យ John Gurden បានទទួលរង្វាន់ ណូបែលផ្នែកសរីរវិទ្យា ឬវេជ្ជសាស្ត្រឆ្នាំ 2012។ បានជ្រើសរើស។
គំនិតនៃ versatility
ក្នុងអំឡុងពេលនៃការអភិវឌ្ឍន៍ធម្មតា កោសិកាផ្លាស់ប្តូរបន្តិចម្តងៗពីស្ថានភាពដែលមិនខុសគ្នាដំបូង ដើម្បីក្លាយជាឯកទេសក្នុងមុខងារ។ កោសិកានៅក្នុងស៊ុតបង្កកំណើតគឺ totipotent ដែលមានន័យថាពួកគេអាចបង្កើតជាលិកាគ្រប់ប្រភេទ រួមទាំងរចនាសម្ព័ន្ធដែលមិនមែនជាអំប្រ៊ីយ៉ុងដូចជាសុក។ នៅពេលដែលដំណាក់កាលនៃការអភិវឌ្ឍន៍រីកចម្រើន ហើយ blastocyst ក្លាយជា blastocyst វាអាចបែងចែកទៅជាកោសិកាខាងក្នុង និងកោសិកាខាងក្រៅ។ នៅពេលនេះ កោសិកាខាងក្នុងមាន pluripotent ហើយអាចវិវត្តទៅជាកោសិកា somatic embryonic និងកោសិកាដំណុះគ្រប់ប្រភេទ។
អត្ថប្រយោជន៍នៃកោសិកាដើម pluripotent ជំរុញ
កោសិកាដើមអំប្រ៊ីយ៉ុងដែលស្រង់ចេញពីម៉ាសកោសិកាខាងក្នុងនៃ blastocyst មានច្រើន ហើយអាចបែងចែកទៅជាកោសិកា endoderm, mesoderm និង ectoderm ។ វាត្រូវបានគេដឹងថាកោសិកាដើមអំប្រ៊ីយ៉ុងរបស់មនុស្សអាចត្រូវបានគេប្រើប្រាស់ដើម្បីព្យាបាលជំងឺ ដូចជាជំងឺផាកឃីនសុ ន របួសឆ្អឹងខ្នង និង ជំងឺទឹកនោមផ្អែម ។ ទោះជាយ៉ាងណាក៏ដោយ កោសិកាដើមអំប្រ៊ីយ៉ុងមានដែនកំណត់ដូចជាបញ្ហាសីលធម៌នៃការបំផ្លាញអំប្រ៊ីយ៉ុង និងលទ្ធភាពនៃ ការបដិសេធ នៅពេលប្តូរចូលទៅក្នុងខ្លួនរបស់អ្នកជំងឺ។ ទោះជាយ៉ាងណាក៏ដោយ កោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិត មានសារៈសំខាន់យ៉ាងខ្លាំង ដែលពួកគេបានដោះស្រាយបញ្ហាសីលធម៌នៃការស្រាវជ្រាវកោសិកាដើមអំប្រ៊ីយ៉ុងដែលមានស្រាប់ ដែលក្នុងនោះកោសិកាដើមអាចទទួលបានដោយការបំផ្លាញអំប្រ៊ីយ៉ុងដែលកំពុងលូតលាស់នៅក្នុងស៊ុតបង្កកំណើតប៉ុណ្ណោះ។ លើសពីនេះទៀត ដោយសារកោសិការាងកាយរបស់អ្នកជំងឺត្រូវបានបំប្លែងទៅជាកោសិកាដើម វាមិនមានបញ្ហាជាមួយនឹងការបដិសេធនៃប្រព័ន្ធភាពស៊ាំនោះទេ។
វិធីសាស្រ្តនៃការបង្កើតកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញ
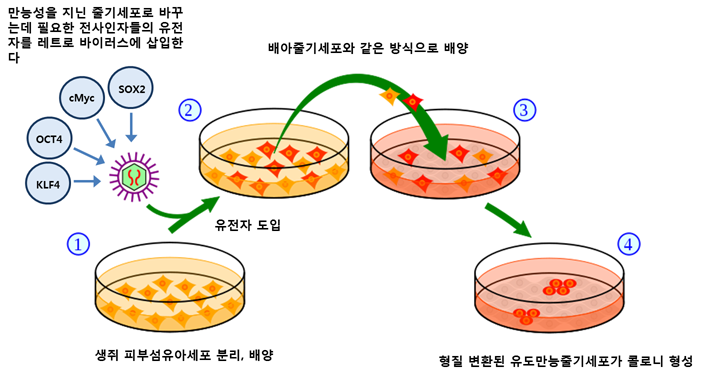
ទីមួយសាស្រ្តាចារ្យ Yamanaka ផ្អែកលើការពិតដែលថា pluripotency ត្រូវបានជំរុញនៅក្នុង កោសិកា នៅពេលដែល ការផ្ទេរនុយក្លេអ៊ែរ កោសិកា somatic ត្រូវបានអនុវត្តនៅលើ oocytes ឬនៅពេលដែលកោសិកា somatic និងកោសិកាដើមអំប្រ៊ីយ៉ុងត្រូវបានបញ្ចូលគ្នា ហ្សែនដែលដើរតួយ៉ាងសំខាន់ក្នុងការរក្សា pluripotency នៅក្នុងកោសិកាដើមអំប្រ៊ីយ៉ុងត្រូវបានកំណត់អត្តសញ្ញាណ។ ពួកគេបានសន្មត់ថាវានឹងដើរតួនាទីយ៉ាងសំខាន់ក្នុងការជំរុញឱ្យមាន pluripotency នៅក្នុងកោសិកា somatic ។ ហើយក្នុងចំណោមហ្សែនផ្សេងៗដែលដើរតួនាទីយ៉ាងសំខាន់ក្នុងការរក្សាបាននូវសារធាតុ pluripotency នៅក្នុងកោសិកាដើមអំប្រ៊ីយ៉ុង មាន 24 ហ្សែន (Ecat1, Dpp5 (Esg1), Fbx015, Nanog, ERas, Dnmt3l, Ecat8, Gdf3, Sox15, Dppa4, Dppa, Fl72, Oct4, Sox2, Rex1, Utf1, Tcl1, Dppa3, Klf4, b-cat, cMyc, Stat3, Grb2) ត្រូវបានជ្រើសរើសជាបេក្ខភាពដែលគិតថានឹងជំរុញឱ្យមានពហុភាពនៅក្នុងកោសិកា somatic ។
មុនពេលណែនាំហ្សែន 24 ជាមួយនឹងមេរោគ retrovirus ហ្សែន neomycin/lacZ ត្រូវបានបញ្ចូលដោយ ការផ្សំឡើងវិញដូចគ្នា នៅជាប់នឹង អ្នកផ្សព្វផ្សាយ Fbx15 នៅក្នុង fibroblasts ស្បែកកណ្តុរ។ Fbx15 គឺជាភ្នាក់ងារផ្សព្វផ្សាយដែលត្រូវបានធ្វើឱ្យសកម្មនៅក្នុងកោសិកាដើម pluripotent ហើយហ្សែនដែលបង្ហាញពីហ្សែន neomycin/lacZ មានភាពធន់នឹង G418 (អង់ទីប៊ីយ៉ូទិក aminoglycoside ដែលបង្ហាញជាតិពុល cytotoxicity ខ្លាំងដោយការរារាំងការសំយោគប្រូតេអ៊ីន) បន្ទាប់មក ហ្សែនទាំង 24 ត្រូវបាន បំប្លែង ទៅជា fibroblasts ស្បែកកណ្ដុរ ដោយប្រើមេរោគ retrovirus ។ កោសិកាទាំងនេះត្រូវបានដាំដុះនៅលើកោសិកាចំណី STO ដែលមានប្រហែល 0.3 mg/ml នៃ G418 ។ ក្នុងចំណោមកោសិកាដែលហ្សែនត្រូវបានគេណែនាំ កោសិកាមួយចំនួនក្លាយជាកោសិកាដើមដែលមានសារធាតុ pluripotent ដែលជំរុញឱ្យមាន ហើយអាណានិគមត្រូវបានបង្កើតឡើង។
ដើម្បីស្វែងយល់ពីកត្តាសំខាន់ៗដែលជំរុញឱ្យមាន pluripotency នៅក្នុងកោសិកា somatic ក្នុងចំណោមហ្សែនទាំង 24 ហ្សែនត្រូវបានជំរុញនៅក្នុង fibroblasts ស្បែកកណ្តុរដោយការលុបហ្សែនមួយក្នុងចំណោមហ្សែនទាំង 24 ។ តាមរយៈដំណើរការនៃការវាស់ស្ទង់ការផ្លាស់ប្តូរកម្រិតនៃការបង្កើតអាណានិគមជាកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញដោយការបាត់បង់ហ្សែនមួយក្នុងចំនោម 24 ហ្សែន ប្រតិចារិកចំនួន 4 គ្រប់គ្រាន់ដើម្បីបំប្លែងកោសិកាស្បែកកណ្ដុរទៅជាកោសិកាដើម pluripotent ត្រូវបានកំណត់អត្តសញ្ញាណ។ កត្តា (តុលា 3/4, Sox2, c-Myc, Klf4) ត្រូវបានរកឃើញ។ ជាលទ្ធផល សាស្រ្តាចារ្យ Yamanaka បានទទួលជោគជ័យក្នុងការបង្កើតកោសិកាដើម pluripotent ដែលជំរុញដោយកត្តាចម្លងចំនួនបួន។ វាអាចត្រូវបានគេមើលឃើញថាកោសិកាដើម pluripotent ដែលជំរុញឱ្យបង្ហាញលក្ខណៈសម្បត្តិស្រដៀងទៅនឹងកោសិកាដើមអំប្រ៊ីយ៉ុង។ កោសិកាដើមអំប្រ៊ីយ៉ុង និងកោសិកាដើម pluripotent ដែលបង្កឡើងគឺស្រដៀងគ្នានៅក្នុង morphology ហ្សែនដែលបានសម្តែង (ប្រៀបធៀបតាមរយៈ RT-PCR និង DNA microarray ) និងគំរូ DNA methylation (ប្រៀបធៀបតាមរយៈបណ្តុំហ្សែន bisulfite) ។
ក្នុងឆ្នាំ 2006 សាស្រ្តាចារ្យ Yamanaka បានទទួលជោគជ័យក្នុងការបង្កើតកោសិកាដើម pluripotent ដោយណែនាំកត្តាចម្លងចំនួន 4 ចូលទៅក្នុង fibroblasts កណ្ដុរ។ នៅឆ្នាំបន្ទាប់គាត់ក៏បានជោគជ័យក្នុងការបង្កើតកោសិកាដើម pluripotent បំផុសគំនិតដោយមនុស្សដោយបង្កើតកត្តាចម្លងចំនួនបួនដូចគ្នានៅក្នុង fibroblasts ស្បែករបស់មនុស្សបានធ្វើ។ ក្នុងឆ្នាំដដែលនោះ ក្រុមការងាររបស់សាស្រ្តាចារ្យ James Thompson នៅសាកលវិទ្យាល័យ Wisconsin Madison បានទទួលជោគជ័យក្នុងការបង្កើតកោសិកាដើម pluripotent ពីកោសិកាស្បែកមនុស្ស ដោយណែនាំហ្សែន (Oct4, Sox2, Nanog និង Lin28) ដោយប្រើមេរោគ retrovirus ។
ដំណើរការដែល fibroblasts កណ្ដុរវិវត្តន៍ទៅជាកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិត ឆ្លងកាត់ដំណាក់កាលជាច្រើនដែលហ្សែនត្រូវបានធ្វើឱ្យសកម្មជាបន្តបន្ទាប់។
ដំណើរការណែនាំលម្អិត
ហ្សែន SOX2 ដើរតួនាទីយ៉ាងសំខាន់ក្នុងការរក្សាបាននូវភាពសម្បូរបែប។ SOX2 គ្រប់គ្រងកន្សោមនៃ 'DKK1' ដែលជាហ្សែនមួយផ្សេងទៀតដែលរារាំង ផ្លូវសញ្ញា Wint ហើយជាលទ្ធផលមិនត្រឹមតែរក្សា 'ពហុប៉ូត' នៃកោសិកាដើមពេញវ័យប៉ុណ្ណោះទេ ប៉ុន្តែថែមទាំងធ្វើនិយ័តកម្មដំណើរការនៃភាពខុសគ្នាទៅជាកោសិកាជាក់លាក់ផងដែរ។ គោលការណ៍នៃសកម្មភាពរបស់ហ្សែន SOX2 យោងតាមប្រព័ន្ធ 'SOX2-DKK1-Wint signal' នេះគឺដូចគ្នាមិនត្រឹមតែនៅក្នុងកោសិកាដើមពេញវ័យប៉ុណ្ណោះទេ ប៉ុន្តែវាក៏មាននៅក្នុងកោសិកាដើមអំប្រ៊ីយ៉ុង និងកោសិកាដើមដែលមានសារធាតុ pluripotent ផងដែរ។
- អាល់កាឡាំង phosphatase (AP) → អង់ទីហ្សែនអំប្រ៊ីយ៉ុងជាក់លាក់ដំណាក់កាលទី 1 (SSEA1) → ហ្សែន Nanog និង Oct4
ក្នុងចំណោមទាំងនេះ AP ចាប់ផ្តើមត្រូវបានបង្ហាញចាប់ពីថ្ងៃទី 3 បន្ទាប់ពីហ្សែនចំនួន 4 (Oct4, Sox2, Klf4, និង c-Myc) ត្រូវបានបង្ហាញនៅក្នុងកោសិកា SSEA1 ចាប់ផ្តើមបង្ហាញចាប់ពីថ្ងៃទី 9 ហើយថ្ងៃទី 4 ខែតុលា និង Nanog ចាប់ផ្តើមបង្ហាញពី ថ្ងៃទី 16. ផ្លាស់ប្តូរទៅជាកោសិកាដើម pluripotent ។ ដូច្នេះ ការបង្ហាញជាបន្តនៃហ្សែនទាំងបួនត្រូវតែកើតឡើងក្នុងរយៈពេល 12 ទៅ 16 ថ្ងៃដើម្បីបង្កើតកោសិកាដើម pluripotent ពេញលេញ។
កត្តាភាពខុសគ្នាដែលទាក់ទង
សុក ២
ហ្សែន c-Myc ដើរតួក្នុងការលើកកម្ពស់ការរីកសាយ និងការផ្លាស់ប្តូរកោសិកា។ លើសពីនេះទៀតទាក់ទងទៅនឹង histone acetyltransferase វា acetylates histones ដើម្បីបន្ធូរទំនាក់ទំនងរបស់ពួកគេជាមួយ DNA ដោយហេតុនេះកាត់បន្ថយស្ថានភាពនៃការបង្ក្រាបហ្សែន។ នេះអនុញ្ញាតឱ្យខែតុលា 3/4 និង Sox2 ភ្ជាប់យ៉ាងល្អទៅនឹងទីតាំងហ្សែនជាក់លាក់ និងជំរុញការចម្លង។ ទោះជាយ៉ាងណាក៏ដោយ ហ្សែននេះគឺជាហ្សែនមហារីកមួយប្រភេទ ហើយសាស្រ្តាចារ្យ Yamanaka បានរកឃើញថា វាមិនចាំបាច់សម្រាប់ការកំណត់កោសិកាឡើងវិញនាពេលអនាគតនោះទេ។
គ-Myc
Klf4 ត្រូវបានគេស្គាល់ថារារាំងដោយផ្ទាល់ p53 ។ p53 ត្រូវបានគេស្គាល់ថាដើម្បីទប់ស្កាត់ Nanog ក្នុងអំឡុងពេលនៃភាពខុសគ្នានៃកោសិកាដើមអំប្រ៊ីយ៉ុង។ កោសិកាដើម pluripotent ដែលត្រូវបានបង្កឡើងបង្ហាញពីប្រូតេអ៊ីន p53 តិចជាង fibroblasts ។ ដូច្នេះ ដោយការទប់ស្កាត់ p53 Klf4 នឹងធ្វើឱ្យ Nanog សកម្ម និងធ្វើឱ្យហ្សែនដែលបង្ហាញជាពិសេសនៅក្នុងកោសិកាដើមអំប្រ៊ីយ៉ុង។
Klf4
កត្តាចម្លងនេះ ត្រូវបានគេស្គាល់ថាជា Oct-3/4 (octamer-binding transcription) ឬ POU5F1 (POU domain, class 5, transcription factor 1) គឺជាប្រូតេអ៊ីនដែលបានអ៊ិនកូដនៅក្នុងរាងកាយដោយហ្សែន POU5F1 ។ ខែតុលា-3/4 គឺជាកត្តាចម្លង homeodomain នៃគ្រួសារ POU ។ ប្រូតេអ៊ីននេះមានសារៈសំខាន់ក្នុងការបន្តដោយខ្លួនឯងនៃកោសិកាដើមអំប្រ៊ីយ៉ុងដែលមិនមានលក្ខណៈខុសគ្នា។ ដូច្នេះ កត្តាចម្លងនេះត្រូវបានប្រើជាសញ្ញាសម្គាល់សម្រាប់ក្រឡាដែលមិនខុសគ្នា។ ការបញ្ចេញមតិនៃខែតុលា-3/4 ត្រូវតែត្រូវបានគ្រប់គ្រង។ ការបញ្ចេញមតិនៃខែតុលា-3/4 ច្រើនពេក ឬតិចពេក បណ្តាលឱ្យកោសិកាដែលមិនមានលក្ខណៈខុសគ្នា។
តុលា-៣/៤
ក្រុមការងាររបស់សាស្រ្តាចារ្យ Shinya Yamanaka នៅសាកលវិទ្យាល័យ Kyoto ក្នុងប្រទេសជប៉ុនបានបង្កើតកោសិកាដើម pluripotent ដោយបញ្ចូលហ្សែន Oct3/4, Sox2, c-Myc និង Klf4 ចូលទៅក្នុងកោសិកាស្បែកកណ្តុរដោយប្រើ មេរោគ retrovirus ។ សាស្ត្រាចារ្យ Shinya Yamanaka បានបង្ហាញថា ការដាក់បញ្ចូលហ្សែនទាំងបួននេះ អាចបង្កើតបានគ្រប់គ្រាន់នូវ pluripotency នៅក្នុងកោសិកា somatic ។
វិធីសាស្រ្តផលិតកោសិកាដើម pluripotent ដោយសុវត្ថិភាព
វិធីសាស្រ្តដំបូងនៃការផលិតកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតគឺដើម្បីជំរុញឱ្យមាន pluripotent ដោយជំរុញឱ្យមានការបញ្ចេញកោសិកាដើម pluripotent ដែលត្រូវបានចាក់ដោយប្រើមេរោគដែលបណ្តាលឱ្យមានភាពខុសគ្នាកើតឡើង។ ទោះជាយ៉ាងណាក៏ដោយ នៅពេលដែលមេរោគមួយត្រូវបានប្រើប្រាស់ដើម្បីចាក់បញ្ចូលកត្តា dedifferentiation ហ្សែនដែលបានមកពីមេរោគអាចត្រូវបានបញ្ចូលទៅក្នុងកោសិកា ដែលបណ្តាលឱ្យមានការផ្លាស់ប្តូរហ្សែន ឬហានិភ័យផ្សេងទៀត។ ដូច្នេះវិធីសាស្រ្ត dedifferentiation ដោយប្រើប្រូតេអ៊ីន ឬ plasmids ដោយមិនបញ្ចូលហ្សែនបរទេសទៅក្នុងហ្សែនត្រូវបានបង្កើតឡើង។
ដើម្បីបញ្ចូល plasmid ឆ្លងចូលទៅក្នុងស្នូលនៃកោសិកាមួយ សារធាតុ nanocarrier មួយផ្សេងទៀតដែលហៅថា nanoparticle Xfect ត្រូវបានប្រើ។ តាមរយៈវិធីសាស្រ្តនេះ ខ្សែកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញអាចត្រូវបានបង្កើតឡើង។
វាក៏មានបច្ចេកវិទ្យាដើម្បីផលិតកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញពី teratoma ដែលត្រូវបានជំរុញនៅក្នុងរាងកាយដោយប្រើសត្វកណ្តុរដែលអាចរៀបចំឡើងវិញបាន។ វិធីសាស្រ្តនេះប្រើសត្វកណ្តុរដែលបង្កើតចេញពីកោសិកាដែលកន្សោមនៃហ្សែនកត្តា pluripotency ត្រូវបានគ្រប់គ្រងដោយ doxycycline ។ កោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតដែលត្រូវបានបង្កើតឡើងតាមរបៀបនេះត្រូវបានវិភាគថាមានសមត្ថភាពខុសគ្នាខ្លាំងជាងកោសិកាដើម pluripotent ដែលបង្កឡើងដែលមានស្រាប់។ វិធីសាស្ត្រដែលមានស្រាប់បានបង្ហាញពីប្រសិទ្ធភាពនៃការបែងចែកកម្រិតទាបបំផុត ដោយមានតែមួយក្នុងចំណោមពួកវាប៉ុណ្ណោះដែលក្លាយជាកោសិកាដើមដែលសម្បូរទៅដោយភាពខុសប្លែកគ្នានៅពេលដែលមានការព្យាយាមលើកោសិកាស្បែកចំនួន 1,000 ។
ការប្រើប្រាស់កោសិកាដើម pluripotent ដែលត្រូវបានជំរុញ
ភាពជឿនលឿននៃបច្ចេកវិទ្យា dedifferentiation
ដំបូងឡើយ វ៉ិចទ័រ retroviral ត្រូវបានប្រើដើម្បីណែនាំហ្សែនទៅក្នុងកោសិកា somatic ។ ដោយសារវ៉ិចទ័រ retroviral ត្រូវបានប្រើប្រាស់ ហ្សែនដែលបានណែនាំត្រូវបានបញ្ចូលទៅក្នុងហ្សែនដោយចៃដន្យ ដែលមានផលប៉ះពាល់នៃការបង្កមហារីក។ ក្នុងឆ្នាំ 2008 ក្រុមរបស់សាស្រ្តាចារ្យ Shinya Yamanaka បានជំរុញកោសិកាដើម pluripotent ដោយគ្មានផលប៉ះពាល់ដូចជា teratoma ដោយបញ្ចូល cDNA ដែលមានផ្ទុក Oct3/4, Sox2, c-Myc និង Klf4 ទៅក្នុងកោសិកា somatic កណ្តុរដោយគ្មានវ៉ិចទ័រមេរោគ។ លើសពីនេះ ថ្មីៗនេះ ជាជម្រើសមួយសម្រាប់ប្រព័ន្ធមេរោគ សមាសធាតុម៉ូលេគុលតូចៗ ប្រូតេអ៊ីន និងវ៉ិចទ័រមិនបញ្ចូលមិនមេរោគ (វ៉ិចទ័រ episomal) ត្រូវបានគេប្រើដើម្បីអនុញ្ញាតឱ្យហ្សែនដែលរក្សានូវសារធាតុ pluripotency ត្រូវបានផ្ទេរទៅក្នុងកោសិកាដោយមិនត្រូវបានដាក់បញ្ចូលទៅក្នុងកោសិកា។ ហ្សែននៃកោសិកា somatic ខ្ញុំកំពុងប្រើវិធីសាស្ត្រនេះ។ ទោះបីជាបច្ចេកវិទ្យា dedifferentiation ទាំងនេះកំពុងត្រូវបានបង្កើតឡើងក៏ដោយ ក៏បញ្ហាជាមួយនឹងប្រសិទ្ធភាព dedifferentiation ទាបជាងគួរឱ្យកត់សម្គាល់ និងការផលិតឡើងវិញបើប្រៀបធៀបទៅនឹងបច្ចេកទេសប្រើប្រាស់មេរោគនៅតែបន្តត្រូវបានបង្ហាញ។
នៅពេលដែលកោសិកា somatic ត្រូវបានជំរុញឱ្យក្លាយទៅជាកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញ កត្តាដែលមានហ្សែន oncogenic (c-Myc, Klf4) ត្រូវបានណែនាំដោយប្រើមេរោគ retroviruses ដូច្នេះវាមានហានិភ័យនៃការបង្កមហារីក និងការផ្លាស់ប្តូរមុខងារកោសិកា។ ទោះជាយ៉ាងណាក៏ដោយ ក្នុងឆ្នាំ 2008 ក្រុមរបស់សាស្រ្តាចារ្យ Shinya Yamanaka បានបង្កើតវិធីសាស្រ្តមួយដើម្បីបង្កើតកោសិកាដើម pluripotent ដែលបង្កឡើងដោយមិនមានហ្សែន Myc ។ ក្រោយមក កោសិកាដើមដែលបណ្តាលឱ្យមានភាពខុសគ្នា មិនមែនជាកោសិកាស្បែកទេ ប៉ុន្តែកោសិកាដើមសរសៃប្រសាទ ដែលជាកោសិកាដើមពេញវ័យដែលបង្ហាញពីខាងក្នុងរបស់ Sox2, Myc និង Klf4 ហើយកោសិកាដើមដែលបែងចែកត្រូវបានបង្កើតឡើងដោយគ្មាន Klf4 ដែលជាហ្សែន oncogenic មួយផ្សេងទៀតក្នុងចំណោមបីដែលនៅសល់។ កត្តា។ វាត្រូវបានផលិត ហើយចាប់តាំងពីកោសិកាស្បែកបង្ហាញ C-Myc និង Klf4 ផងដែរ មានរបាយការណ៍មួយថា ភាពខុសគ្នាគឺជោគជ័យជាមួយនឹងតែ Oct4 និង Sox2 ក្នុងការសិក្សាតាមដាន។ នេះធ្វើឱ្យវាអាចបង្កើតកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញដោយមិនចាំបាច់ប្រើហ្សែន oncogenic ។
វាត្រូវបានបង្ហាញថាកត្តាតិចជាងបួន (Oct3/4, Sox2, c-Myc, និង Klf4) ត្រូវបានទាមទារដើម្បីជំរុញឱ្យមានពហុភាពនៅក្នុងប្រភេទមួយចំនួននៃកោសិកា។ ជាឧទាហរណ៍ មានតែថ្ងៃទី 4 ប៉ុណ្ណោះដែលត្រូវការដើម្បីជំរុញកោសិកាសរសៃប្រសាទនៅក្នុងសត្វកណ្តុរ។ ក្រុមរបស់សាស្រ្តាចារ្យ Seung-kwon Yoo មកពីនាយកដ្ឋានជីវបច្ចេកវិទ្យានៅសាកលវិទ្យាល័យកូរ៉េបានបង្កើតកោសិកាដើមសរសៃប្រសាទដោយបញ្ចូលហ្សែន 'Id3' ទៅក្នុងកោសិកា somatic របស់កណ្តុរ ហើយបន្ទាប់មកបញ្ចូលពួកវាទៅក្នុងកោសិកាដើម pluripotent ដោយប្រើតែហ្សែន 'Oct4' ប៉ុណ្ណោះ។
ដើម្បីបង្កើតកោសិកាដើម pluripotent ប្រកបដោយគុណភាព ដែលបំពេញតាមតម្រូវការទីផ្សារនានានាពេលអនាគត និងពន្លឿនការធ្វើពាណិជ្ជកម្មរបស់ពួកគេ វាជារឿងចាំបាច់ក្នុងការអភិវឌ្ឍបច្ចេកវិទ្យាឌីផេរ៉ង់ស្យែលប្រកបដោយសុវត្ថិភាព និងប្រសិទ្ធភាពខ្ពស់ជាមុនសិន។
បន្ទាប់មកនៅឆ្នាំ 2010 ក្រុមសាស្រ្តាចារ្យ Kim Hyo-soo នៃមន្ទីរពេទ្យសាកលវិទ្យាល័យជាតិសេអ៊ូល និងសាស្រ្តាចារ្យ Kwon Kwon Wook នៃវិទ្យាស្ថានស្រាវជ្រាវជីវវេជ្ជសាស្ត្រ ដែលបានទទួលជោគជ័យក្នុងការបង្កើត iPS ដោយការចាក់ប្រូតេអ៊ីនដែលចម្រាញ់ចេញពីកោសិកាដើមអំប្រ៊ីយ៉ុងចូលទៅក្នុងកោសិកា somatic ជាលើកដំបូងនៅក្នុង ពិភពលោកក្នុងឆ្នាំ 2010 ត្រូវបានបោះពុម្ភផ្សាយនៅក្នុង 'Biomaterials' ចេញផ្សាយខែឧសភា ដែលជាទិនានុប្បវត្តិសិក្សាអន្តរជាតិក្នុងវិស័យជីវវត្ថុធាតុក្នុងឆ្នាំ 2015។ តាមពិត ក្រដាសនេះចែងថាប្រសិទ្ធភាពនៃដំណើរការ dedifferentiation អាចប្រសើរឡើងយ៉ាងខ្លាំង ប្រសិនបើប្រូតេអ៊ីនចម្រាញ់ចេញពី iPS ជាជាងកោសិកាដើមអំប្រ៊ីយ៉ុងត្រូវបានចាក់ចូលទៅក្នុងកោសិកា somatic ។ នៅក្នុងបទសម្ភាសន៍ជាមួយសាស្រ្តាចារ្យ Kim សាស្រ្តាចារ្យ Kim បាននិយាយថា "អត្រានៃការបែងចែកទៅក្នុង iPS គឺលឿនជាង 10 ដងសម្រាប់កោសិកា somatic ដែលចាក់ដោយប្រូតេអ៊ីនដែលស្រង់ចេញពី iPS ជាងពេលដែលប្រូតេអ៊ីនពីកោសិកាដើមអំប្រ៊ីយ៉ុងត្រូវបានចាក់" ។ ក្រុមរបស់សាស្ត្រាចារ្យ Kim ក៏បានរកឃើញថា សារធាតុដែលបង្កើតឥទ្ធិពលនេះគឺ 'Zscan4' ក្នុងចំណោមប្រូតេអ៊ីន iPS។ សាស្ត្រាចារ្យ Kim បាននិយាយថា "ប្រូតេអ៊ីននេះមានឥទ្ធិពលធ្វើឱ្យកោសិការាងកាយមានភាពរស់រវើកឡើងវិញ ធ្វើឱ្យដំណើរការឡើងវិញនៃកោសិការាងកាយកាន់តែមានប្រសិទ្ធភាព" ។ Reprogramming សំដៅលើការផ្លាស់ប្តូរកម្មវិធីដែលកំណត់ជោគវាសនានៃក្រឡាជាក់លាក់មួយដើម្បីបែងចែកទៅជាក្រឡាមួយណា។
មានវិធីសាស្រ្តនៃការបង្កើត dedifferentiation នៅក្នុងកោសិកាដើមសរសៃប្រសាទ ដែលជាកោសិកាដើមមនុស្សពេញវ័យ ជាជាង dedifferentiating កោសិកា somatic ។ ដោយប្រើវិធីសាស្រ្តនេះ វាបង្ហាញពីប្រសិទ្ធភាពទាបបំផុត ព្រោះនៅពេលដែល dedifferentiation ត្រូវបានជំរុញនៅក្នុងកោសិកាស្បែក 1,000 ដែលជាកោសិកា somatic ទូទៅ កោសិកាមួយក្នុងចំណោមពួកវាបានក្លាយទៅជាកោសិកាដើម pluripotent។ ទោះជាយ៉ាងណាក៏ដោយ នៅពេលដែល dedifferentiation ត្រូវបានជំរុញនៅក្នុងកោសិកាដើមសរសៃប្រសាទ ដែលជាដើមពេញវ័យ។ កោសិកាពួកវាមានការរីកចម្រើនជាងកោសិកា somatic ប្រសិទ្ធភាព dedifferentiation គឺខ្ពស់ជាងប្រហែល 100 ទៅ 3000 ដង។ លើសពីនេះទៀតពេលវេលា dedifferentiation គឺប្រហែល 5 ដងលឿនជាងពេលវេលា dedifferentiation នៃកោសិកា somatic ដែលមានរយៈពេល 2 សប្តាហ៍ដែលបង្ហាញពីប្រសិទ្ធភាពខ្ពស់។ សរុបសេចក្តីមក ប្រសិនបើកោសិកាដើមពេញវ័យ ដែលជាកោសិកាដែលបង្ហាញពីកត្តា pluripotency ខាងក្នុង ត្រូវបានប្រើដើម្បីជំរុញឱ្យមានភាពខុសគ្នា នោះ dedifferentiation អាចត្រូវបានបង្កឡើង ទោះបីជាកត្តាត្រូវបានព្យាបាលខាងក្រៅក៏ដោយ។
កោសិកាដើម pluripotent បង្កឡើងជាការព្យាបាលកោសិកាដើម [dead link]
កោសិកាដើម រួមទាំងកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតអាចជំនួសកោសិកាដែលខូចដោយជំងឺដូចជាជំងឺផាកឃីនសុន ឬជំងឺទឹកនោមផ្អែមប្រភេទទី 1 ។ ការព្យាបាលកោសិកាដើមដោយប្រើកោសិកាដើម pluripotent ជំរុញឱ្យមានការប្តូរសរីរាង្គដោយស្វ័យប្រវត្ត ដូច្នេះកាត់បន្ថយប្រូបាប៊ីលីតេនៃអ្នកជំងឺដែលបង្កើតប្រតិកម្មបដិសេធភាពស៊ាំ។ ទោះយ៉ាងណាក៏ដោយ មានបញ្ហាដែលវាអាចបណ្តាលឱ្យមានការផ្លាស់ប្តូរ ឬភាពមិនប្រក្រតីនៃហ្សែនផ្សេងទៀត។ ដូច្នេះ ការស្រាវជ្រាវតាមដានជាច្រើនគឺត្រូវការជាចាំបាច់ ដើម្បីធានាការប្រើប្រាស់ប្រកបដោយសុវត្ថិភាពចំពោះអ្នកជំងឺ។
ប្រើក្នុងការស្រាវជ្រាវវេជ្ជសាស្រ្ត
ការដោះដូរដ៏សំខាន់ក្នុងការផលិតកោសិកា iPS នៅតែត្រូវបានសិក្សាដោយសារតែបញ្ហាដែលបានរៀបរាប់ខាងលើ។ វិធីសាស្រ្តភាគច្រើនដែលមិនពឹងផ្អែកលើរបាំងវិស្វកម្មហ្សែនគឺមិនមានប្រសិទ្ធភាពទេ ខណៈពេលដែលវិធីសាស្ត្រដែលពឹងផ្អែកលើការរួមបញ្ចូលនៃការប្តូរហ្សែនត្រូវបានព្យាយាម បើទោះបីជា បច្ចេកវិទ្យា និងវិធីសាស្រ្តជាច្រើនត្រូវបានព្យាយាម។ បច្ចុប្បន្នយើងកំពុងប្រឈមមុខនឹងបញ្ហានៃការសរសេរកម្មវិធីឡើងវិញមិនពេញលេញ និងការវិវត្តនៃដុំសាច់។ យុទ្ធសាស្ត្រទ្រង់ទ្រាយធំមួយទៀតគឺដើម្បីអនុវត្តការកំណត់លក្ខណៈប្រូតេអ៊ីននៃកោសិកា iPS ។ ការស្រាវជ្រាវបន្ថែម និងយុទ្ធសាស្ត្រថ្មីគឺត្រូវបានទាមទារ ដើម្បីផ្តល់នូវដំណោះស្រាយដ៏ល្អប្រសើរមួយ។ វិធីសាស្រ្តមួយអាចព្យាយាមទាញយកទិដ្ឋភាពវិជ្ជមាននៃយុទ្ធសាស្ត្រទាំងនេះ ហើយបញ្ចូលវាទៅក្នុងបច្ចេកទេសដ៏មានប្រសិទ្ធភាពមួយសម្រាប់ការសរសេរកម្មវិធីកោសិកាឡើងវិញសម្រាប់កោសិកា iPS ។
វិធីសាស្រ្តមួយទៀតគឺការប្រើកោសិកា iPS ដែលកើតចេញពីអ្នកជំងឺដើម្បីកំណត់អត្តសញ្ញាណថ្នាំព្យាបាលដែលអាចធ្វើត្រាប់តាម phenotype នៃជំងឺ។ ជាឧទាហរណ៍ កោសិកា iPS ដែលកើតចេញពីអ្នកជំងឺដែលរងផលប៉ះពាល់ដោយ EEC (Ectoderal Edysplasia Syndrome) ដែលហ្សែន p63 ត្រូវបានផ្លាស់ប្តូរ ត្រូវបានរៀបចំឡើងវិញដោយកត្តា reprogramming (OSKM) ដើម្បីក្លាយជាកោសិកាដើម pluripotent ដែលបន្ទាប់មកត្រូវបានបែងចែកទៅជាកោសិកាជាក់លាក់អ្នកជំងឺ។ មានអត្ថន័យនៅក្នុងនោះ វាអនុញ្ញាតឱ្យបង្កើតផលិតផលព្យាបាលកោសិកាតាមតម្រូវការ។
សមស្របសម្រាប់ phenotype ជំងឺ
តាមរយៈការទទួលបានកោសិកា somatic ការបង្កើតកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិត និងការបែងចែកពួកវានៅក្នុង vitro គំរូជំងឺអាចទទួលបានដោយសិក្សាពីដំណើរនៃជំងឺផ្សេងៗ។ បច្ចុប្បន្ននេះកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតកំពុងត្រូវបានបង្កើត និងសិក្សាពីអ្នកជំងឺដែលទទួលរងពីជំងឺផ្សេងៗ ហើយ phenotypes ដែលទាក់ទងនឹងជំងឺកំពុងត្រូវបានគេសង្កេតឃើញនៅក្នុងគំរូជំងឺទាំងនេះ។ ឧទាហរណ៍ នៅក្នុងករណីនៃកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញពីអ្នកជំងឺដែលមានសាច់ដុំឆ្អឹងខ្នង ការបាត់បង់បន្តិចម្តងៗនៃណឺរ៉ូនម៉ូទ័រត្រូវបានគេសង្កេតឃើញ។ នៅពេលដែលកោសិកាដើម pluripotent បង្កឡើងពីអ្នកជំងឺដែលមានកង្វះ alpha1-antitrypsin-ត្រូវបានបែងចែកទៅជា hepatocytes ការប្រមូលផ្តុំនៃ lipids និង glycogen កើនឡើង។ កោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតក៏ត្រូវបានគេប្រើផងដែរក្នុងការធ្វើគំរូជំងឺនៃជម្ងឺអាល់ហ្សៃមឺរ។
ការស្រាវជ្រាវតាមកោសិកាក្នុងការអភិវឌ្ឍន៍ថ្នាំ
កោសិកាដែលមានលក្ខណៈខុសប្លែកគ្នានៅក្នុង vitro ដោយផ្អែកលើកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិត ត្រូវបានគេប្រើយ៉ាងទូលំទូលាយក្នុងការអភិវឌ្ឍថ្នាំថ្មី និងក្នុងការធ្វើតេស្តសុវត្ថិភាពនៃថ្នាំថ្មី។ ជាឧទាហរណ៍ វាត្រូវបានគេរកឃើញថា kinetin ធ្វើឱ្យធម្មតាផ្នែកខ្លះនៃការបែងចែកមិនធម្មតានៃហ្សែន IKBKAP ដែលបណ្តាលឱ្យមានភាពស្វ័យភាពក្នុងគ្រួសារ។ លើសពីនេះទៀត beta-blockers និង ion channel blockers ក៏ត្រូវបានគេរកឃើញថាមានប្រសិទ្ធភាពក្នុងការគ្រប់គ្រង phenotype នៃ long QT syndrome ។
ការព្យាបាលភាពគ្មានកូន
នៅថ្ងៃទី 8 ខែកក្កដា ឆ្នាំ 2009 ក្រុមស្រាវជ្រាវរបស់ វេជ្ជបណ្ឌិត Karim Nayenia នៅ សាកលវិទ្យាល័យ Newcastle ក្នុងចក្រភពអង់គ្លេស និង វិទ្យាស្ថាន New England Complex Systems Institute (NESCI) បានផលិត មេជីវិតឈ្មោលនៅក្នុង vitro ដំបូងបង្អស់របស់ពិភពលោកពីកោសិកាដើមអំប្រ៊ីយ៉ុងរបស់មនុស្ស។ កោសិកាដើមអំប្រ៊ីយ៉ុងអាចបែងចែកទៅជាកោសិកាប្រភេទណាក៏បាន ប៉ុន្តែនេះជាលើកដំបូងដែលពួកវាត្រូវបានដាំដុះដោយជោគជ័យទៅជាមេជីវិតឈ្មោល។ ទោះយ៉ាងណាក៏ដោយ កោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតមិនត្រូវបានប្រើទេ។ វេជ្ជបណ្ឌិត Karim Nayenia មកពីប្រទេសអ៊ីរ៉ង់ កំពុងធ្វើការស្រាវជ្រាវនៅប្រទេសអាល្លឺម៉ង់ ប៉ុន្តែនៅពេលដែលរដ្ឋាភិបាលអាល្លឺម៉ង់បានហាមឃាត់ការស្រាវជ្រាវកោសិកាដើមអំប្រ៊ីយ៉ុងរបស់មនុស្ស គាត់បានផ្លាស់ទៅសាកលវិទ្យាល័យ Newcastle ក្នុងប្រទេសអង់គ្លេសក្នុងឆ្នាំ 2006 ដើម្បីបន្តការស្រាវជ្រាវរបស់គាត់។
នៅថ្ងៃទី 5 ខែសីហា ឆ្នាំ 2011 ក្រុមស្រាវជ្រាវរបស់សាស្រ្តាចារ្យ Michinori Saito នៅសាកលវិទ្យាល័យ Kyoto ក្នុងប្រទេសជប៉ុនបានក្លាយជាមនុស្សដំបូងគេក្នុងពិភពលោកដែលរៀបចំកោសិកា somatic របស់កណ្តុរចូលទៅក្នុងកោសិកាដើម pluripotent បំផុសគំនិត រៀបចំពួកវាម្តងទៀតដើម្បីបង្កើតមេជីវិតឈ្មោល និងបង្កកំណើតនៅក្នុង vitro ដើម្បីផ្តល់កំណើតដល់ទារក។ សត្វកណ្ដុរ។ នៅថ្ងៃដដែលនោះវាក៏ត្រូវបានគេបង្ហាញនៅលើអ៊ីនធឺណិតកំណែ របស់ទស្សនាវដ្ដី Cell ដែរ។ វាជាលើកដំបូងនៅលើពិភពលោកដែលបង្កើតមេជីវិតឈ្មោលពីកោសិកាដើមអំប្រ៊ីយ៉ុងកណ្តុរ ដើម្បីបង្កើតមេជីវិតឈ្មោលពីកោសិកាដើម pluripotent ដែលជំរុញដោយកណ្តុរ និងសម្រេចបានជោគជ័យក្នុងការបង្កកំណើត និងកំណើតតាមរយៈមេជីវិតឈ្មោល។
ក្នុងឆ្នាំ 2012 ក្រុមស្រាវជ្រាវ នៅសាកលវិទ្យាល័យ Pittsburgh ក្នុងសហរដ្ឋអាមេរិកបានក្លាយជាមនុស្សដំបូងគេក្នុងពិភពលោកដែលទទួលបានជោគជ័យក្នុងការបង្កើតកោសិកាមេជីវិតឈ្មោលដោយបំប្លែងកោសិកាស្បែកពីបុរសដែលមានមុខងារបន្តពូជធម្មតាទៅជាកោសិកាដើម pluripotent បង្កឡើង។
នៅថ្ងៃទី 1 ខែឧសភា ឆ្នាំ 2014 វេជ្ជបណ្ឌិត Rayho Pera នៃវិទ្យាស្ថាន Stem Cell Biology and Regenerative Medicine នៃ សាកលវិទ្យាល័យ Stanford បានកាត់បន្ថយកោសិកាស្បែករបស់បុរសដែលមានជំងឺ azoospermia ដែលមិនមានមេជីវិតឈ្មោលដោយសារតែភាពមិនប្រក្រតីនៃក្រូម៉ូសូម Y ចូលទៅក្នុងកោសិកាដើម pluripotent ដែលបង្កឡើង ហើយចាក់ចូលទៅក្នុង ពងស្វាសរបស់សត្វកណ្ដុរ។ យើងជោគជ័យក្នុងការរីកលូតលាស់ កោសិកាមេជីវិតឈ្មោល ដែលជាកោសិកាមេជីវិតឈ្មោលដំណាក់កាលដំបូង ។ ជាលើកដំបូងនៅក្នុងពិភពលោក មេជីវិតឈ្មោលត្រូវបានផលិតចេញពីស្បែករបស់បុរស azoospermic ។
ដែនកំណត់
ក្នុងឆ្នាំ 2006 ក្រុមស្រាវជ្រាវរបស់ Yamanaka បានជ្រើសរើសហ្សែនចំនួន 24 ដែលអាចជំរុញឱ្យមាន pluripotency នៅក្នុងកោសិកា somatic ជាបេក្ខជន។ ក្នុងចំនោមពួកគេ ខែតុលា 3/4 និង Sox2 ត្រូវបានគេរកឃើញថាជាកត្តាសំខាន់សម្រាប់ការបង្កើតកោសិកាដើម pluripotent ហើយ Nanog ដែលត្រូវបានគេស្គាល់នៅក្នុងការសិក្សាពីមុនថាជាកត្តាចម្លងដ៏សំខាន់មួយដែលរក្សា pluripotency ត្រូវបានគេរាយការណ៍ថាមិនទាក់ទងទៅនឹងយន្តការ reprogramming ពិតប្រាកដនោះទេ។ . លើសពីនេះទៀត វាត្រូវបានគេរកឃើញថា c-Myc និង Klf4 ដើរតួនាទីយ៉ាងសំខាន់ក្នុងការបង្កើតកោសិកាដើម pluripotent ដែលត្រូវបានជំរុញ ហើយកត្តាដែលទាក់ទងនឹងដុំសាច់ទាំងពីរនេះត្រូវបានផ្សារភ្ជាប់ទៅនឹង oncogenes ផ្សេងទៀត (E-Ras, Tcl1, ß-catenin, Stat3) ។ វាត្រូវបានរាយការណ៍ថាវាមិនអាចទៅរួចទេក្នុងការជំនួសវា។ ក្រោយមកក្នុងឆ្នាំ 2007 ក្រុមស្រាវជ្រាវ Thomson បានធ្វើការពិសោធន៍ដោយប្រើបន្សំផ្សេងគ្នា (Oct4, Sox2, Nanog, Lin28) ជាងការពិសោធន៍របស់ក្រុមស្រាវជ្រាវ Yamanaka ជាលទ្ធផលកត្តា Nanog ដែលត្រូវបានគេដឹងថាមិនទាក់ទងទៅនឹងយន្តការ reprogramming នៅក្នុងការសិក្សាពីមុន វាត្រូវបានគេរកឃើញថាវារួមចំណែកដល់ការបង្កើនប្រសិទ្ធភាពនៃ reprogramming និងបង្កើនអត្រារស់រានមានជីវិតដំបូងនៃកោសិកា reprogrammed ហើយវាត្រូវបានគេរាយការណ៍ថា Lin28 ក៏ចូលរួមក្នុងការបង្កើតកោសិកាដើម pluripotent ផងដែរ។ ទោះបីជាការសិក្សាជាច្រើនបានព្យាយាមវិភាគយន្តការជាមូលដ្ឋាននៃកោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិត និងធ្វើអោយប្រសើរឡើងនូវភាពពេញលេញនៃបច្ចេកវិទ្យាក៏ដោយ កោសិកាដើម pluripotent ដែលត្រូវបានបំផុសគំនិតនៅតែមានដែនកំណត់មួយចំនួននៅក្នុងការអនុវត្តផ្នែកព្យាបាល។ ការប្រើប្រាស់មេរោគសម្រាប់ការណែនាំហ្សែន (iPSCs) និងដុំសាច់នៃកត្តាដូចជា c-Myc និង Klf4 ត្រូវបានចាត់ទុកថាជាដែនកំណត់តំណាងនៃកោសិកាដើម pluripotent ដែលបង្កឡើង។
លេខយោង
សូមមើលផងដែរ
- Shinya Yamanaka
- រង្វាន់ណូបែលផ្នែកសរីរវិទ្យា ឬវេជ្ជសាស្ត្រ
- សទិសន័យ
- កោសិកាដើម pluripotent
- កោសិកាដើម pluripotent សិប្បនិម្មិត
- កោសិកា IPS
This article uses material from the Wikipedia ភាសាខ្មែរ article ការបង្កឡើងរបស់ កោសិកាដើម pluripotent, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). ខ្លឹមសារអត្ថបទប្រើប្រាស់បានក្រោមអាជ្ញាបណ្ឌCC BY-SA 4.0 លើកលែងតែមានបញ្ជាក់ផ្សេងពីនោះ។ Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki ភាសាខ្មែរ (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.