Серин
Серин (съкратено Ser или S) е α-аминокиселина с химическа формула HО2CCH(NH2)CH2OH.
Тя е една от протеиногенните аминокиселини. Нейните кодони в генетичния код са UCU, UCC, UCA, UCG, AGU, UGC. Поради наличието на хидроксилна група, серина се класифицира като полярна аминокиселина.
| Серин | |
  | |
| Имена | |
|---|---|
| По IUPAC | Серин |
| Други | 2-амино-3-хидроксипропанова киселина |
| Свойства | |
| Формула | C3H7N1O3 |
| Моларна маса | 105.09 g/mol |
| Външен вид | бели кристали или прах |
| Плътност | 1.603 g/cm3 |
| Точка на топене | 246 °C разпадане |
| Разтворимост във вода | разтворим |
| pKa карбокси | 2.21 |
| pKb амино | 9.15 |
| Идентификатори | |
| CAS номер | 56-45-1, 302-84-1, 312-84-5 |
| PubChem | 617 |
| ChemSpider | 5736 |
| DrugBank | DB00133 |
| KEGG | D00016 |
| MeSH | D012694 |
| ChEBI | 17115 |
| ChEMBL | CHEMBL11298 |
| SMILES | C([C@@H](C(=O)O)N)O |
| InChI | InChI=1S/C3H7NO3/c4-2(1-5)3(6)7/h2,5H,1,4H2,(H,6,7)/t2-/m0/s1 |
| InChI ключ | MTCFGRXMJLQNBG-REOHCLBHSA-N |
| UNII | 452VLY9402 |
| Gmelin | 2570 |
| Данните са при стандартно състояние на материалите (25 °C, 100 kPa), освен ако не е указано друго. | |
| Серин в Общомедия | |
Разпространение и биосинтез
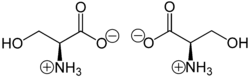
Това е една от природно срещащите се протеиногенни аминокиселини. Само L-стереоизомера се намира естествено в протеините. Тя е заменима аминокиселина в човешкото хранене, тъй като се синтезира в тялото от различни метаболити, включително глицин. Първоначално е получена от копринен протеин, особено богат източник през 1865. Името произлиза от латинското наименование на коприната, sericum. Структурата на серина бива установена през 1902 г.
Биосинтезата на серин започва с окислението на 3-фосфоглицерат до 3-фосфохидроксипируват и НАДН. Редуктивно аминиране на получения кетон, последвано от хидролиза дава серин. Серин хидроксиметилтрансфераза катализира обратната реакция на серин до глицин.
Тази аминокиселина може също да се получи спонтанно в природата, когато ултравиолетова светлина освети мръсен лед, в който присъстват вещества като вода, метанол, циановодород и амоняк, предполагайки лесното му образуване в студените райони на космоса.
Производство
Индустриално, L-серин се получава чрез ферментация, като годишния добив се оценява между 100 и 1000 тона. В лабораторни условия рацемичен серин може да бъде приготвен от метил акрилат на няколко етапа:
Роля в организма
Метаболитна

Серинът е важен за метаболизма с това, че участва в биосинтеза на пурини и пиримидини. Прекурсор е на няколко аминокиселини, включително глицин и цистеин, както и триптофан в бактериите. Той е прекурсор и на множество други метаболити, включително сфинголипиди и фолат, който е основния донор на едноатомни въглеродни остатъци (метилови групи) в биосинтеза на организма.
Структурна
Серинът изпълнява важна роля в каталитичната функция на много ензими. Доказано е присъствието му в активните центрове на химотрипсин и трипсин и много други ензими. Така наречените нервнопаралитични газове, както и много други вещества използвани като инсектициди, притежават действие основаващо се на свързване с активния център на ензима ацетилхолинестераза, което напълно инхибира ензима.
Като съставка на протеините неговата странична верига може да претърпи O-свързано гликиране, което може да бъде функционално свързано с диабет.
Серинът е един от трите аминокиселинни остатъка в протеините, които се фосфорилират от кинази по време на сигналната трансдукция в еукариотите. Фосфорилираните серинови остатъци най-често се наричат фосфосерин. Обратният процес се катализира от ензими, наречени серин фосфатази.
Серин протеазите са често срещан тип протеази.
Серин чрез декарбоксилиране образува етаноламин, който участва в структурата на фосфатидилсерините, от които се синтезира фосфатидилхолин.
Сигнална
D-серин, синтезиран в мозъка от серин рацемаза от L-серин (неговия енантиомер), служи едновремнно като невротрансмитер и глиотрансмитер чрез активиране на NMDA-рецепторите, правейки ги способни да се отварят при едновремнно свързване с глутамат. D-серинът е силен агонист в глициновото свързващо място в NMDA-рецепторните глутаматергични неврони. За да се отвори рецептора, той трябва задължително да е свързан с глутамат и или глицин или D-серин. Всъщност самият D-серин е много по-силен агонист на глицин-свързващото място от колкото самият глицин. Смятало се е, че D-серин съществува само в бактериите; той представлява едва втората D-аминокиселина, която бива открита че съществува естествено в човека, наличен като сигнална молекула в мозъка, скоро след откритието на D-аспартат. Ако това откритие се бе случило по-рано, участъка в NMDA-рецептора нямаше да се казва глицинов, а D-серинов.
Източници
 | Тази страница частично или изцяло представлява превод на страницата Serine в Уикипедия на английски. Оригиналният текст, както и този превод, са защитени от Лиценза „Криейтив Комънс – Признание – Споделяне на споделеното“, а за съдържание, създадено преди юни 2009 година – от Лиценза за свободна документация на ГНУ. Прегледайте историята на редакциите на оригиналната страница, както и на преводната страница, за да видите списъка на съавторите. ВАЖНО: Този шаблон се отнася единствено до авторските права върху съдържанието на статията. Добавянето му не отменя изискването да се посочват конкретни източници на твърденията, които да бъдат благонадеждни. |
This article uses material from the Wikipedia Български article Серин, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Съдържанието е достъпно под условията на лиценза CC BY-SA 4.0, освен ако не е посочено друго. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Български (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.
