氢键: 分子间作用力的一种
氫鍵是分子間作用力的一種,是一种永久偶极之间的作用力,氢键发生在已经以共价键与其它原子键结合的氢原子与另一个原子之间(X-H…Y),通常发生氢键作用的氢原子两边的原子(X、Y)都是电负性较强的原子。氢键既可以是分子间氢键,也可以是分子内的。其键能最大约为200kJ/mol,一般为5-30kJ/mol,比一般的共价键、离子键和金属键键能要小,但强于静电引力。

成键
氢键通常可用X-H…Y來表示。其中X以共价键与氢相连,具有较高的电负性,可以稳定负电荷,因此氢易解离,具有酸性(质子给予体)。而Y则具有较高的电子密度,一般是含有孤电子对的原子,容易吸引氢原子,从而与X和H原子形成三中心四电子键。
键能
氢键键能大多在25-40kJ/mol之间。一般认为键能小於25kJ/mol的氢键属于较弱氢键,键能在25-40kJ/mol的属于中等强度氢键,而键能大於40kJ/mol的氢键则是较强氢键。 曾经有一度认为最强的氢键是[HF2]−中的FH…F−键,计算出的键能大约为169kJ/mol。 而事实上,用相同方法计算甲酸和氟离子间的[HCO2H…F−]氢键键能,结果要比HF2−的高出大约30kJ/mol。
| 较弱 | 中等 | 较强 | |||
|---|---|---|---|---|---|
| HSH…SH2 NCH…NCH H2NH…NH3 MeOH…OHMe HOH…OH2 | 7 16 17 19 22 | FH…FH ClH…OMe2 FH…OH2 | 29 30 38 | HOH…Cl− HCONH2…OCHNH2 HCOOH…OCHOH HOH…F− H2OH+…OH2 FH…F− HCO2H…F− | 55 59 59 98 151 169 ~200 |
常见氢键的平均键能数据为:
- F—H
:F (155 kJ/mol 或 40 kcal/mol)
- O—H
:N (29 kJ/mol 或 6.9 kcal/mol)
- O—H
:O (21 kJ/mol 或 5.0 kcal/mol)
- N—H
:N (13 kJ/mol 或 3.1 kcal/mol)
- N—H
:O (8 kJ/mol 或 1.9 kcal/mol)
- HO—H
:OH3+ (18 kJ/mol 或 4.3 kcal/mol)
成键原子
典型的氢键中,X和Y是电负性很强的F、N和O原子。但C、S、Cl、P甚至Br和I原子在某些情况下也能形成氢键,但通常键能较低。
碳在与数个电负性强的原子相连时也有可能产生氢键。例如在氯仿CHCl3中,碳原子直接与三个氯原子相连,氯原子周围电子云密度较大,因而氢原子周围即带有部分正电荷,碳也因此参与了氢键的形成,扮演了质子供体的角色。
芳香环、碳碳三键或双键在某些情况下都可作为电子供体,与强极性的X-H(如-O-H)形成氢键。
方向
X-H…Y往往不是严格的直线。 哪怕不算分叉的氢键,一对一的氢键中也有很多键角处在150°-180°之间的情况,氟化氢长链中的氢键即是一例。
对称氢键
通常氢是通过共价键与X原子相连,并通过较长和较弱的“氢链”与Y原子连接,即使X与Y是相同的元素,X-H和H…Y距离也往往不相等。但在M+HA2−型的酸式盐中,其中A是F−或某些有机酸(如乙酸和苯甲酸),氢原子恰好处于X和Y原子的中心(X-H…Y)。这一类例子被称作对称氢键,它们往往键能较大,键长较短。
对称氢键和不对称氢键的现象往往难以解释。一个比较认同的解释是,将FHF−离子中的氢键看成氢桥,类似于乙硼烷中的BHB硼桥键。只不过硼桥键是三中心两电子键,而氢桥键是三中心四电子键。
双氢键
1995年以来,报道了许多种分子间存在一种被称为双氢键的新型分子间力,可用通式AH…HB表示。 双氢键的键长一般小于220pm,极限可能为270pm,键能从n~n*10kJ/mol不等,相当于传统分子间力能量数量级。双氢键的一些例子包括:BH4−…HCN、BH4−…CH4、LiH…NH4、LiH…HCN、LiH…HC≡CH,CH4…H-NH3+和H-Be-H…H-NH3等,其中以BH4−…HCN双氢键的键长为最短(171pm),键能也最高(75.44kJ/mol),远大于水和HF间的氢键键能。目前对双氢键的研究还不是很深入。
影响

氢键的影响包括:
- 与同族的化合物相比,NH3、H2O和HF具有反常高的熔点和沸点。
- 氨在水中的非常大的溶解度与它和水分子间的氢键有关。
- 甘油、无水磷酸和硫酸具有较大的黏度。
- 邻硝基苯酚中存在分子内氢键,因此熔点较间硝基苯酚和对硝基苯酚低。
- 冰中水分子在冰晶体结构中空间占有率较低,因而冰密度较小,甚至小于水。
- 分子内形成氢键常使酸性增强。如苯甲酸的pKa=11.02,而邻羟基苯甲酸的pKa=11,2,6-二羟基苯甲酸可在分子内形成两个氢键,它的pKa=8.3。其原因是分子内氢键的形成,促进了氢的解离。
- 结晶水合物中存在由氢键构建的类冰骨架,其中可装入小分子或离子。参见甲烷气水包合物。
- C=O…H-N氢键使蛋白质形成α螺旋。
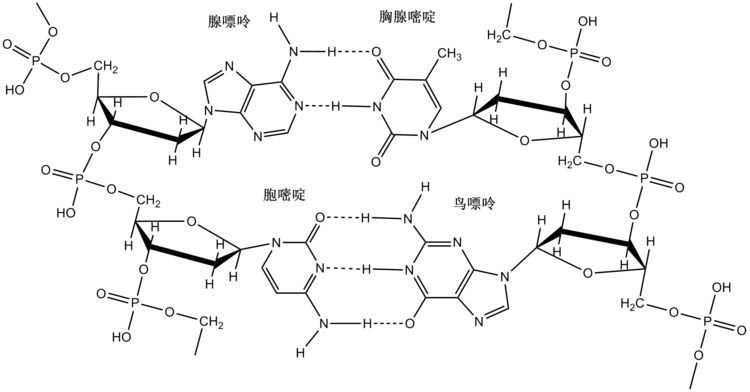
- DNA(去氧核糖核酸)中两条链的碱基通过氢键配对,而氢键的饱和性和方向性使得双螺旋的碱基配对具有专一性,即A-T靠2个氢键配对而C-G靠3个氢键配对,如下图:
参见
参考资料
外部链接
This article uses material from the Wikipedia 中文 article 氢键, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). 除非另有声明,本网站内容采用CC BY-SA 4.0授权。 Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki 中文 (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.