Cobaltii-Thiocyanat: Chemische Verbindung
Cobalt(II)-thiocyanat ist eine anorganische chemische Verbindung des Cobalts aus der Gruppe der Thiocyanate.
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
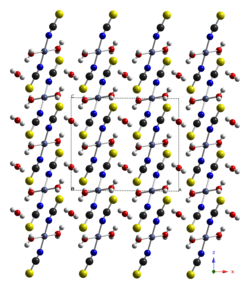 | ||||||||||
| _ Co _ S _ C _ N | ||||||||||
| Allgemeines | ||||||||||
| Name | Cobalt(II)-thiocyanat | |||||||||
| Andere Namen |
| |||||||||
| Verhältnisformel | Co(SCN)2 | |||||||||
| Kurzbeschreibung | gelb-brauner Feststoff | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 175,10 g·mol−1 | |||||||||
| Aggregatzustand | fest | |||||||||
| Dichte | 1,786 g·cm−3 (Trihydrat) | |||||||||
| Löslichkeit |
| |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Cobalt(II)-thiocyanat kann durch Reaktion von Cobalt(II)-sulfat mit Bariumthiocyanat gewonnen werden.
Ebenfalls möglich ist die Darstellung durch Reaktion von Thiocyansäure mit Cobalt(II)-carbonat oder durch Reaktion von Ammoniumthiocyanat und Cobaltsalzen in neutraler Lösung.
Eigenschaften

Cobalt(II)-thiocyanat ist ein gelb-brauner Feststoff, der in Wasser löslich ist. Die Lösung hat eine rötliche Farbe. Das Trihydrat hat eine violette bis braune Farbe, das im Durchlicht rot aussieht und sich in Wasser unter Blaufärbung löst. Es wandelt sich ab 105 °C in das Anhydrat um. Das Trihydrat besitzt eine monokline Kristallstruktur mit der Raumgruppe C2/c (Raumgruppen-Nr. 15).
Verwendung
Cobalt(II)-thiocyanat kann zum Nachweis von Alkaloiden, Methadon, Ephedrin, Cocain und anderen Drogen verwendet werden. Wenn diese zu einer 2-prozentigen Lösung von Cobalt(II)-thiocyanat zugegeben werden, so bildet sich je nach Verbindung ein blauer oder blau-grüner Niederschlag. Dies wird (mit Zugabe von Chloroform) als Scott-Test bezeichnet. Das Trihydrat wird als Luftfeuchtigkeitsindikator verwendet. Eine wässrige Lösung der Verbindung kann zur Bestimmung von nichtionischen Tensiden auf Basis von Ethoxylaten in Wasser verwendet werden.
Einzelnachweise
This article uses material from the Wikipedia Deutsch article Cobalt(II)-thiocyanat, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Abrufstatistik · Autoren Der Inhalt ist verfügbar unter CC BY-SA 4.0, sofern nicht anders angegeben. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Deutsch (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.


