Реакція Дільса — Альдера
Реа́кція Ді́льса — А́льдера — реакція циклоприєднання між спряженим дієном та заміщеним алкеном (що також називається дієнофілом) що призводить до утворення заміщених циклогексенів.
Реакція проходить також у тому випадку, коли деякі атоми в новоутвореному циклі не є атомами вуглецю. У деяких випадках реакція Дільса — Альдера може протікати у зворотному напрямку і називається реакцією ретро-Дільса — Альдера. Отто Дільс та Курт Альдер вперше повідомили про цю реакцію у 1928 році, за що у 1950 році були нагороджені Нобелівською премією з хімії.

Механізм реакції
Реакція Дільса — Альдера належить до так званих перициклічних реакцій. Перициклічні реакції, в результаті яких утворюються циклічні сполуки, називаються реакціями циклоприєднання. Існує багато різновидів реакцій циклоприєднання, одним з найпоширеніших є [4+2]-циклоприєднання, де ключовим етапом є узгоджена взаємодія 4π-електронів дієну і 2π-електронів дієнофілу, що знаходяться на вищій зайнятій (HOMO) і нижній вільній (LUMO) молекулфрних орбіталях сполук. Ця реакція проходить порівняно легко, зважаючи на те, що перехідний стан містить шестичленну π-електронну ароматичну структуру, котра знижує енергію активації.

Дієн
Дієновий компонент реакції Дільса — Альдера може бути як відкритим ланцюгом, так і циклічним та містити різноманітні замісники.. Проте існує обмеження: дієн повинен існувати в s-цис конформації. Циклічні дієни, котрі постійно перебувають у s-цис конформації, є винятково активними в даній реакції (наприклад, циклопентадієн), у той час як циклічні дієни, котрі можуть перебувати лише в s-транс конформації, в реакцію Дільса — Альдера взагалі не вступають. Особливо реакційноздатним є дієн Данішефського (1-метокси-3-триметилсилілокси-1,3-бутадієн) та схожі дієни з замісниками при C1 та C3. Їх підвищена реакційна здатність обумовлена підняттям енергії HOMO орбіталі (найвищої зайнятої молекулярної орбіталі) дієну.

Надзвичайно високореакційними є також є нестабільні дієни, які можна отримати тільки як проміжні сполуки (in situ) і які стабілізуются через утворення аромаичного кільця при циклоприєднанні.

Бензеноїдні сполуки рідко піддаються реакції Дільса — Альдера і часто вимагають дуже активних дієнофілів. Одним з прикладів такої рідкісної реакції є реакція Ваґнера-Яуреґґа.
Дієнофіл
Як правило, у реакції Дільса — Альдера дієнофіл має електроноакцепторну групу, спряжену із алкеном. Проте активніші дієнофіли повинні бути сильніше спряжені, як мінімум з фенільною групою або з атомом хлору. Дієнофіл може бути активований також кислотою Льюїса, наприклад пентахлоридом ніобію.

Регіоселективність
Див. Регіоселективність
Реакція Дільса — Альдера між несиметричними сполуками може приводити до двох різних продуктів. При різній електронодонорності замісників відбувається розподіл зарядів у молекулах дієну та дієнофілу, що впливає на відносну кількість двох можливих продуктів.

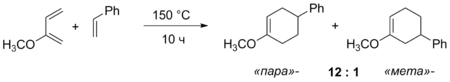
Стереоселективність
Див. також Стереоселективність
Оскільки реакція Дільса — Альдера це узгоджений проецес перерозподілу електронної густини через циклічний перехідний стан, то конфігурація продукту визначається конфігурацією реагентів. Так, з(Z)-алкенів утворюються цис-продукти, а з (E)-алкенів — транс-продукти. Аналогічним чином можна визначити і орієнтацію замісників дієну в продукті циклоприєднанняи:
 | 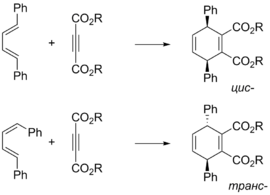 |
Джерела
- Глосарій термінів з хімії / уклад. Й. Опейда, О. Швайка ; Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Дон. : Вебер, 2008. — 738 с. — ISBN 978-966-335-206-0.
Примітки
This article uses material from the Wikipedia Українська article Реакція Дільса — Альдера, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Вміст доступний на умовах CC BY-SA 4.0, якщо не вказано інше. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Українська (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.