พันธุวิศวกรรม
พันธุวิศวกรรม หรือ วิศวกรรมพันธุศาสตร์ (อังกฤษ: Genetic engineering) หรือที่เรียกว่า การดัดแปลงพันธุกรรม (อังกฤษ: genetic modification) คือการยักย้ายถ่ายเทโดยตรงของจีโนมของสิ่งมีชีวิตโดยใช้เทคโนโลยีชีวภาพ ดีเอ็นเอใหม่อาจถูกแทรกอยู่ในจีโนมของเจ้าภาพโดยตอนแรกต้องแยกและคัดลอกสารพันธุกรรมที่น่าสนใจโดยใช้วิธีการโคลนนิงโมเลกุลเพื่อสร้างลำดับดีเอ็นเอขึ้นมาอันหนึ่ง หรือโดยการสังเคราะห์ดีเอ็นเอ จากนั้นก็แทรกโครงสร้างนี้เข้าไปในสิ่งมีชีวิตของเจ้าภาพ หลายยีนอาจถูกลบออกหรือ เคาะออกมา (อังกฤษ: knockout) โดยใช้ nuclease การกำหนดเป้าหมายยีน (อังกฤษ: Gene targeting) เป็นเทคนิคที่แตกต่างอันหนึ่งที่ใช้วิธีการรวมตัวแบบคล้ายคลึง (อังกฤษ: homologous recombination) เพื่อเปลี่ยนแปลงยีนภายใน, และสามารถนำมาใช้ในการลบยีน, รื้อถอน exons, เพิ่มยีน, หรือการใส่การกลายพันธุ์แบบจุด (อังกฤษ: point mutation).
สิ่งมีชีวิตที่ถูกสร้างขึ้นผ่านทางพันธุวิศวกรรมจะถือว่าเป็นสิ่งมีชีวิตดัดแปลงพันธุกรรม (จีเอ็มโอ) GMOs แรกเป็นเชื้อแบคทีเรียในปี 1973 และหนูจีเอ็มถูกสร้างขึ้นในปี 1974. แบคทีเรียที่ผลิตโดยอินซูลินอยู่ในการพาณิชย์ในปี 1982 และอาหารดัดแปลงพันธุกรรมได้มีการจำหน่ายตั้งแต่ปี 1994. Glofish, จีเอ็มโอแรกที่ออกแบบมาเป็นสัตว์เลี้ยง, ออกจำหน่ายครั้งแรกในประเทศสหรัฐอเมริกาในเดือนธันวาคมปี 2003
เทคนิคพันธุวิศวกรรมมีการนำไปใช้ในหลายสาขารวมถึงการวิจัย, การเกษตร, อุตสาหกรรมเทคโนโลยีชีวภาพ, และการแพทย์. เอนไซม์ที่ใช้ในน้ำยาซักผ้าและยารักษาโรคเช่นอินซูลินและฮอร์โมนการเจริญเติบโตของมนุษย์มีการผลิตในขณะนี้ในเซลล์ GM, สายการทดลองเซลล์จีเอ็มและสัตว์จีเอ็มเช่นหนูหรือ zebrafish กำลังถูกใช้เพื่อการวิจัย, และพืชดัดแปลงพันธุกรรมได้อยู่ในการพาณิชย์.
ปรับเปลี่ยนสิ่งมีชีวิตที่เฉพาะเจาะจงสำหรับวัตถุประสงค์เพื่อเปลี่ยนแปลงลักษณะของมัน.
หมายเหตุ: ดัดแปลงมาจาก ref..ความหมาย
พันธุวิศวกรรมทำการเปลี่ยนแปลงส่วนประกอบทางพันธุกรรมของสิ่งมีชีวิตโดยใช้เทคนิคที่ถอดทิ้งวัสดุที่ถ่ายทอดได้หรือที่ใช้ดีเอ็นเอที่เตรียมด้านนอกสิ่งมีชีวิตโดยตรงเข้าสู่เจ้าภาพหรือเข้าสู่เซลล์ที่จากนั้นจะถูกหลอมละลายหรือถูกไฮบริดกับเจ้าภาพ, ซึ่งเกี่ยวข้องกับการใช้เทคนิคกรดนิวคลีอิก recombinant (DNA หรือ RNA) เพื่อสร้างรูปแบบผสมใหม่ของวัสดุพันธุกรรมที่ถ่ายทอดได้ตามมาด้วยการรวมตัวกันของวัสดุนั้นทั้งทางอ้อมผ่านระบบโมเลกุลเวกเตอร์หรือโดยตรงผ่านเทคนิคการฉีดแบบไมโคร (อังกฤษ: micro-injection), การฉีดแบบแมคโครและการห่อหุ้มแบบไมโคร (อังกฤษ: micro-encapsulation).
พันธุวิศวกรรมตามปกติไม่ได้รวมถึงการเพาะพันธ์สัตว์และการเพาะพันธ์พืชแบบดั้งเดิม, การปฏิสนธินอกร่างกาย (อังกฤษ: In vitro fertilisation), การเหนี่ยวนำของเซลล์ที่มีโครโมโซมเหมือนกันมากกว่าสองคู่ (อังกฤษ: polyploidy), การกลายพันธุ์และเทคนิคการละลายของเซลล์ที่ไม่ใช้กรดนิวคลีอิก recombinant หรือสิ่งมีชีวิตดัดแปลงพันธุกรรมในกระบวนการ. อย่างไรก็ตามคณะกรรมาธิการยุโรปยังกำหนดพันธุวิศวกรรมในวงกว้างที่รวมทั้งการคัดเลือกพันธุ์และวิธีการอื่นๆของการเลือกประดิษฐ์. การโคลนิงและการวิจัยเซลล์ต้นกำเนิด, แม้ว่าจะไม่ได้รับการพิจารณาว่าเป็นพันธุวิศวกรรม, ถูกนำไปสัมพันธ์กันอย่างใกล้ชิดและพันธุวิศวกรรมสามารถนำมาใช้ภายในพวกมัน. ชีววิทยาสังเคราะห์ (อังกฤษ: Synthetic biology) เป็นสาขาวินัยที่เกิดขึ้นใหม่ที่ใช้พันธุวิศวกรรมอีกขั้นหนึ่งไกลกว่าเดิมโดยการใช้สารพันธุกรรมสังเคราะห์เทียมจากวัตถุดิบให้เป็นสิ่งมีชีวิต.
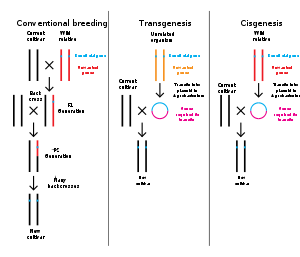
หากสารพันธุกรรมจากสายพันธุ์อื่นถูกเพิ่มลงในเจ้าภาพ, มีชีวิตที่เกิดขึ้นจะถูกเรียกว่าพันธุกรรมดัดแปร (อังกฤษ: transgenic). หากสารพันธุกรรมจากสายพันธุ์เดียวกันหรือสายพันธุ์ที่สามารถผสมพันธุ์ตามธรรมชาติกับเจ้าภาพถูกใช้, สิ่งมีชีวิตที่เกิดขึ้นจะถูกเรียกว่า cisgenic. พันธุวิศวกรรมนอกจากนี้ยังสามารถใช้ในการรื้อถอนสารพันธุกรรมจากสิ่งมีชีวิตเป้าหมายอีกด้วย, ในการสร้างสิ่งมีชีวิตที่ยีนถูกน็อคเอาท์. ในยุโรปการดัดแปลงพันธุกรรมเป็นคำพ้องกับพันธุวิศวกรรมในขณะที่ภายในสหรัฐอเมริกา มันยังสามารถหมายถึงวิธีการเพาะพันธุ์ธรรมดา. ระบบการกำกับดูแลของแคนาดาจะขึ้นอยู่กับว่าผลิตภัณฑ์มีคำอธิบายโดยไม่คำนึงถึงวิธีการ ต้นกำเนิดหรือไม่. พูดอีกอย่าง, ผลิตภัณฑ์จะได้รับการกำกับดูแลแบบดัดแปลงพันธุกรรมถ้าจะประกอบด้วยลักษณะบางอย่างที่ไม่พบก่อนหน้านี้ในสายพันธุ์ไม่ว่ามันจะถูกสร้างขึ้นโดยใช้วิธีการปรับปรุงพันธุ์แบบดั้งเดิมหรือไม่ (เช่นการคัดเลือกพันธุ์, การละลายเซลล์, การเพาะพันธุ์แบบกลายพันธุ์) หรือพันธุวิศวกรรม. ในชุมชนวิทยาศาสตร์, คำว่า "พันธุวิศวกรรม" ไม่ได้ถูกใช้กันทั่วไป; คำที่เฉพาะเจาะจงมากกว่าเช่น transgenic จะถูกใช้มากกว่า.
สิ่งมีชีวิตดัดแปลงพันธุกรรม
บทความหลัก: Genetically modified organism
พืช, สัตว์หรือสิ่งมีชีวิตขนาดเล็กที่มีการเปลี่ยนแปลงผ่านทางพันธุวิศวกรรมเรียกว่าสิ่งมีชีวิตดัดแปลงพันธุกรรมหรือจีเอ็มโอ. แบคทีเรียเป็นสิ่งมีชีวิตแรกที่ได้รับการดัดแปลงทางพันธุกรรม. ดีเอ็นเอแบบ Plasmid ที่ประกอบด้วยยีนใหม่ที่สามารถถูกแทรกเข้าไปในเซลล์ของแบคทีเรีย จากนั้นเชื้อแบคทีเรียก็จะแสดงยีนเหล่านั้นออกมา. ยีนเหล่านี้สามารถเป็นรหัสสำหรับยาหรือเอนไซม์ที่ปรุงอาหารและพื้นผิวทางชีวะอื่นๆ. พืชหลายชนิดได้รับการดัดแปลงเพื่อใช้ป้องกันแมลง, ต้านทานสารกำจัดวัชพืช, ต้านทานไวรัส, เพิ่มโภชนาการ, อดทนต่อแรงกดดันด้านสิ่งแวดล้อมและผลิตวัคซีนที่กินได้. จีเอ็มโอในเชิงพาณิชย์ส่วนใหญ่จะต้านแมลงและ/หรืออดทนต่อสารกำจัดวัชพืช. สัตว์ดัดแปลงพันธุกรรมได้ถูกนำมาใช้สำหรับการวิจัย, จำลองแบบสัตว์และการผลิตสินค้าเกษตรหรือยา. พวกมันรวมถึงสัตว์ที่มียีนที่ถูกเคาะออก, ถูกเพิ่มความไวต่อการเกิดโรค, มีฮอร์โมนสำหรับการเจริญเติบโตให้เกินและมีความสามารถในการแสดงโปรตีนในนมของพวกมัน.
ประวัติ
บทความหลัก: ประวัติของพันธุวิศวกรรม
มนุษย์ได้ทำการเปลี่ยนแปลงจีโนมของสายพันธุ์เป็นเวลาหลายพันปีมาแล้วโดยการคัดเลือกเทียม (อังกฤษ: artificial selection) และเมื่อเร็วๆนี้เป็นพันธุกรรมกลายพันธ์ (อังกฤษ: mutagenesis). พันธุวิศวกรรมแบบการยักย้ายถ่ายเทดีเอ็นเอโดยตรงโดยมนุษย์นอกเหนือจากการเพาะพันธุ์และการกลายพันธุ์เพิ่งมีมาตั้งแต่ปี 1970s เท่านั้น. คำว่า "พันธุวิศวกรรม" ถูกตั้งขึ้นเป็นครั้งแรกโดยแจ็ค วิลเลียมสันในนิยายวิทยาศาสตร์เรื่อง "เกาะมังกร" ตีพิมพ์ในปี 1951, หนึ่งปีก่อนที่บทบาทของดีเอ็นเอในการถ่ายทอดทางพันธุกรรมได้รับการยืนยันโดยอัลเฟรด เฮอร์ชีย์และมาร์ธา เชส, และสองปีก่อนที่ เจมส์ วัตสันและฟรานซิส คริกแสดงว่าโมเลกุลของดีเอ็นเอมีโครงสร้างเป็นเกลียวคู่.

ในปี 1972 พอล Berg ได้สร้างโมเลกุลดีเอ็นเอ recombinant ขึ้นครั้งแรกโดยการรวมดีเอ็นเอจาก SV40 ไวรัสของลิงกับดีเอ็นเอของไวรัสแลมบ์ดา. ในปี 1973 เฮอร์เบิร์ท บอยเยอร์และสแตนลีย์ โคเฮนที่สร้างสิ่งมีชีวิตดัดแปรพันธุกรรมครั้งแรกโดยการแทรกยีนต้านทานยาปฏิชีวนะเข้าไปในพลาสมิดของแบคทีเรีย E. coli. หนึ่งปีต่อมารูดอล์ฟ Jaenisch สร้างหนูดัดแปรพันธุกรรมโดยการใส่ดีเอ็นเอต่างถิ่นเขัไปในตัวอ่อนของมัน, ทำให้มันเป็นสัตว์ดัดแปลงพันธุกรรมตัวแรกของโลก. ความสำเร็จเหล่านี้นำไปสู่ความกังวลในชุมชนวิทยาศาสตร์เกี่ยวกับศักยภาพของความเสี่ยงจากพันธุวิศวกรรม, ซึ่งได้รับการกล่าวถึงเป็นครั้งแรกในเชิงลึกที่'การประชุม Asilomar' ในปี 1975. หนึ่งในข้อเสนอแนะหลักจากการประชุมครั้งนี้คือการกำกับดูแลของรัฐบาลของการวิจัยดีเอ็นเอ recombinant ควรได้รับการจัดตั้งขึ้นจนกว่าเทคโนโลยีจะถือว่าปลอดภัย.
ในปี 1976 Genentech, บริษัทพันธุวิศวกรรมแห่งแรก, ก่อตั้งโดยเฮอร์เบิร์ท บอยเยอร์และโรเบิร์ต สเวนสันและหนึ่งปีต่อมาบริษัทนี้ได้ผลิตโปรตีนของมนุษย์ (somatostatin) ใน "E.coli". Genentech ประกาศการผลิตอินซูลินของมนุษย์ดัดแปลงพันธุกรรมในปี 1978. ในปี 1980 ศาลฎีกาสหรัฐในคดีระหว่าง Diamond กับ Chakrabarty ได้ตัดสินว่าชีวิตที่ถูกเปลี่ยนแปลงทางพันธุกรรมสามารถจดสิทธิบัตรได้. อินซูลินที่ผลิตโดยแบคทีเรีย, ตรา humulin, ได้รับการอนุมัติให้เผยแพร่จากคณะกรรมการอาหารและยาในปี 1982.
ในปี 1970s นักศึกษาระดับบัณฑิตศึกษา สตีเว่น Lindow แห่งมหาวิทยาลัยวิสคอนซิน-แมดิสันกับ D.C. Arny และ C Upper พบแบคทีเรียที่เขาระบุว่าเป็น "P. syringae" ที่มีบทบาทในนิวเคลียสน้ำแข็ง และในปี 1977, เขาค้นพบสายพันธุ์น้ำแข็ง-ลบ (อังกฤษ: Ice-minus bacteria) ที่กลายพันธุ์. หลังจากนั้นเขาก็ประสบความสำเร็จในการสร้างสายพันธุ์น้ำแข็ง-ลบ recombinant. ในปี 1983, บริษัทเทคโนโลยีชีวภาพ Advanced Genetic Sciences (AGS) ยื่นขอรับการอนุมัติจากรัฐบาลสหรัฐเพื่อดำเนินการทดสอบภาคสนามกับสายพันธ์น้ำแข็ง-ลบของ "P. syringae" เพื่อปกป้องพืชจากน้ำค้างแข็ง, แต่กลุ่มสิ่งแวดล้อมและผู้ประท้วงถ่วงเวลาการทดสอบภาคสนามออกไปเป็นเวลาสี่ปีกับความท้าทายทางกฎหมาย. ในปี 1987 สายพันธุ์น้ำแข็งลบ-ของ "P. syringae" กลายเป็นสิ่งมีชีวิตดัดแปลงพันธุกรรม (จีเอ็มโอ)อันแรกที่จะถูกปล่อยออกสู่สิ่งแวดล้อม เมื่อไร่สตรอเบอร์รี่และไร่มันฝรั่งในรัฐแคลิฟอร์เนียถูกพ่นด้วยมัน. ทั้งสองสนามทดสอบถูกโจมตีโดยกลุ่มนักกิจกรรมในคืนก่อนการทดสอบจะเกิดขึ้น. "สถานที่ทดสอบแห่งแรกของโลกได้ดึงดูดสนามขยะแห่งแรกของโลก".
การทดลองภาคสนามครั้งแรกของพืชดัดแปลงพันธุกรรมเกิดขึ้นในฝรั่งเศสและสหรัฐอเมริกาในปี 1986, ต้นยาสูบถูกดัดแปลงให้ทนต่อสารเคมีกำจัดวัชพืช. สาธารณรัฐประชาชนจีนเป็นประเทศแรกที่จะทำการตลาดพืชดัดแปรพันธุกรรม, โดยการนำเสนอยาสูบทนไวรัสในปี 1992. ในปี 1994 Calgene ได้รับการอนุมัติให้จำหน่ายมะเขือเทศ Flavr Savr ในเชิงพาณิชย์, มะเขือเทศที่ถูกดัดแปลงมาเพื่อมีชีวิตในชั้นเก็บยาวขึ้น. ในปี 1994 สหภาพยุโรปได้อนุมัติยาสูบออกแบบที่ถูกดัดแปลงให้ทนต่อสารกำจัดวัชพืช bromoxynil, ทำให้มันเป็นพืชดัดแปลงพันธุกรรมแรกที่จำหน่ายในเชิงพาณิชย์ในยุโรป. ในปี 1995 Bt Potato ได้รับการอนุมัติความปลอดภัยโดยหน่วยงานคุ้มครองสิ่งแวดล้อม, หลังจากที่ได้รับการรับรองจากองค์การอาหารและยา, ทำให้มันเป็นพืชที่ผลิตยาฆ่าแมลงตัวแรกที่ได้รับการอนุมัติในประเทศสหรัฐอเมริกา. ในปี 2009 พืชดัดแปรพันธุกรรม 11 ตัวได้ปลูกในเชิงพาณิชย์ใน 25 ประเทศ, ที่ใหญ่ที่สุดโดยพื้นที่ที่ปลูกเป็นสหรัฐอเมริกา, บราซิล, อาร์เจนตินา, อินเดีย, แคนาดา, จีน, ปารากวัยและแอฟริกาใต้.
ในช่วงปลายปี 1980s และต้นปี 1990s, คำแนะนำเกี่ยวกับการประเมินความปลอดภัยของพืชดัดแปลงพันธุกรรมและอาหารได้เกิดขึ้นจากองค์กรรวมทั้ง FAO และ WHO.
ในปี 2010 นักวิทยาศาสตร์ที่สถาบัน J. Craig Venter ประกาศว่าพวกเขาได้สร้างจีโนมแบคทีเรียสังเคราะห์ตัวแรก. นักวิจัยได้เพิ่มจีโนมใหม่ให้กับเซลล์แบคทีเรียและเลือกเซลล์ที่มีจีโนมใหม่. เพื่อทำเช่นนี้เซลล์จะผ่านกระบวนการที่เรียกว่า resolution, นั้นคือในระหว่างการแบ่งตัวของเซลล์แบคทีเรีย เซลล์ใหม่หนึ่งตัวจะได้รับจีโนมดีเอ็นเอเดิมของแบคทีเรีย, ในขณะที่ตัวอื่นๆได้รับจีโนมสังเคราะห์ใหม่. เมื่อเซลล์นี้แบ่งตัว มันจะใช้จีโนมสังเคราะห์เป็นแม่แบบของมัน. แบคทีเรียที่ได้จากการพัฒนาของนักวิจัย, ชื่อ Synthia, เป็นรูปแบบชีวิตสังเคราะห์ตัวแรกของโลก.
กระบวนการ
บทความหลัก: เทคนิคทางพันธุวิศวกรรม
ขั้นตอนแรกคือการเลือกและแยกยีนที่จะแทรกเข้าไปในสิ่งมีชีวิตดัดแปลงพันธุกรรม. ณ ปี 2012, ในพืชจีเอ็มเชิงพาณิชย์ส่วนใหญ่มียีนที่โอนเข้ามาในตัวมันที่ให้การป้องกันแมลงหรือทนทานต่อสารเคมีกำจัดวัชพืช. ยีนสามารถแยกได้โดยการใช้เอนไซม์ข้อจำกัด (อังกฤษ: restriction enzymes) เพื่อตัดดีเอ็นเอให้เป็นเศษๆและใช้วิธี gel electrophoresis เพื่อแยกพวกมันออกตามความยาว. ปฏิกิริยาลูกโซ่โพลิเมอร์ (PCR) ยังสามารถเพื่อขยายขึ้นส่วนของยีน, ซึ่งจากนั้นจะสามารถแยกได้ผ่านวิธีการ gel electrophoresis. ถ้ายีนที่ถูกเลือกหรือจีโนมของสิ่งมีชีวิตผู้บริจาคได้มีการศึกษามาดี, มันก็อาจจะปรากฏในห้องสมุดทางพันธุกรรม. ถ้ารู้ลำดับดีเอ็นเอ, แต่ไม่มีสำเนาของยีน, มันก็สามารถถูกสังเคราะห์แบบเทียมได้.
ยีนที่จะแทรกเข้าไปในสิ่งมีชีวิตดัดแปลงพันธุกรรมจะต้องรวมเข้ากับองค์ประกอบทางพันธุกรรมอื่นๆเพื่อให้มันทำงานอย่างถูกต้อง. ยีนยังสามารถได้รับการดัดแปลงในขั้นตอนนี้เพื่อให้มันการแสดงออกหรือมีประสิทธิภาพที่ดีกว่าอีกด้วย. เช่นเดียวกับยีนที่จะแทรกเข้าไป, โครงสร้างดีเอ็นเอส่วนใหญ่จะประกอบด้วยผู้ก่อการ(ทางชีวภาพ) (อังกฤษ: (biology) promoter) และภูมิภาคที่เป็นตัวปิดท้ายทางพันธุกรรม (อังกฤษ: (genetics) terminator region) เช่นเดียวกับยีนเครื่องหมายที่เลือกได้ (อังกฤษ: selectable marker gene). ภูมิภาคผู้ก่อการจะเริ่มต้นการถอดรหัสของยีนและสามารถนำมาใช้ในการควบคุมสถานที่และระดับของการแสดงออกของยีน, ในขณะที่ภูมิภาคตัวปิดท้ายสิ้นสุดการถอดความ. เครื่องหมายที่เลือกได้, ซึ่งในกรณีส่วนใหญ่ประศาสน์ความต้านทานยาปฏิชีวนะให้กับสิ่งมีชีวิตที่มันแสดงออก, จำเป็นที่จะต้องตรวจสอบว่าเซลล์ตวไหนจะถูกแปลงกับยีนใหม่. โครงสร้างจะถูกทขึ้นำโดยใช้เทคนิคดีเอ็นเอ recombinant, เช่นข้อจำกัดน้ำย่อย (อังกฤษ: restriction digest), การผูก (อังกฤษ: ligations) และการโคลนโมเลกุล. การยักย้ายถ่ายเทของดีเอ็นเอมักเกิดขึ้นภายในพลาสมิด.
รูปแบบที่พบมากที่สุดของพันธุวิศวกรรมเกี่ยวข้องกับการแทรกสารพันธุกรรมใหม่แบบสุ่มภายในจีโนมเจ้าภาพ[ต้องการอ้างอิง]. เทคนิคอื่นๆจะยอมให้สารพันธุกรรมใหม่ที่จะถูกแทรกในสถานที่เฉพาะในจีโนมเจ้าภาพหรือสร้างการกลายพันธุ์ที่ loci จีโนมที่สามารถเคาะยีนที่เกิดขึ้นภายในสิ่งมีชีวิต (อังกฤษ: endogenous genes) ออก. เทคนิคของ gene targeting จะใช้ homologous recombination เพื่อกำหนดเป้าหมายที่ต้องการที่จะเปลี่ยนแปลง endogenous genes ที่เฉพาะเจาะจง. สิ่งนี้มีแนวโน้มที่จะเกิดขึ้นที่ความถี่ที่ค่อนข้างต่ำในพืชและสัตว์และโดยทั่วไปต้องใช้ selectable markers. ความถี่ของ gene targeting สามารถเพิ่มขึ้นอย่างมากด้วยการใช้ nucleases ดัดแปลงเช่น zinc finger nucleases, homing endonucleases ที่ถูกดัดแปลง, หรือ nucleases ที่สร้างจาก TAL effectors. นอกจากการเสริมสร้าง gene targeting, nucleases ที่ถูกดัดแปลงยังสามารถถูกใช้ในการแนะนำการกลายพันธุ์ใน endogenous genes ที่สร้าง gene knockout.
การแปลง
บทความหลัก: การแปลง (พันธุศาสตร์)

ประมาณ 10% เท่านั้นของแบคทีเรียที่โดยธรรมชาติมีความสามารถดูดกลืนดีเอ็นเอต่างถิ่น. อย่างไรก็ตาม, ความสามารถนี้สามารถถูกเหนี่ยวนำให้เกิดในเชื้อแบคทีเรียอื่นผ่านความเครียด (เช่นช็อกด้วยความร้อนหรือไฟฟ้า), จึงเป็นการเพิ่มความสามารถในการซึมผ่านของเยื่อหุ้มเซลล์ให้กับดีเอ็นเอ, ดีเอ็นเอที่ถูกดูดกลืนสามารถรวมเข้ากับจีโนมหรือมีอยู่เป็นดีเอ็นเอแบบหลายโครโมโซม (อังกฤษ: extrachromosomal DNA). ดีเอ็นเอถูกแทรกโดยทั่วไปเข้าสู่เซลล์สัตว์โดยใช้ microinjection, ที่มันสามารถถูกฉีดผ่านเปลือกนิวเคลียร์ของเซลล์โดยตรงเข้าสู่นิวเคลียสหรือผ่านการใช้ viral vectors. ในพืช, ดีเอ็นเอถูกแทรกโดยทั่วไปโดยใช้การรวมแบบพึ่งพาแบคทีเรียเกษตร (อังกฤษ: Agrobacterium-mediated recombination) หรือ biolistics(การฉีดเซลล์ด้วย gene gun).
ในการรวมแบบพึ่งพาแบคทีเรียเกษตร, โครงสร้างพลาสมิดจะประกอบด้วย Transfer DNA (T-DNA), ดีเอ็นเอซึ่งเป็นผู้รับผิดชอบสำหรับการแทรกของดีเอ็นเอเข้าสู่จีโนมพืชเจ้าภาพ. พลาสมิดนี้จะถูกแปลงให้เป็น "Agrobacterium" ที่ไม่มีพลาสมิดก่อนที่จะติดเชื้อเซลล์พืช. Agrobacterium จากนั้นโดยธรรมชาติจะแทรกสารพันธุกรรมเข้าไปในเซลล์พืช. ในการแปลงแบบ biolistics, อนุภาคของทองหรือทังสเตนจะถูกเคลือบด้วยดีเอ็นเอจากนั้นจะถูกยิงเข้าไปในเซลล์พืชอ่อนหรือตัวอ่อนของพืช. บางสารพันธุกรรมจะเข้าสู่เซลล์และแปลงพวกมัน. วิธีการนี้สามารถนำมาใช้กับพืชที่ไม่ไวต่อการติดเชื้อ Agrobacterium และยังช่วยในการแปลงของ plastids พืช. วิธีการอีกวิธีหนึ่งสำหรับเซลล์พืชและสัตว์คือ Electroporation. Electroporation เกี่ยวข้องการช๊อคด้วยไฟฟ้ากับเซลล์พืชหรือสัตว์, ซึ่งสามารถทำให้เยื่อหุ้มเซลล์สามารถดูดซึมเข้าไปในพลาสมิดดีเอ็นเอ. ในบางกรณีเซลล์ที่ถูก electroporated จะรวมดีเอ็นเอเข้าไปในจีโนมของพวกมัน. เนื่องจากความเสียหายที่เกิดจากเซลล์และดีเอ็นเอ, ประสิทธิภาพการแปลงของ biolistics และ electroporation จะต่ำกว่าการแปลงแบบ agrobacterial mediated และ แบบ microinjection.
เนื่องจากบ่อยๆที่เพียงเซลล์เดียวเท่านั้นจะถูกแปลงด้วยสารพันธุกรรม, สิ่งมีชีวิตจะต้องถูกสร้างขึ้นใหม่จากเซลล์เดียวอันนั้น. เมื่อแบคทีเรียประกอบด้วยเซลล์เดียวและถูกผลิตใหม่ (อังกฤษ: reproduce) แบบโคลนิง, การสร้างขึ้นใหม่ (อังกฤษ: regeneration) จึงไม่จำเป็น. ในพืช สิ่งนี้สามารถทำได้โดยการใช้การเพาะเลี้ยงเนื้อเยื่อ. พืชแต่ละสปีซีส์จะมีความต้องการที่แตกต่างกันสำหรับการ regeneration ที่ประสบความสำเร็จผ่านการเพาะเลี้ยงเนื้อเยื่อ. หากประสบความสำเร็จ, พืชผู้ใหญ่จะผลิตสิ่งที่ประกอบด้วยสิ่งดัดแปรพันธุกรรมในทุกๆเซลล์. ในสัตว์, มันมีความจำเป็นเพื่อให้แน่ใจว่าดีเอ็นเอที่ถูกแทรกจะปรากฏในเซลล์ต้นกำเนิดตัวอ่อน (อังกฤษ: embryonic stem cells). Selectable markers จะถูกใช้เพื่อง่ายต่อการแยกความแตกต่างของเซลล์ที่แปลงกับเซลล์ที่ไม่ถูกแปลง. markers เหล่านี้มักจะปรากฏในสิ่งมีชีวิตดัดแปรพันธุกรรม, แม้ว่าหลายกลยุทธ์ได้รับการพัฒนาที่สามารถลบ selectable marker ออกจากพืชดัดแปรพันธุกรรมผู้ใหญ่. เมื่อลูกหลานถูกผลิต, พวกมันสามารถได้รับการคัดเลือกเพื่อหาการปรากฏตัวของยีน. ลูกหลานทั้งหมดจากรุ่นแรกจะเป็น heterozygous สำหรับยีนที่ถูกแทรกและจะต้องผสมพันธ์กันเพื่อผลิตสัตว์ homozygous.
การทดสอบเพิ่มเติมใช้วิธี polymerase chain reaction (PCR), Southern hybridization, และ DNA sequencing จะถูกดำเนินการเพื่อยืนยันว่าสิ่งมีชีวิตมียีนใหม่. การทดสอบเหล่านี้ยังสามารถยืนยันสถานที่ตั้งของโครโมโซมและคัดลอกหมายเลขของยีนที่ถูกแทรกอีกด้วย. การปรากฏตัวของยีนไม่ได้รับประกันว่ามันจะมีการแสดงออกในระดับที่เหมาะสมหรือไม่ในเนื้อเยื่อเป้าหมายดังนั้นวิธีการที่จะมองหาและวัดผลิตภัณฑ์ยีน (อาร์เอ็นเอและโปรตีน) ยังมีการใช้อีกด้วย. เหล่านี้รวมถึง northern hybridization, quantitative RT-PCR, Western blot, immunofluorescence, ELISA และการวิเคราะห์แบบ phenotype. สำหรับการแปลงที่เสถียร, ยีนควรจะถูกส่งผ่านไปยังลูกหลานในรูปแบบการถ่ายทอดทางพันธุกรรมของเมนเดล (อังกฤษ: Mendelian inheritance) เพื่อที่ว่าลูกหลานของสิ่งมีชีวิตจะได้ถูกศึกษาด้วย.
การแก้ไขจีโนม
บทความหลัก: การแก้ไขจีโนม
การแก้ไขจีโนมเป็นชนิดของพันธุวิศวกรรมในการที่ดีเอ็นเอจะถูกแทรก, ถูกแทนที่, หรือถูกเคลื่อนย้ายออกจากจีโนมโดยใช้ nucleases วิศวกรรมเทียม, หรือ "กรรไกรโมเลกุล". nucleases จะสร้างการแบ่งเกลียวคู่ (อังกฤษ: double-stranded break (DSBs)) ที่เฉพาะในสถานที่ที่ต้องการในจีโนม, และใชประโยชน์ของกลไกภายใน (อังกฤษ: endogenous mechanisms) ของเซลล์เพื่อซ่อมแซมการแบ่งที่เกิดจากกระบวนการทางธรรมชาติของการรวมตัวกันอีกแบบคล้ายคลึงกัน (อังกฤษ: homologous recombination (HR)) และการเชื่อมปลายแบบไม่คล้ายคลึงกัน (อังกฤษ: nonhomologous end-joining (NHEJ)). ปัจจุบันมีสี่ครอบครัวของ nucleases วิศวกรรมคือ:. meganucleases, zinc finger nucleases (ZFNs), transcription activator-like effector nuclease (TALENs) และ CRISPRs.
การประยุกต์ใช้งาน
พันธุวิศวกรรมมีการประยุกต์ใช้ในงานด้านการแพทย์, การวิจัย, อุตสาหกรรมและการเกษตรและสามารถนำมาใช้ในวงกว้างของพืช, สัตว์และจุลินทรีย์.
การแพทย์
ในการแพทย์, พันธุวิศวกรรมได้ถูกนำมาใช้เพื่อผลิตแบบมวลของอินซูลิน, ฮอร์โมนที่สร้างการเจริญเติบโตของมนุษย์, follistim (สำหรับการรักษาภาวะมีบุตรยาก), อัลบูมินมนุษย์ (โปรตีนชนิดหนึ่งพบในไข่ นม เนื้อสัตว์ และเลือด เป็นตัวขนส่งฮอร์โมน, กรดไขมัน, และส่วนผสมอื่นๆ, ผ่อนความเป็นกรดหรือความเป็นด่าง, และรักษาแรงดันของสารละลายที่ไหลผ่านเนื้อเยื่อ, ไปยังส่วนต่างๆของร่างกาย), monoclonal antibodies, antihemophilic factors, วัคซีนและยาอื่นๆอีกมากมาย. ขบวนการของวัคซีนโดยทั่วไปเกี่ยวข้องกับการฉีดรูปแบบของไวรัสหรือสารพิษของพวกมันที่อ่อนแอ, มีชีวิต, ตายแล้วหรือไม่มีกิจกรรมแล้วเข้าสู่บุคคลที่ไม่มีภูมิคุ้มกัน. ไวรัสดัดแปลงพันธุกรรมกำลังมีการพัฒนาที่ยังคงสามารถให้ภูมิคุ้มกัน, แต่ขาดลำดับการติดเชื้อ. หนูไฮบริด, เซลล์หลอมรวมกันเพื่อสร้าง monoclonal antibodies, ถูกทำให้ใช้ได้กับมนุษย์ผ่านทางพันธุวิศวกรรมเพื่อสร้าง monoclonal antibodies ของมนุษย์. พันธุวิศวกรรมได้แสดงให้เห็นสัญญาสำหรับการรักษารูปแบบบางอย่างของโรคมะเร็ง.
พันธุวิศวกรรมถูกนำมาใช้เพื่อสร้างแบบจำลองสัตว์ของโรคของมนุษย์. หนูดัดแปลงพันธุกรรมเป็นแบบจำลองสัตว์ดัดแปลงพันธุกรรมที่พบมากที่สุด. พวกมันได้ถูกนำมาใช้เพื่อการศึกษาและทำแบบจำลองมะเร็ง (หนู oncomouse), โรคอ้วน, โรคหัวใจ, โรคเบาหวาน, โรคไขข้อ, สารเสพติด, ความวิตกกังวล, โรคแก่และโรคพาร์กินสัน. การรักษาที่มีศักยภาพสามารถทดสอบกับแบบจำลองหนูเหล่านี้. นอกจากนี้หมูดัดแปลงพันธุกรรมยังถูกเพาะพันธ์โดยมีวัตถุประสงค์เพื่อเพิ่มความสำเร็จของการปลูกถ่ายอวัยวะสุกรให้กับมนุษย์.
การบำบัดด้วยยีนเป็นพันธุวิศวกรรมที่ทำกับมนุษย์โดยการเปลี่ยนยีนบกพร่องของมนุษย์ด้วยสำเนาการทำงานซึ่งอาจเกิดขึ้นในเนื้อเยื่อของร่างกายหรือเนื้อเยื่อ germline. ถ้ายีนถูกแทรกเข้าไปในเนื้อเยื่อ germline มันสามารถส่งผ่านลงไปที่ลูกหลานของบุคคลนั้น. การบำบัดด้วยยีนได้ถูกใช้อย่างประสบความสำเร็จในการรักษาหลายโรครวมถึง X-linked SCID, มะเร็งเม็ดเลือดขาวเรื้อรังแบบ lymphocytic (CLL) และโรคพาร์กินสัน. ในปี 2012, Glybera กลายเป็นการรักษาด้วยยีนบำบัดอันแรกที่ได้รับการอนุมัติสำหรับการใช้งานทางคลินิกทั้งในยุโรปหรือสหรัฐอเมริกาหลังจากการรับรองโดยคณะกรรมาธิการยุโรป. นอกจากนี้ยังมีความกังวลเกี่ยวกับจริยธรรมว่าเทคโนโลยีควรจะถูกใช้ไม่เพียงแต่สำหรับการรักษาเท่านั้น, แต่สำหรับการเพิ่มประสิทธิภาพ, การดัดแปลงหรือการเปลี่ยนแปลงของภาพลักษณ์, การปรับตัว, ความเฉลียวฉลาด, นิสัยหรือพฤติกรรมของมนุษย์ด้วยหรือไม่. ความแตกต่างระหว่างการรักษาและการเพิ่มประสิทธิภาพยังคงเป็นเรื่องยากที่จะจัดทำขึ้น. นักแปลงมนุษย์พิจารณาว่าการเพิ่มประสิทธิภาพของมนุษย์เป็นสิ่งพึงประสงค์.
การวิจัย


พันธุวิศวกรรมเป็นเครื่องมือที่สำคัญอันหนึ่งสำหรับนักวิทยาศาสตร์ธรรมชาติ. ยีนและข้อมูลทางพันธุกรรมอื่นๆจากหลากหลายของสิ่งมีชีวิตจะถูกแปลงให้เป็นเชื้อแบคทีเรียสำหรับการจัดเก็บและการดัดแปลง, เป็นการสร้างแบคทีเรียดัดแปลงพันธุกรรมในกระบวนการ. แบคทีเรียมีราคาถูก, ง่ายต่อการเติบโต, ทำโคลนิงได้, ทวีคูณอย่างรวดเร็ว, ค่อนข้างง่ายที่จะแปลงและสามารถเก็บไว้ที่ -80 °C เกือบจะนานไม่สิ้นสุด. เมื่อยีนถูกแยกออก, มันก็สามารถถูกจัดเก็บไว้ภายในแบคทีเรียเป็นให้อุปทานที่ไม่จำกัดสำหรับการวิจัย.
สิ่งมีชีวิตจะได้รับการดัดแปลงพันธุกรรมเพื่อค้นหาการทำงานของยีนบางตัว, ซึ่งอาจเป็นผลกระทบต่อฟีโนไทป์ของสิ่งมีชีวิต, ที่ยีนจะแสดงหรือสิ่งที่ยีนอื่นๆที่มันโต้ตอบด้วย. การทดลองเหล่านี้มักจะเกี่ยวข้องกับการสูญเสียหน้าที่การทำงานบางอย่างไป, การได้รับหน้าที่การทำงานบางอย่างมา, การติดตามและการแสดงออก.
- การทดลองของการสูญเสียหน้าที่การทำงานบางอย่างไป, เช่นในการทดลองเกี่ยวกับ gene knockout ครั้งหนึ่ง, สิ่งมีชีวิตถูกดัดแปลงให้ขาดกิจกรรมของยีนหนึ่งยีนหรือมากกว่า. การทดลอง gene knockout จะเกี่ยวข้องกับการสร้างและการยักย้ายถ่ายเทของดีเอ็นเอที่สร้าง ในหลอดทดลอง, ซึ่งในการ knockout อย่างง่ายประกอบด้วยหนึ่งสำเนาของยีนที่ต้องการ, ซึ่งมีการเปลี่ยนแปลงให้มันไม่ทำงาน. เซลล์ต้นกำเนิดจากตัวอ่อน (อังกฤษ: Embryonic stem cells) จะรวมกับยีนที่ถูกดัดแปลง, ซึ่งไปแทนที่สำเนาหน้าที่การทำงานที่ปรากฏอยู่แล้ว. เซลล์ต้นกำเนิดเหล่านี้จะถูกฉีดเข้าไปในตัวอ่อนซึ่งเป็นระยะก่อนที่จะฝังตัวกับมดลูก (อังกฤษ: blastocysts), ซึ่งจะถูกฝังลงในแม่อุ้มบุญ. วิธีการนี้จะช่วยให้ผู้ทดลองสามารถวิเคราะห์ข้อบกพร่องที่เกิดจากการกลายพันธุ์นี้และเพื่อกำหนดบทบาทของยีนนั้นๆ. มันถูกใช้บ่อยโดยเฉพาะอย่างยิ่งในการพัฒนาทางชีววิทยา. อีกวิธีหนึ่ง, ที่มีประโยชน์ในสิ่งมีชีวิตเช่นแมลงหวี่ (แมลงวันผลไม้), คือการเหนี่ยวนำให้เกิดการกลายพันธุ์ในประชากรขนาดใหญ่แล้วทำการสกรีนลูกหลานเพื่อให้ได้แบบการกลายพันธุ์ที่ต้องการ. กระบวนการที่คล้ายกันนี้สามารถนำมาใช้ทั้งในพืชและ prokaryotes (สิ่งมีชีวิตเซลล์เดียวที่มีนิวเคลียสที่ขาดเยื่อหุ้ม).
- การทดลองของการได้รับหน้าที่การทำงานบางอย่างมา, คู่ที่คล้ายกันแบบตรรกะของการ knockouts. การทดลองเหล่านี้ในบางครั้งจะดำเนินการร่วมกับการทดลองแบบ knockouts เพื่อสร้างการทำงานของยีนที่ต้องการอย่างประณีตมากขึ้น. กระบวนการนี้เหมือนมากกับกระบวนการในงานดัดแปลงแบบ knockout, ยกเว้นว่าโครงสร้างที่ถูกออกแบบมาเพื่อเพิ่มหน้าที่การทำงานของยีน, ที่มักจะโดยการให้สำเนาพิเศษของยีนหรือการกระตุ้นให้เกิดการสังเคราะห์โปรตีนให้บ่อยขึ้น.
- การทดลองการติดตาม, ซึ่งพยายามที่จะได้รับข้อมูลเกี่ยวกับการเป็นแบบท้องถิ่นและการปฏิสัมพันธ์ของโปรตีนที่ต้องการ. วิธีหนึ่งที่จะทำเช่นนี้คือการแทนที่ยีนป่าด้วยยิน 'ละลาย', ซึ่งเป็นการวางติดกันเพื่อเทียบเคียงชนิดหนึ่งของยีนป่าชนิดที่มีองค์ประกอบของการรายงานเช่นโปรตีนเรืองแสงสีเขียว (GFP) ที่จะช่วยให้มองเห็นได้ง่ายของผลิตภัณฑ์ของการดัดแปลงพันธุกรรม. ในขณะที่นี่เป็นเทคนิคที่มีประโยชน์อันหนึ่ง, การยักย้ายถ่ายเทสามารถทำลายหน้าที่การทำงานของยีน, เป็นการสร้างผลรองและอาจเรียกหาคำถามสำหรับผลของการทดลอง. เทคนิคที่ซับซ้อนมากขึ้นในขณะนี้อยู่ระหว่างการพัฒนาที่สามารถติดตามผลิตภัณฑ์โปรตีนโดยไม่ต้องบรรเทาฟังก์ชันการทำงานของพวกมัน, เช่นการเพิ่มลำดับขนาดเล็กที่จะทำหน้าที่แรงจูงใจแบบผูกพันกับแอนติบอดีแบบโมโนโคลนอล.
- การศึกษาการแสดงออก, มีวัตถุประสงค์ที่จะค้นพบที่ไหนและเมื่อไหร่ที่โปรตีนที่เจาะจงจะถูกผลิตขึ้น. ในการทดลองเหล่านี้, ลำดับดีเอ็นเอก่อนดีเอ็นเอที่บอกรหัสสำหรับโปรตีน, ที่รู้จักกันว่าเป็นโปรโมเตอร์ของยีน, จะถูกใส่เข้าไปใหม่ในสิ่งมีชีวิตที่มีภูมิภาคเข้ารหัสโปรตีนถูกแทนที่โดยยีนนักรายงานเช่น GFP หรือเอนไซม์ที่เร่งปฏิกิริยาการผลิตของสีย้อม. ดังนั้นเวลาและสถานที่ที่เป็นโปรตีนที่เจาะจงจะถูกผลิตจึงสามารถสังเกตได้. การศึกษาการแสดงออกสามารถก้าวไปอีกขั้นโดยการเปลี่ยนโปรโมเตอร์เพื่อที่จะหาชิ้นไหนที่มีความสำคัญสำหรับการแสดงออกที่เหมาะสมของยีนและถูกผูกไว้จริงโดยโปรตีนปัจจัยการถอดความ (อังกฤษ: transcription factor proteins); ขั้นตอนนี้ถูกเรียกว่าการทุบตีโปรโมเตอร์ (อังกฤษ: promoter bashing).
ด้านอุตสาหกรรม
การใช้เทคนิคพันธุวิศวกรรม, เราสามารถแปลงจุลินทรีย์เช่นแบคทีเรียหรือยีสต์, หรือแปลงเซลล์จากสิ่งมีชีวิตหลายเซลล์เช่นแมลงหรือสัตว์เลี้ยงลูกด้วยนม, ที่มียีนรหัสเข้าเป็นโปรตีนที่มีประโยชน์, เช่นเอนไซม์แบบหนึ่ง, เพื่อที่ว่าสิ่งมีชีวิตหลังการแปลงจะแสดงออกอย่างชัดแจ้งว่ามีโปรตีนที่ต้องการ. เราสามารถผลิตปริมาณแบบมวลของโปรตีนโดยการปลูกสิ่งมีชีวิตที่ถูกแปลงในอุปกรณ์เครื่องปฏิกรณ์ชีวภาพโดยใช้เทคนิคของการหมักอุตสาหกรรม, จากนั้นก็ทำโปรตีนให้บริสุทธิ์. ยีนบางตัวไม่ทำงานได้ดีในแบคทีเรีย, ดังนั้นยีสต์, เซลล์แมลง, หรือเซลล์สัตวืเลี้ยงลูกด้วยนม, แต่ละ eukaryote, ยังสามารถนำมาใช้ได้. เทคนิคเหล่านี้ถูกนำมาใช้ในการผลิตยารักษาโรคเช่นอินซูลิน, ฮอร์โมนการเจริญเติบโตของมนุษย์, และวัคซีน, อาหารเสริมเช่น tryptophan, ช่วยในการผลิตอาหาร (chymosin ในการทำชีส) และเชื้อเพลิง. การประยุกต์ใช้งานอื่นๆที่เกี่ยวข้องกับเชื้อแบคทีเรียดัดแปลงพันธุกรรมที่กำลังทำการตรวจสอบอยู่จะเกี่ยวกับการทำให้แบคทีเรียปฏิบัติงานนอกวงจรธรรมชาติของพวกมัน, เช่นการทำเชื้อเพลิงชีวภาพ, การทำความสะอาดน้ำมันรั่วไหล, คาร์บอนและขยะพิษอื่นๆ และการตรวจสอบสารหนูในน้ำดื่ม.
การประยุกต์ใช้ในอุตสาหกรรมและการทดลองในขนาดห้องปฏิบัติการ
ในวัสดุศาสตร์, ไวรัสดัดแปลงพันธุกรรมได้ถูกนำมาใช้ในห้องปฏิบัติการทางวิชาการโดยเป็นนั่งร้านสำหรับการประกอบแบตเตอรี่ลิเธียมไอออนที่เป็นมิตรกับสิ่งแวดล้อมมากขึ้น.
แบคทีเรียได้รับการดัดแปลงมาเพื่อทำงานเป็นเซ็นเซอร์โดยแสดงโปรตีนเรืองแสงภายใต้สภาพแวดล้อมบางอย่าง.
เกษตรกรรม
บทความหลัก: พืชดัดแปลงพันธุกรรม

หนึ่งในการประยุกต์ใช้พันธุวิศวกรรมที่รู้จักกันดีที่สุดและมีการโต้เถียงคือการสร้างและการใช้พืชดัดแปลงพันธุกรรมหรือสิ่งมีชีวิตดัดแปลงพันธุกรรม, เช่นปลาดัดแปลงพันธุกรรม, ซึ่งจะใช้ในการผลิตอาหารและวัสดุดัดแปลงพันธุกรรมที่มีการใช้งานที่หลากหลาย. มีสี่เป้าหมายหลักในการสร้างพืชดัดแปลงพันธุกรรม.
เป้าหมายหนึ่งและเป็นสิ่งแรกที่จะต้องตระหนักในเชิงพาณิชย์คือการให้ความคุ้มครองจากภัยคุกคามสิ่งแวดล้อม, เช่นความเย็น (ในกรณีของแบคทีเรียน้ำแข็ง-ลบ), หรือเชื้อโรค pathogen, เช่นแมลงหรือไวรัส, และ/หรือความต้านทานต่อสารเคมีกำจัดวัชพืช. นอกจากนี้ยังมีพืชทนเชื้อราและเชื้อไวรัสที่พัฒนาแล้วหรือกำลังพัฒนา. พวกมันได้รับการพัฒนาเพื่อให้การจัดการแมลงและวัชพืชของพืชทำได้ง่ายขึ้นและสามารถเพิ่มผลผลิตของพืชได้ทางอ้อม.
อีกเป้าหมายหนึ่งในการสร้าง GMOs ก็คือเพื่อปรับเปลี่ยนคุณภาพของผลผลิตโดย, ตัวอย่างเช่น, การเพิ่มคุณค่าทางโภชนาการหรือเพื่อให้เกิดประโยชน์ต่อวงการอุตสาหกรรมมากขึ้นทั้งปริมาณและคุณภาพ. มันฝรั่ง Amflora, ยกตัวอย่าง, ก่อให้เกิดประโยชน์มากขึ้นในอุตสาหกรรมการบ่มของแป้ง. วัวได้รับการดัดแปลงเพื่อผลิตโปรตีนในนมของพวกมันมากขึ้นเพื่ออำนวยความสะดวกในการผลิตชีส. ถั่วเหลืองและคาโนลาได้รับการดัดแปลงพันธุกรรมในการผลิตน้ำมันเพื่อสุขภาพมากขึ้น.
เป้าหมายอีกประการหนึ่งประกอบด้วยการผลักดันจีเอ็มโอเพื่อผลิตวัสดุที่ปกติมันไม่ได้ทำ. ตัวอย่างหนึ่งคือ "การทำฟาร์ม", ซึ่งใช้พืชเป็นตัวปฏิกรณ์ชีวะ (อังกฤษ: bioreactor) เพื่อผลิตวัคซีน, ตัวกลางยาหรือตัวยาเอง; ผลิตภัณฑ์ที่มีประโยชน์ถูกมำให้บริสุทธิ์จากการเก็บเกี่ยวแล้วนำไปใช้ในกระบวนการผลิตยามาตรฐาน. วัวและแพะที่ได้รับดัดแปลงเพื่อแสดงฤทธ์ของยาและโปรตีนอื่นๆในนมของพวกมัน, และในปี 2009 องค์การอาหารและยาได้อนุมัติยาที่ผลิตในนมแพะ.
เป้าหมายอีกอันในการสร้าง GMOs คือการเพิ่มผลผลิตโดยตรงด้วยการเร่งการเจริญเติบโต, หรือการทำสิ่งมีชีวิตบึกบึนกว่าเดิม (สำหรับพืช, โดยการปรับปรุงเกลือ, การอดทนต่อความเย็นหรือภัยแล้ง). บางสัตว์ที่สำคัญทางเกษตรกรรมได้รับการดัดแปลงพันธุกรรมด้วยฮอร์โมนการเจริญเติบโตเพิ่มขนาดของพวกมัน.
วิศวกรรมทางพันธุกรรมของพืชผลทางการเกษตรสามารถเพิ่มอัตราการเจริญเติบโตและความต้านทานต่อโรคที่แตกต่างกันที่เกิดจากเชื้อโรคและปรสิต. นี้จะเป็นประโยชน์อย่างมากในขณะที่มันสามารถเพิ่มการผลิตของแหล่งอาหารด้วยการใช้ทรัพยากรที่น้อยลงกว่าที่จะต้องใช้จริงเพื่อเป็นเจ้าภาพด้านประชากรที่เพิ่มมากขึ้นของโลก. พืชดัดแปลงเหล่านี้ยังจะช่วยลดการใช้สารเคมี, เช่นปุ๋ยและสารกำจัดศัตรูพืช, และดังนั้นจึงลดความรุนแรงและความถี่ของการเกิดความเสียหายที่เกิดจากมลพิษทางเคมีเหล่านี้อีกด้วย.
ความกังวลด้านจริยธรรมและความปลอดภัยได้รับการพูดถึงรอบๆการใช้อาหารดัดแปลงพันธุกรรม. ความกังวลด้านความปลอดภัยที่สำคัญเกี่ยวข้องกับผลกระทบต่อสุขภาพของมนุษย์จากการกินอาหารดัดแปลงพันธุกรรม, โดยเฉพาะเจาะจงว่าจะเป็นปฏิกิริยาที่เป็นพิษหรือการแพ้ที่อาจเกิดขึ้น. การไหลของยีนเข้าสู่พืชดัดแปรพันธุกรรมที่เกี่ยวข้อง, และผลกระทบนอกเป้าหมายในสิ่งมีชีวิตที่เป็นประโยชน์และผลกระทบต่อความหลากหลายทางชีวภาพเป็นปัญหาสิ่งแวดล้อมที่สำคัญ. ความกังวลด้านจริยธรรมเกี่ยวข้องกับประเด็นทางศาสนา, การควบคุมในองค์รวมของอุปทานอาหาร, สิทธิในทรัพย์สินทางปัญญาและระดับของการติดฉลากที่จำเป็นบนผลิตภัณฑ์ดัดแปลงทางพันธุกรรม.
BioArt และความบันเทิง
พันธุวิศวกรรมนอกจากนี้ยังถูกใช้ในการสร้าง BioArt. แบคทีเรียบางชนิดที่ได้รับการดัดแปลงพันธุกรรมเพื่อสร้างภาพขาวดำ.
พันธุวิศวกรรมได้ถูกนำมาใช้ในการสร้างรายการแปลกเช่นดอกคาร์เนชั่นสีลาเวนเดอร์ ดอกกุหลาบสีฟ้า และปลาเรืองแสง.
การกำกับดูแล
บทความหลัก: การกำกับดูแลของพันธุวิศวกรรมและการกำกับดูแลของการเปิดตัวของสิ่งมีชีวิตดัดแปลงพันธุกรรม
การกำกับดูแลของพันธุวิศวกรรมเกี่ยวข้องกับวิธีการดำเนินการของรัฐบาลในการประเมินและจัดการความเสี่ยงที่เกี่ยวข้องกับการพัฒนาและการเปิดตัวของพืชดัดแปลงพันธุกรรม. มีความแตกต่างในการกำกับดูแลของพืชดัดแปลงพันธุกรรมในแต่ละประเทศ, ที่มีบางประเทศที่แตกต่างกันส่วนใหญ่เกิดขึ้นระหว่างสหรัฐอเมริกาและยุโรป. การกำกับดูแลที่แตกต่างกันในประเทศหนึ่งๆขึ้นอยู่กับวัตถุประสงค์ของการใช้ผลิตภัณฑ์ของทางพันธุวิศวกรรม. ยกตัวอย่างเช่นพืชที่ไม่ได้มีไว้สำหรับใช้เป็นอาหารโดยทั่วไปจะไม่ถูกตรวจสอบโดยหน่วยงานที่รับผิดชอบสำหรับความปลอดภัยของอาหาร.
การโต้เถียง
บทความหลัก: การถกเถียงเรื่องการดัดแปลงพันธุกรรมอาหารและพันธุวิศวกรรมของมนุษย์
นักวิจารณ์ได้คัดค้านการใช้พันธุวิศวกรรมด้วยเหตุผลหลายอย่าง, รวมถึงความกังวลด้านจริยธรรม, ความกังวลด้านระบบนิเวศ, และความกังวลทางเศรษฐกิจที่ถูกยกขึ้นมาโดยความเป็นจริงที่ว่าเทคนิคจีเอ็มและสิ่งมีชีวิตจีเอ็มอยู่ภายใต้กฎหมายทรัพย์สินทางปัญญา. GMOs ยังเกี่ยวข้องกับการถกเถียงกันในเรื่องอาหารจีเอ็มด้วยคำถามที่ว่าอาหารที่ผลิตจากพืชจีเอ็มมีความปลอดภัยหรือไม่, ว่ามันควรจะได้รับการติดฉลากหรือไม่, และว่าพืชจีเอ็มมีความจำเป็นเพื่อแก้ปัญหาความต้องการอาหารของโลกหรือไม่. โปรดดูบทความการถกเถียงเรื่องอาหารดัดแปลงพันธุกรรมสำหรับการอภิปรายในประเด็นที่เกี่ยวกับพืชจีเอ็มและอาหารจีเอ็ม. การถกเถียงเหล่านี้ได้นำไปสู่การฟ้องร้อง, ข้อพิพาทการค้าระหว่างประเทศ, และการประท้วง, และการกำกับดูแลที่เข้มงวดของผลิตภัณฑ์ในเชิงพาณิชย์ในบางประเทศ.
ดูเพิ่ม
- Biological engineering
- Gene patent
- Gene drive
- Genetic engineering in the United States
- Genetically modified crops
- Genetically modified food
- Genetically modified food controversies
- Genetically modified organisms
- Induced stem cells
- Marker assisted selection, วิธีหนึ่งที่คัดเลือกลูกหลานที่เหมาะสมโดยไม่ต้องใช้พันธุวิศวกรรม
- Paratransgenesis
- Regulation of the release of genetic modified organisms
อ้างอิง
This article uses material from the Wikipedia ไทย article พันธุวิศวกรรม, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). เนื้อหาอนุญาตให้เผยแพร่ภายใต้ CC BY-SA 4.0 เว้นแต่ระบุไว้เป็นอื่น Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki ไทย (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.