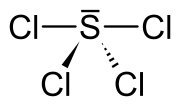硫黄 の化合物
「硫黄 の化合物」の検索結果 - Wiki 硫黄 の化合物
このウィキでページ「硫黄+の化合物」は見つかりませんでした。以下の検索結果も参照してください。
 硫黄から製造される硫酸は化学工業上、もっとも重要な酸である。一般的に酸として用いられるのは希硫酸で、脱水剤や乾燥剤に用いられるのは濃硫酸である。また、種々の硫黄を含んだ化合物が合成されている。 硫黄は古来から漂白剤、儀式用の香料、殺虫剤、接着剤など多様に用いられていた。また黒色火薬の…
硫黄から製造される硫酸は化学工業上、もっとも重要な酸である。一般的に酸として用いられるのは希硫酸で、脱水剤や乾燥剤に用いられるのは濃硫酸である。また、種々の硫黄を含んだ化合物が合成されている。 硫黄は古来から漂白剤、儀式用の香料、殺虫剤、接着剤など多様に用いられていた。また黒色火薬の… 3つのヘテロ原子を含む五員環も大きなグループである。例として、2つの硫黄原子と1つの窒素原子を含むジチアゾールがある。 6つの窒素原子を含む仮想上の化合物は、ヘキサジンと呼ばれる。 七員環の場合、通常の芳香族安定化を利用するためには、ヘテロ原子が空のπ軌道(例:ホウ素)を提供できる必要がある。それ以外の場合には、ホモ芳香族性による安定化が可能である。…
3つのヘテロ原子を含む五員環も大きなグループである。例として、2つの硫黄原子と1つの窒素原子を含むジチアゾールがある。 6つの窒素原子を含む仮想上の化合物は、ヘキサジンと呼ばれる。 七員環の場合、通常の芳香族安定化を利用するためには、ヘテロ原子が空のπ軌道(例:ホウ素)を提供できる必要がある。それ以外の場合には、ホモ芳香族性による安定化が可能である。…- 二元化合物(にげんかごうぶつ、英: binary compound)とは、全く異なる2種類の元素を含む化合物である。共有結合性二元化合物には、水 (H2O)、一酸化炭素 (CO)、六フッ化硫黄 (SF6) などがある。イオン結合性二元化合物には、塩化カルシウム (CaCl2)、フッ化ナトリウム (NaF)、酸化マグネシウム…
- 有機硫黄化合物(ゆうきいおうかごうぶつ)とは硫黄原子を含む有機化合物の総称である。有機硫黄化合物に分類されるものは多岐にわたるが、一般的に不快な臭気を持ち、糖鎖(炭水化物の鎖)や硫黄の化合物を含む生物が生長するときの老廃物として、あるいは腐敗する際に自然に生成する。海洋においても生物起源の硫黄化合物…
- 硫黄の化合物の一覧(いおうのかごうぶつのいちらん)は硫黄の化合物(有機化合物を除く)の一覧。 二臭化硫黄(SBr2) 四臭化硫黄(SBr4) 二臭化二硫黄(S2Br2) 二塩化硫黄(SCl2) 四塩化硫黄(SCl4) 二塩化二硫黄(S2Cl2) 二フッ化硫黄(SF2) 四フッ化硫黄(SF4) 六フッ化硫黄(SF6)…
- 無機化合物(むきかごうぶつ、英語: inorganic compound)は、有機化合物以外の化合物であり、具体的には単純な一部の炭素化合物(下に示す)と、炭素以外の元素で構成される化合物である。無機には「生命力を有さない」という意味がある。 炭素化合物のうち無機化合物…
 二酸化硫黄は火山活動や工業活動により産出される。石炭や石油は多量の硫黄化合物を含んでおり、この硫黄化合物が燃焼することで発生する。また、火山活動でも発生する。二酸化硫黄は二酸化窒素などの存在下で酸化され硫酸となり、酸性雨の原因となる。空気よりも重い。 二酸化硫黄は硫黄の完全燃焼により発生する。 S ( s ) + O…
二酸化硫黄は火山活動や工業活動により産出される。石炭や石油は多量の硫黄化合物を含んでおり、この硫黄化合物が燃焼することで発生する。また、火山活動でも発生する。二酸化硫黄は二酸化窒素などの存在下で酸化され硫酸となり、酸性雨の原因となる。空気よりも重い。 二酸化硫黄は硫黄の完全燃焼により発生する。 S ( s ) + O… 硫酸 (カテゴリ 硫黄の化合物)肥料としては硫安、過リン酸石灰の製造原料として大量に消費される。紙を濃硫酸で処理した半透明の薄い紙は硫酸紙と呼ばれ、羊皮紙の代用として用いられる。 硫酸イオン(りゅうさんいおん、sulfate, SO2− 4)は主に硫酸およびその化合物の電離、分解などによって生成する2価の陰イオンで硫酸塩結晶中にも存在する、硫黄化合物である。…
硫酸 (カテゴリ 硫黄の化合物)肥料としては硫安、過リン酸石灰の製造原料として大量に消費される。紙を濃硫酸で処理した半透明の薄い紙は硫酸紙と呼ばれ、羊皮紙の代用として用いられる。 硫酸イオン(りゅうさんいおん、sulfate, SO2− 4)は主に硫酸およびその化合物の電離、分解などによって生成する2価の陰イオンで硫酸塩結晶中にも存在する、硫黄化合物である。…- 芳香族化合物(ほうこうぞくかごうぶつ、aromatic compounds)は、ベンゼンを代表とする環状不飽和有機化合物の一群。炭化水素のみで構成されたものを芳香族炭化水素 (aromatic hydrocarbon)、環構造に炭素以外の元素を含むものを複素芳香族化合物 (heteroaromatic…
- フッ化硫黄(フッかいおう、sulfur fluoride)はフッ素と硫黄とから構成される無機化合物で、異性体を含めて以下の6種類が知られている。十フッ化二硫黄のみが常温常圧で液体であり、他は気体の化合物である。 二フッ化二硫黄(にフッかにいおう、disulfur difluoride)には F−S−S−F…
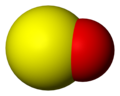 と同様である。基底状態で三重項の電子配置をとる化合物は珍しく、同じく類縁体である S2 が一重項であるのと対照的である。 S−O結合長は148.1 pmであり、低級硫黄酸化物(例: S8O, S−O = 148 pm)で見られる結合長と同様であるが、ガス状のS2O (146 pm)、SO2 (143.1 pm)、SO3…
と同様である。基底状態で三重項の電子配置をとる化合物は珍しく、同じく類縁体である S2 が一重項であるのと対照的である。 S−O結合長は148.1 pmであり、低級硫黄酸化物(例: S8O, S−O = 148 pm)で見られる結合長と同様であるが、ガス状のS2O (146 pm)、SO2 (143.1 pm)、SO3…- 硫黄酸化物(いおうさんかぶつ、英: sulfur oxide)は、硫黄の酸化物の総称。一酸化硫黄 (SO)、二酸化硫黄(亜硫酸ガス)(SO2)、三酸化硫黄 (SO3) などが含まれる。化学式から SOx (ソックス)と略称される。 石油や石炭など硫黄分が含まれる化石燃料を燃焼させることにより発生す…
 化学物質 (カテゴリ Webarchiveテンプレートのウェイバックリンク)substance)とは、一定の化学組成と特徴的な性質を持つ物質の一形態である。化学物質には、単体(単一の化学元素からなる物質)、化合物、または合金がある。 物理的な手段によって、より単純な構成成分に分離できない化学物質は「純粋(pure)」であると言われ、この概念は混合物と区別することを意図している。純粋な化学物質の…
化学物質 (カテゴリ Webarchiveテンプレートのウェイバックリンク)substance)とは、一定の化学組成と特徴的な性質を持つ物質の一形態である。化学物質には、単体(単一の化学元素からなる物質)、化合物、または合金がある。 物理的な手段によって、より単純な構成成分に分離できない化学物質は「純粋(pure)」であると言われ、この概念は混合物と区別することを意図している。純粋な化学物質の… ジスルフィド (カテゴリ 硫黄の化合物)disulphide) とは、2個の硫黄原子が繋がったジスルフィド基 (-S-S-) を官能基として有する有機硫黄化合物の総称。一般式は R-S-S-R' と表される。 ジスルフィドの英語表記はdisulfideで、この用語は二硫化物イオン (S22−) を構造に含む塩や錯体の総称でもある。日本語ではその総称をもっぱら…
ジスルフィド (カテゴリ 硫黄の化合物)disulphide) とは、2個の硫黄原子が繋がったジスルフィド基 (-S-S-) を官能基として有する有機硫黄化合物の総称。一般式は R-S-S-R' と表される。 ジスルフィドの英語表記はdisulfideで、この用語は二硫化物イオン (S22−) を構造に含む塩や錯体の総称でもある。日本語ではその総称をもっぱら… セレン (カテゴリ Webarchiveテンプレートのウェイバックリンク)セレンを主成分とする鉱物は、銅あるいは銀との化合物のセレン銀鉱やセレン銅銀鉱が知られるが、産出量の少ない鉱物であるため鉱石として利用はされない。硫黄化合物として産出することが多いため、工業的には硫酸製造の際の沈殿物や銅精錬時の副産物を精錬し得る。 21世紀になって中国が需要増により自国生産を始めるまでは日本が世界最大の…
セレン (カテゴリ Webarchiveテンプレートのウェイバックリンク)セレンを主成分とする鉱物は、銅あるいは銀との化合物のセレン銀鉱やセレン銅銀鉱が知られるが、産出量の少ない鉱物であるため鉱石として利用はされない。硫黄化合物として産出することが多いため、工業的には硫酸製造の際の沈殿物や銅精錬時の副産物を精錬し得る。 21世紀になって中国が需要増により自国生産を始めるまでは日本が世界最大の…- EC番号 (酵素番号) (カテゴリ 日本語版記事がリダイレクトの仮リンクを含む記事)-(チトクロームを用いる) EC 1.3.3.-(酸素を用いる) EC 1.3.5.-(キノンあるいは類縁化合物を用いる) EC 1.3.7.-(鉄硫黄蛋白質を用いる) EC 1.3.99.-(その他の電子受容体を用いる) EC 1.4.-(CH-NH2に対し酸化酵素として働く) EC 1.4.1.- EC…
 古くから製鉄などにおいて、フッ素の化合物である蛍石(CaF2)が融剤として用いられた。たとえば、ドイツの鉱物学者ゲオルク・アグリコラは1530年に著書『ベルマヌス(Bermannus, sive de re metallica dialogus)』において、蛍石を炎の…
古くから製鉄などにおいて、フッ素の化合物である蛍石(CaF2)が融剤として用いられた。たとえば、ドイツの鉱物学者ゲオルク・アグリコラは1530年に著書『ベルマヌス(Bermannus, sive de re metallica dialogus)』において、蛍石を炎の…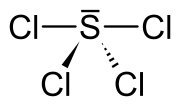 四塩化硫黄(英語:Sulfur tetrachloride、化学式:SCl4)は、硫黄と塩素から成る無機化合物である。不安定な淡黄色の化合物であり、固体状態のものしか得られていない。 低温で二塩化硫黄を塩素と反応させることで得られる。 SCl 2 + Cl 2 → 193 K SCl 4 {\displaystyle…
四塩化硫黄(英語:Sulfur tetrachloride、化学式:SCl4)は、硫黄と塩素から成る無機化合物である。不安定な淡黄色の化合物であり、固体状態のものしか得られていない。 低温で二塩化硫黄を塩素と反応させることで得られる。 SCl 2 + Cl 2 → 193 K SCl 4 {\displaystyle… 二硫酸 (カテゴリ 硫黄の化合物)二硫酸(にりゅうさん)は硫黄のオキソ酸のひとつ。ピロ硫酸(pyrosulfuric acid)とも呼ばれる。化学式はH2S2O7。2分子の硫酸が脱水縮合した化合物に相当する。発煙硫酸中に存在し、芳香族化合物に対してスルホン化剤としてはたらく。 スルホン化やニトロ化などにおいて二硫酸の反応性を利用するときは、通常は発煙硫酸をそのまま用いる。…
二硫酸 (カテゴリ 硫黄の化合物)二硫酸(にりゅうさん)は硫黄のオキソ酸のひとつ。ピロ硫酸(pyrosulfuric acid)とも呼ばれる。化学式はH2S2O7。2分子の硫酸が脱水縮合した化合物に相当する。発煙硫酸中に存在し、芳香族化合物に対してスルホン化剤としてはたらく。 スルホン化やニトロ化などにおいて二硫酸の反応性を利用するときは、通常は発煙硫酸をそのまま用いる。… 二塩化硫黄(にえんかいおう)とは、硫黄と塩素からなる。塩化硫黄(II)とも呼ばれる。Cl-S-Cl の構造を持つ分子で、硫黄上の結合角は 109.3 °。外見は赤色の液体である。 一塩化硫黄に塩素を作用させると、二塩化硫黄に変わる。 S2Cl2+Cl2⟶2SCl2{\displaystyle {\ce…
二塩化硫黄(にえんかいおう)とは、硫黄と塩素からなる。塩化硫黄(II)とも呼ばれる。Cl-S-Cl の構造を持つ分子で、硫黄上の結合角は 109.3 °。外見は赤色の液体である。 一塩化硫黄に塩素を作用させると、二塩化硫黄に変わる。 S2Cl2+Cl2⟶2SCl2{\displaystyle {\ce…
- 高等学校の学習 > 高等学校理科 > 高等学校 化学 > 有機化合物の特徴 炭素を含む化合物を有機化合物(organic compound)という。しかし、一酸化炭素 CO {\displaystyle {\ce {CO}}} や二酸化炭素 CO 2 {\displaystyle {\ce {CO_2}}}
- の粉末を飽和させ、ダイナマイト、雲母粉、デュアリン、レンドロックなどと呼ばれるさまざまな発破粉を形成する。これらの化合物は比較的安全に輸送することができる。しかし、ニトログリセリンは簡単に粉末から排出され、化合物を入れている容器の隙間からにじみ出てくる。そのため、箱の
- りゅうか 【流下】流れ下ること。 【琉歌】沖縄の短詩的歌謡。 【硫化】硫黄の化合物。
- カルボン酸の酸ハロゲン化物は、これを構成するカルボン酸が属する項に属する。 6 第29.30 項又は第29.31 項の化合物は、その分子中において水素、酸素又は窒素の原子のほか硫黄、砒素、鉛その他の非金属又は金属の原子が炭素原子と直接に結合している有機化合物に限る。第29.30 項(有機硫黄化合物)及び第29