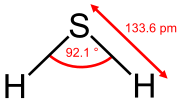水素 イオン
「水素 イオン」の検索結果 - Wiki 水素 イオン
このウィキでページ「水素+イオン」は見つかりませんでした。以下の検索結果も参照してください。
 - プント系列 化学 水素化 水素結合 水素脆化 水素爆発 水素イオン 水素化合物 工学 水素製造 熱化学水素製造 水素吸蔵合金 水素爆弾 ニッケル・水素充電池 燃料電池 文学 水素製造法(小説) ウィキペディアの姉妹プロジェクトで 「水素」に関する情報が検索できます。 ウィクショナリーの辞書項目 コモンズのメディア…
- プント系列 化学 水素化 水素結合 水素脆化 水素爆発 水素イオン 水素化合物 工学 水素製造 熱化学水素製造 水素吸蔵合金 水素爆弾 ニッケル・水素充電池 燃料電池 文学 水素製造法(小説) ウィキペディアの姉妹プロジェクトで 「水素」に関する情報が検索できます。 ウィクショナリーの辞書項目 コモンズのメディア… 水素イオン指数(すいそイオンしすう、英:potential of hydrogen 、独: Wasserstoffionenexponent)とは、溶液の酸と塩基の程度を表す物理量で、記号pH(ピーエッチ、ピーエイチ、ペーハー)で表す。水素イオン濃度指数または水素…
水素イオン指数(すいそイオンしすう、英:potential of hydrogen 、独: Wasserstoffionenexponent)とは、溶液の酸と塩基の程度を表す物理量で、記号pH(ピーエッチ、ピーエイチ、ペーハー)で表す。水素イオン濃度指数または水素… 水素イオン(1価の陽イオン) - H + {\displaystyle {\ce {H^+}}} 硫酸イオン(2価の陰イオン) - SO 4 2 − {\displaystyle {\ce {SO4{}^{2-}}}} イオンの名称は、陽イオンについては「元素名+イオン」(例:水素イオン)、陰イオンについては「元素名…
水素イオン(1価の陽イオン) - H + {\displaystyle {\ce {H^+}}} 硫酸イオン(2価の陰イオン) - SO 4 2 − {\displaystyle {\ce {SO4{}^{2-}}}} イオンの名称は、陽イオンについては「元素名+イオン」(例:水素イオン)、陰イオンについては「元素名…- 水素イオン(hydrogen ion)という用語は、国際純正・応用化学連合によって、水素及びその同位体の全てのイオンを表す一般名として勧告されている。イオンの電荷によって、陽イオンと陰イオンの2つの異なる分類に分けることができる。 水素が電子を失うと、以下の陽イオンが形成されうる。 ヒドロン -…
 炭酸水素塩(たんさんすいそえん、hydrogencarbonate)または重炭酸塩(じゅうたんさんえん、Bicarbonate)は炭酸水素イオンを含む、水素塩(酸性塩)の一種である。リチウムを除くアルカリ金属塩、カドミウム塩、およびアンモニウム塩などが固体の結晶として単離されているが、アルカリ土類金…
炭酸水素塩(たんさんすいそえん、hydrogencarbonate)または重炭酸塩(じゅうたんさんえん、Bicarbonate)は炭酸水素イオンを含む、水素塩(酸性塩)の一種である。リチウムを除くアルカリ金属塩、カドミウム塩、およびアンモニウム塩などが固体の結晶として単離されているが、アルカリ土類金…- 炭酸水素塩泉(たんさんすいそえんせん)は、掲示用泉質名に基づく温泉の泉質の分類の1種である。療養泉の中の塩類泉に分類される。 温泉水1 kg中に含まれる水以外の成分が1000 mg以上存在し、そのうち炭酸水素ナトリウム (NaHCO3) の含有量が340 mgを超える温泉。 炭酸水素イオン…
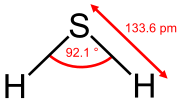 硫化水素は共有結合性の水素化合物で、硫黄と酸素とが周期表において同じ元素の族(第16族)であるため水と分子構造がよく似ている。密度は、空気を1とすると1.190であり空気よりも重い。 水溶液(硫化水素酸)では、硫化水素イオン (HS−) と水素イオン (H+) に電離して弱い酸性を示す。…
硫化水素は共有結合性の水素化合物で、硫黄と酸素とが周期表において同じ元素の族(第16族)であるため水と分子構造がよく似ている。密度は、空気を1とすると1.190であり空気よりも重い。 水溶液(硫化水素酸)では、硫化水素イオン (HS−) と水素イオン (H+) に電離して弱い酸性を示す。…- CH 2O (水素原子は炭素や酸素の2倍)だが、分子式は C 6H 12O 6 (水素原子12個、炭素と酸素原子6個)である。 化学式が示性式(condensed formula)として記述される場合、原子が化学的に結合する固有の方法(共有結合、イオン…
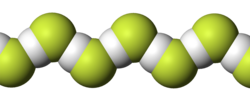 で、常温では気体または液体。塩化水素などの他のハロゲン化水素の場合に比べて性質が異なる点がある。まず、F-H の結合エネルギーが大きいために電離し難く、希薄水溶液においては弱酸として振舞う。これはフッ化物イオンのイオン半径が小さいため、水素イオンとの静電気力が強いことによるとも解釈される。また、水素…
で、常温では気体または液体。塩化水素などの他のハロゲン化水素の場合に比べて性質が異なる点がある。まず、F-H の結合エネルギーが大きいために電離し難く、希薄水溶液においては弱酸として振舞う。これはフッ化物イオンのイオン半径が小さいため、水素イオンとの静電気力が強いことによるとも解釈される。また、水素… 燃料電池にはさまざまな種類があるが、いずれも陽極と陰極、そしてイオン(多くは正電荷の水素イオン(プロトン))を行き来させる電解質で構成され、その電解質は燃料電池の両側面に存在する。陽極では、触媒によって燃料が酸化反応を起こし、イオン(多くの場合、正電荷の水素イオン)と電子が生成される。イオン…
燃料電池にはさまざまな種類があるが、いずれも陽極と陰極、そしてイオン(多くは正電荷の水素イオン(プロトン))を行き来させる電解質で構成され、その電解質は燃料電池の両側面に存在する。陽極では、触媒によって燃料が酸化反応を起こし、イオン(多くの場合、正電荷の水素イオン)と電子が生成される。イオン…- 炭酸水素イオンが陰イオンの主成分であるもので、陽イオンの主成分により以下のように細別する ナトリウム-炭酸水素塩泉 カルシウム-炭酸水素塩泉 マグネシウム-炭酸水素塩泉 硫酸塩泉 - 硫酸イオンが陰イオンの主成分であるもので(硫酸イオンと硫酸水素イオンの合計)、陽イオンの主成分により以下のように細別する ナトリウム-硫酸塩泉…
 水素・非共有電子対の相対配置にも依存する相互作用であるため、水素イオン(プロトン)の「キャッチボール」と表現されることもある。 典型的な水素結合(5〜30 kJ/mol)は、ファンデルワールス力より10倍程度強いが、共有結合やイオン結合よりはるかに弱い。水素…
水素・非共有電子対の相対配置にも依存する相互作用であるため、水素イオン(プロトン)の「キャッチボール」と表現されることもある。 典型的な水素結合(5〜30 kJ/mol)は、ファンデルワールス力より10倍程度強いが、共有結合やイオン結合よりはるかに弱い。水素… 5℃であり固体(H3O+·HSO4−)はオキソニウムイオンと硫酸水素イオンからなるイオン結晶である。 硫酸水素アンモニウム (NH4HSO4) 硫酸水素カリウム (KHSO4) 硫酸水素カルシウム (Ca(HSO4)2) 硫酸水素ナトリウム (NaHSO4) 硫酸水素ニトロシル (NOHSO4) – ニトロソ化試薬…
5℃であり固体(H3O+·HSO4−)はオキソニウムイオンと硫酸水素イオンからなるイオン結晶である。 硫酸水素アンモニウム (NH4HSO4) 硫酸水素カリウム (KHSO4) 硫酸水素カルシウム (Ca(HSO4)2) 硫酸水素ナトリウム (NaHSO4) 硫酸水素ニトロシル (NOHSO4) – ニトロソ化試薬…- おもに有機化合物への還元剤、特に水素化試薬として用いる。 非金属との水素化合物では、水素の酸化数は +1 である。これらは水素化物イオンを持たないため、水素化物とは呼ばない。17族元素との水素化合物はハロゲン化水素と呼ばれ、フッ化水素が弱酸である他は全て強酸である。 また、炭素との水素化合物は炭化水素であり石油中に多くの種類が産出する。…
- < HI の順である。 それに対して、液化フッ化水素は水に相当する誘電率と相対的に高い沸点を持ち、水素結合を形成する極性物質である点で特徴的である。また、希薄溶液であってもフッ化水素は水中で完全電離しない。これはイオン半径の小さなものほど水素イオンとの間の静電気力が強くなり、結合が強くなるためである。…
 −10)。ヨウ素と水素は電気陰性度に差がほとんどなく分子の極性は小さいが、ヨウ化物イオンのイオン半径が大きく水素イオンとの静電気力が小さく電離しやすいため、ヨウ化水素は強酸となる。還元力が強く、空気中の酸素に触れると容易に酸化を受けヨウ素の赤紫色を呈する。 水に極めて溶解しやすい気体であり、水溶液はヨウ化水素酸 (hydroiodic…
−10)。ヨウ素と水素は電気陰性度に差がほとんどなく分子の極性は小さいが、ヨウ化物イオンのイオン半径が大きく水素イオンとの静電気力が小さく電離しやすいため、ヨウ化水素は強酸となる。還元力が強く、空気中の酸素に触れると容易に酸化を受けヨウ素の赤紫色を呈する。 水に極めて溶解しやすい気体であり、水溶液はヨウ化水素酸 (hydroiodic…- 酸(さん、英: acid)は、化学において、水素イオンを与える、または電子対を受け取る性質をもつ物質である。塩基と対になってはたらく。 一般に、プロトン(H+)を与える、または電子対を受け取る物質である。歴史上、概念の拡大を伴いながら、幾つかの定義が考えられた。…
 アンモニウムイオン (英: ammonium) はアンモニアに水素イオンが付加(配位結合)することにより生成し、アンモニア水の電離によっても一部生成する1価の陽イオンであり、オニウムイオンの一種である。正四面体型構造をとる。 アンモニウムイオンを含むイオン結晶をアンモニウム塩(アンモニウムえん、英:…
アンモニウムイオン (英: ammonium) はアンモニアに水素イオンが付加(配位結合)することにより生成し、アンモニア水の電離によっても一部生成する1価の陽イオンであり、オニウムイオンの一種である。正四面体型構造をとる。 アンモニウムイオンを含むイオン結晶をアンモニウム塩(アンモニウムえん、英:…- リチウムイオン二次電池(リチウムイオンにじでんち、英: lithium-ion battery)は、正極と負極の間をリチウムイオンが移動することで充電や放電を行う二次電池(充電可能な電池)である。正極、負極、電解質それぞれの材料は用途やメーカーによって様々であるが、代表的な構成は、正極にリチウム遷…
 イオンとともに隣接する水分子に水素結合していることが明らかになった。(この問題についてのより深い議論についてはヒドロニウムを参照すること) 強酸なので、塩化水素のKa (酸解離定数) は大きい。理論的な推定では、塩化水素のpKaは-5.9であることが示唆されている。ただし、塩化水素…
イオンとともに隣接する水分子に水素結合していることが明らかになった。(この問題についてのより深い議論についてはヒドロニウムを参照すること) 強酸なので、塩化水素のKa (酸解離定数) は大きい。理論的な推定では、塩化水素のpKaは-5.9であることが示唆されている。ただし、塩化水素…
- この樹脂は、水溶液中では水素イオンを放出し、代わりに溶液中の他の陽イオンと結合する事ができる。このような、水溶液中では水素イオンを放出し、代わりに溶液中の他の陽イオンと結合する事ができる 樹脂を陽イオン交換樹脂という。 このスチレンとp-ジビニルベンゼンを共重合化させたものを濃硫酸でスルホ化させた樹脂は、陽イオン
- (十一) 負の水素イオンビーム用の電流注入器 (十二) 加速器の部分品であって、人工衛星又は高度一〇〇キロメートル以上の上空を飛行中の飛行体内で使用できるもの (十三) 負のイオンビーム注入装置 (十四) 高エネルギーのイオンビームを制御し、又は方向転換するための装置 (十五) 負の水素
- 水素イオン濃度、水素イオン指数 ドイツ語: potenz+H ペーハー
- pH(ピーエッチまたはペーハー)とは溶液の酸性度またはアルカリ性度を示す指標で、potential of hydrogen または power of hydrogenの略。 溶液中の水素イオン濃度を[H+]として、pH = -log10[H+] で計算されます。中性水溶液においては7で、アルカリ性度が上がるほど数値は大きくなり、酸性度