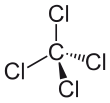
Ogljikov Tetraklorid
Ogljikov tetraklorid, znan tudi kot tetraklorometan in tetraklorogljik, je organska spojina s formulo CCl4.
Nekateri viri ga uvrščajo med anorganske spojine.
| |||
 | |||
| Imena | |||
|---|---|---|---|
| IUPAC ime ogljikov tetraklorid, tetraklorometan | |||
| Druga imena benziform, benzinoform, ogljikov klorid, halon-104, metan tetraklorid, perklorometan, tetraform, tetrasol | |||
| Identifikatorji | |||
3D model (JSmol) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.239 | ||
| EC število |
| ||
| KEGG | |||
PubChem CID | |||
| RTECS število |
| ||
| UNII | |||
| UN število | 1846 | ||
CompTox Dashboard (EPA) | |||
| |||
| |||
| Lastnosti | |||
| CCl4 | |||
| Molska masa | 153,81 g·mol−1 | ||
| Videz | brezbarvna tekočina | ||
| Vonj | sladkoben, etru podoben vonj | ||
| Gostota | 1,5867 g cm−3 (tekoč) 1,831 g cm−3 pri −186 °C (trden) | ||
| Tališče | −22,92 °C (−9,26 °F; 250,23 K) | ||
| Vrelišče | 76,72 °C (170,10 °F; 349,87 K) | ||
| 0,097 g/100 mL (0 °C) 0.081 g/100 mL (25 °C) | |||
| Topnost | topen v etanolu, etru, kloroformu, benzenu, bencinu, ogljikovem disulfidu in mravljinčni kislini | ||
| log P | 2.64 | ||
| Parni tlak | 11,94 kPa pri 20 °C | ||
| kH | 2,76x10−2 atm·m3/mol | ||
| Lomni količnik (nD) | 1,4607 | ||
| Dipolni moment | 0 D | ||
| Struktura | |||
| Kristalna struktura | monoklinski | ||
| Oblika molekule | tetraedrična | ||
| Termokemija | |||
| Specifična toplota, C | 132,6 J/mol K | ||
| Standardna molarna entropija S | 214,4 J/mol K | ||
Std tvorbena entalpija (ΔfH⦵298) | -139,3 kJ/mol | ||
Gibbsova prosta energija (ΔfG˚) | -686 kJ/mol | ||
| Nevarnosti | |||
EU klasifikacija (DSD) (zastarelo) | |||
| R-stavki (zastarelo) | R23/24/25, R40, R48/23, Predloga:R59, Predloga:R52/53 | ||
| S-stavki (zastarelo) | (S1/2), (S23), S36/37, (S45), R59, (S61) | ||
| NFPA 704 (diamant ognja) | |||
| Plamenišče | ni vnetljiv | ||
| Smrtni odmerek ali koncentracija (LD, LC): | |||
LD50 (srednji odmerek) | 2350 mg/kg | ||
| Sorodne snovi | |||
| Drugi kationi | silicijev tetraklorid, germanijev tetraklorid, kositrov tetraklorid, svinčev tetraklorid | ||
| Sorodno klorometani | klorometan, diklorometan, kloroform | ||
| Sorodne snovi | tetrafluorometan, tetrabromometan, tetrajodometan | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
V preteklosti se je pogosto uporabljal kot sredstvo za gašenje, hladilno sredstvo in topilo. Je brezbarvna tekočina s sladkobnim vonjem, ki je zaznaven že pri majhnih koncentracijah.
Zgodovina in sinteza
Ogljikov tetraklorid je prvi sintetiziral francoski kemik Henri Victor Regnault leta 1839 z reakcijo kloroforma s klorom. Sedaj se proizvaja predvsem s kloriranjem metana:
- CH4 + 4 Cl2 → CCl4 + 4 HCl
Za proizvodnjo se pogosto uporabljajo stranski produkti drugih reakcij, na primer diklorometan in kloroform:
- C2Cl6 + Cl2 → 2 CCl4
Do 1950. let se je proizvajal s kloriranjem ogljikovega disulfida pri temperaturi 105−130 °C:
- CS2 + 3Cl2 → CCl4 + S2Cl2
Proizvodnja ogljikovega trtraklorida je v 1980. letih začela močno upadati zaradi njegovega škodljivega vpliva na okolje in upadanja potreb po halogeniranih alkanih, ki se je proizvajali iz njega. Leta 1992 je bila proizvodnja ogljikovega tetraklorida v ZDA, Evropi in na Japonskem približno 720.000 ton.
Lastnosti
V molekuli ogljikovega tetraklorida so štirje atomi klora razporejeni v oglišča tetraedra z ogljikovim atomom v središču. Atomi klora in ogljika so povezani z enojnimi kovalentnimi vezmi. Molekula je zaradi simetrije nepolarna. Ogljikov tetraklorid je dobro topilo za druge nepolarne spojine, maščobe, olja in celo jod. Njegovi hlapi imajo podoben vonj kot druga klorirana topila in je značilen za kemične čistilnice.
Trdni ogljikov tetraklorid ima dva polimorfa: kristalnega II pri temperaturah pod −47,5 °C in kristalnega I pri temperaturah nad −47,5 °C. Pri −47,3 °C ima monoklinsko kristalno strukturo s prostorsko skupino C2/c in mrežnimi konstantami a = 2,03 Å, b = 1,16 Å, c = 1,99 Å in β = 111°. Pri izlitju v naravno okolje se zaradi gostote, večje od gostote vode, obravnava kot težka faza, ki se ne meša z vodo.
Uporaba
V preteklosti
V preteklosti se je ogljikov tetraklorid uporabljal za različne namene. Ko je postalo jasno, da škodljivo vpliva na zdravje, na primer da povzroča akutno odpoved jeter, so se namesto njega začeli uporabljati bolj varni proizvodi, na primer tetrakloroeten. Njegova poraba je začela padati že leta 1940, še vedno pa se je uporabljal kot pesticid za uničevanje žuželk v silosih za žito. Po letu 1970 so ga v ZDA že prepovedali.
Do podpisa Montrealskega sporazuma, ki je začel veljati 1. januarja 1989, se je še vedno uporabljal za proizvodnjo hladilnih sredstev R-11 (klorofluoroogljik) in R-12 (diklorodifluorometan), po tem datumu pa se je proizvodnja zaradi povzročanja ozonske luknje ustavila. Ogljikov tetraklorid se je uporabljal tudi za detekcijo nevtrinov.
Sedanja raba
Ogljkov tetraklorid je eden od najmočnejših strupov za jetra, zato se je na široko uporabljal za vrednotenje učinkov snovi za zaščito jeter.
Pri nizkih temperaturah je praktično nevnetljiv. Pri visokih temperaturah v zraku tvori strupen fosgen. V organski kemiji se uporablja kot vir klora.
Ker nima nobene vezi C-H, težko reagira v radikalskih reakcijah, zato je primerno topilo za halogeniranje ali z elementarnim klorom ali s halogenirajočinmi agensi, na primer bromosukcinimidom.
V raziskovalni organski sintezni kemiji se še uporablja kot topilo, zaradi škodljivega vpliva na zdravje pa se ga poskuša nadomestiti z drugimi bolj varnimi topili. Včasih se uporablja tudi kot topilo v infrardeči spektroskopiji, ker nima značilnih absorpcijskih črt pri valovnih dolžinah, večjih od 1600 cm-1. Ker nima nobenega vodikovega atoma, se je v preteklosti uporabljal v protonski jedrski magnetni resonančni spektroskopiji. Zaradi strupenosti in slabih topilnih lastnosti ga vedno bolj izpodrivajo devterirana topila. V analizah vsebnosti olj so ga zamenjala druga topila, na primer tetrakloroeten.
Varnost
Izpostavljenost visokim koncentracijam ogljikovega trtraklorida, tudi hlapom, lahko poškoduje osrednji živčni sistem, degenerira jetra in ledvica in po daljši izpostavljenosti povzroči nezavest in smrt. Stalna izpostavljenost lahko povzroči okvaro jeter in ledvic in celo raka.
Leta 2008 so naredili študijo običajnih gospodinjskih čistil in v njih odkrili "zelo visoke koncentracije" ogljikovega tetraklorida (do 110 mg/m3). V teh proizvodih je nastal zaradi dodajanje belila natrijevega hipoklorita v pralna sredstva in mila.
Ogljikov tetraklorid se je zaradi možnega depresivnega in/ali disociativnega vpliva na osrednji živčni sistem tudi zlorabljal z vdihavanjem. Takšna uporaba predstavlja resno tveganje za zdravje in lahko povzroči vse omenjene okvare.
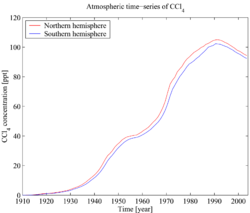
Ogljikov tetraklorid je tudi toplogredni plin in ena od snovi, ki tanjšajo ozonski plašč. Leta 1992< je njegova vsebnost v ozračju zaradi vseh naštetih ukrepov začela padati. Življenjska doba ogljikovega tetraklorida z zraku je 85 let.
Sklici
This article uses material from the Wikipedia Slovenščina article Ogljikov tetraklorid, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Vsebina je na voljo pod licenco CC BY-SA 4.0, razen če je navedeno drugače. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Slovenščina (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.