Azotni Oksidi
Pojam azotni oksidi se obično odnosi na binarna jedinjenja kiseonika i azota ili njihova jedinjenja:
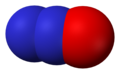
- Azot-monoksid (NO), azot(II) oksid
- Azot-dioksid (NO2), azot(IV) oksid
- Azot-suboksid (N2O), azot (I) oksid
- Azot-trioksid (N2O3), azot(II, IV) oksid, anhidrid azotaste kiseline.
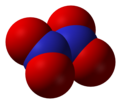
- Azot-tetroksid (N2O4), azot(IV) oksid
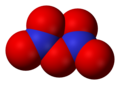
- Azot-pentoksid (N2O5), azot(V) oksid, anhidrid azotne kiseline
(Poslednja tri sa spiska su nestabilna jedinjenja.)
Hemijske reakcije koje dovode do nastanka azotnih oksida mogu proizvesti nekoliko različitih jedinjenja kiseonika i azota (različiti proporcionalni odnosi), u zavisnosti od uslova same reakcije. Ovo je jedan od razloga zašto su sporedni, nusproizvodi N2O nepoželjni; proizvodnja ostala dva stabilna oksida azota, koja su uzgred veoma otrovna, su zakonom regulisana.
-
Azot-monoksid, NO -
Azot-dioksid, NO2 -
Azot-suboksid, N2O -
Azot-trioksid, N2O3 -
Azot-tetroksid, N2O4 -
Azot-pentoksid, N2O5
NOx
NOx je uopštena forma za mono-azotne okside(NO i NO2). Ovi oksidi nastaju prilikom procesa sagorevanja, naročito prilikom procesa sagorevanja na visokim temperaturama.
Na normalnoj, ambijentalnoj, temperaturi kiseonik i azot ne reaguju međusobno. Prilikom rada motora sa unutrašnjim sagorevanjem, sagorevanje smeše vazduha i goriva proizvodi dovoljno visoku temperaturu da bi izazvalo endotermnu reakciju atmosferskog azota i kiseonika u plamenu. U gradovima gde je saobraćaj gust, količina azotnih oksida je primetna i može biti čak i štetna.
U prisustvu viška kiseonika (O2), Azot-monoksid (NO) će reagovati i nastaće Azot-dioksid (NO2), a vremenski period ove reakcije zavisi od same koncentracije u vazduhu, vidi se na tabeli:
| NO koncentracija u vazduhu (ppm) | Vreme potrebno da se polovina prisutnog NO oksiduje u NO2 (min) |
|---|---|
| 20,000 | 0.175 |
| 10,000 | 0.35 |
| 1,000 | 3.5 |
| 100 | 35 |
| 10 | 350 |
| 1 | 3500 |
Kada su NOx i neke od organskih isparljivih smeša (VOC) zajedno u vazduhu, i uz prisustvo sunčeve svetlosti, one formiraju fotohemijski smog, koji daje veliki udeo u zagađenju prirode. Pored zagađenja ove komponente i negativno utiču na čovekovo zdravlje.
1. Azot-dioksid, ako se rastvori u vlagi iz vazduha, formira komponentu (azotnu kiselinu) kisele kiše:
- 2NO2 + H2O → HNO2 + HNO3
(Azot-dioksid + voda → azotasta kiselina + azotna kiselina).
2. Zatim se azotasta kiselina razlaže:
- 3HNO2 → HNO3 + 2NO + H2O
(azotasta kiselina → azotna kiselina + azot-monoksid + voda),
3. Gde azot-monoksid reaguje sa kiseonikom, oksiduje, i formira azot-dioksid koji opet reaguje sa vodom i opet stvara azotnu kiselina:
- 4NO + 3O2 + 2H2O → 4HNO3
(azot-monoksid + kiseonik + voda → azotna kiselina).
Azot-monoksid takođe učestvuje u stvaranju ozona u troposferi.
Biogenetičko poreklo
U poljoprivredi fertilizacija i obogaćivanje zemljišta azotnim đubrivima takođe pripomaže obogaćivanju atmosferskih NOx, preko fertilizacije zemljišta pomoću mikroorganizmima koji pospešuju proces.
Izvori
Spoljašnje veze
This article uses material from the Wikipedia Srpskohrvatski / Српскохрватски article Azotni oksidi, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Sadržaj je dostupan pod CC BY-SA 4.0 osim ako je drugačije navedeno. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Srpskohrvatski / Српскохрватски (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.