Pentafluoruro Di Antimonio: Composto chimico
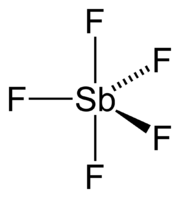
Il pentafluoruro di antimonio è il composto chimico con formula SbF5, dove l'antimonio ha numero di ossidazione +5.
In condizioni standard è un liquido incolore viscoso. È noto soprattutto per le sue caratteristiche di acido di Lewis, ma anche come ossidante e fluorurante. Viene utilizzato per la preparazione dell'acido fluoroantimonico, un superacido che è il più potente acido conosciuto.
| Pentafluoruro di antimonio | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| pentafluoruro di antimonio | |
| Nomi alternativi | |
| fluoruro di antimonio(V) fluoruro antimonico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | SbF5 |
| Massa molecolare (u) | 216,74 |
| Aspetto | liquido incolore oleoso igroscopico |
| Numero CAS | |
| Numero EINECS | 232-021-8 |
| PubChem | 24557 |
| SMILES | F[Sb](F)(F)(F)F |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,99 |
| Solubilità in acqua | reazione violenta |
| Temperatura di fusione | 281,4 (8,3 °C) |
| Temperatura di ebollizione | 422,7 (149,5 °C) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
   | |
| pericolo | |
| Frasi H | 301+311+331 - 314 - 411 - EUH014 |
| Consigli P | 260 - 264 - 273 - 280 - 305+351+338 - 310 |
Struttura

Il pentafluoruro di antimonio è un composto molecolare. Allo stato gassoso la molecola ha struttura a bipiramide trigonale, con simmetria D3h, in accordo con la teoria VSEPR. Allo stato liquido è molto viscoso, ed è formato da catene polimeriche di ottaedri SbF6 dove due dei fluoruri collegano due centri Sb vicini. Allo stato cristallino si formano tetrameri di formula [SbF3(μ-F)]4. Le distanze Sb–F nell'anello a otto termini Sb4F4 sono circa 202 pm; per gli altri fluoruri diretti all'esterno la distanza Sb–F è più corta, circa 182 pm. Negli altri elementi dello stesso gruppo, le specie pentafluoruro di fosforo (PF5) e pentafluoruro di arsenico (AsF5) sono monomeriche anche allo stato liquido e solido, probabilmente perché l'atomo centrale è più piccolo impedendo un aumento del numero di coordinazione. Il pentafluoruro di bismuto (BiF5) è un polimero.
Sintesi
Il pentafluoruro di antimonio fu preparato per la prima volta da Otto Ruff e Wilhelm Plato nel 1904, facendo reagire pentacloruro di antimonio con acido fluoridrico anidro:
Si può preparare anche da trifluoruro di antimonio e fluoro:
Reattività
Il pentafluoruro di antimonio è un composto estremamente reattivo, forte acido di Lewis ed energico fluorurante e ossidante.
Come acido di Lewis
Il pentafluoruro di antimonio è un accettore particolarmente forte di ioni fluoruro, formando l'anione esafluoroantimoniato, [SbF6]−, molto stabile. Si possono formare anche anioni di maggiori dimensioni, dato che [SbF6]− può ulteriormente reagire con il pentafluoruro di antimonio formando [Sb2F11]− e [Sb3F16]−. Ad esempio:
La formazione e la stabilità di [SbF6]− è alla base dell'utilizzo delpentafluoruro di antimonio per la generazione di superacidi. Miscele di perntafluoruro di antimonio e acido fluoridrico sono note come acido fluoroantimonico, il più forte superacido noto, in grado di protonare anche basi estremamente deboli come gli idrocarburi:
Un altro superacido, noto come acido magico, si ottiene con miscele di pentafluoruro di antimonio e acido fluorosulfonico:
Altre reazioni che evidenziano la tendenza ad accettare ioni fluoruro sono:
La grande affinità del pentafluoruro di antimonio per lo ione fluoruro ha permesso anche di realizzare la prima reazione chimica che porta alla formazione di fluoro elementare:
Come fluorurante e ossidante
Nella formazione di superacidi, l'acidità di Lewis del pentafluoruro di antimonio serve ad aumentare l'acidità di Brønsted dell'acido fluoridrico e acido fluorosolforico (HSO3F). Analogamente, il pentafluoruro di antimonio può servire ad aumentare il potere ossidante del fluoro per arrivare ad ossidare l'ossigeno:
Anche lo zolfo può essere ossidato con pentafluoruro di antimonio usando un solvente inerte come l'anidride solforosa (SO2):
Come fluorurante, il pentafluoruro di antimonio è spesso usato in miscela col pentacloruro di antimonio (SbCl5); in questo modo, ad esempio, dal cloruro di tionile (SOCl2) e dall'ossicloruro di fosforo (POCl3) si ottengono rispettivamente fluoruro di tionile (SOF2) e POFCl2.
Sicurezza
Il pentafluoruro di antimonio è un composto chimico pericoloso. È tossico per inalazione, ingestione e contatto. È fortemente corrosivo per la pelle e non è classificato come cancerogeno. È tossico per gli organismi acquatici e provoca danni a lungo termine per l'ambiente acquatico.
Note
Altri progetti
 Wiki Commons contiene immagini o altri file su Pentafluoruro di antimonio
Wiki Commons contiene immagini o altri file su Pentafluoruro di antimonio
This article uses material from the Wikipedia Italiano article Pentafluoruro di antimonio, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Il contenuto è disponibile in base alla licenza CC BY-SA 4.0, se non diversamente specificato. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Italiano (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.











