Oxid Železnato-Železitý: Chemická zlúčenina
Oxid železnato-železitý, (Fe3O4, FeO.Fe2O3) je podvojný oxid železa.
V prírode sa vyskytuje ako minerál, magnetit. Je ferimagnetický do teploty 570 °C, nad túto teplotu sa stáva paramagnetickým.
| Oxid železnato-železitý | |||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||
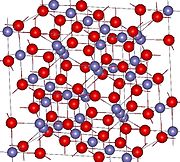 | |||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||
| Sumárny vzorec | FeO ∙ Fe2O3 (Fe3O4) | ||||||||||||||||||||||||||||||||
| Synonymá | magnetit | ||||||||||||||||||||||||||||||||
| Vzhľad | Čierna feromagnetická prášková látka | ||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 231,5 u | ||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 231,531 g/mol | ||||||||||||||||||||||||||||||||
| Teplota rozkladu | 1 595 °C | ||||||||||||||||||||||||||||||||
| Hustota | 5,195 g/cm3 (20 °C) | ||||||||||||||||||||||||||||||||
| Rozpustnosť | nerozpustný vo vode | ||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||
| Entropia topenia | 576 J/g | ||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | -1 118 kJ/mol | ||||||||||||||||||||||||||||||||
| Štandardná entropia | 146 J K-1 mol-1 | ||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | -1 015 kJ/mol | ||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 0,619 J K-1 g-1 | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||
| Číslo CAS | 1317-61-9 | ||||||||||||||||||||||||||||||||
| EINECS číslo | 215-277-5 | ||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||

Používa sa na výrobu železa vo vysokej peci. V hornej časti pece sa pridavajú železné rudy (napr. magnetit a hematit) spolu s vápencom a koksom. Reakcia koksu so vzdušným kyslíkom, ktorý je do pece vháňaný v dolnej časti, vzniká oxid uhoľnatý, pomocou ktorého prebieha nepriama redukcia rúd. Vzniknutý oxid železnatý klesá do nižšej časti vysokej pece, kde je redukovaný pomocou koksu na železo. Vznikajúci oxid uhličitý reaguje s koksom za vzniku 2 molekúl oxidu uhoľnatého, ktorý ďalej redukuje rudy železa.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Oxid železnato-železitý na českej Wikipédii.
This article uses material from the Wikipedia Slovenčina article Oxid železnato-železitý, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Obsah je dostupný pod licenciou CC BY-SA 4.0, pokiaľ nie je uvedené inak. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Slovenčina (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.


