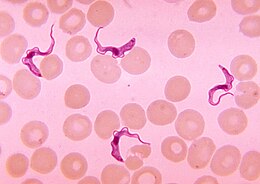
Maladie Du Sommeil: Maladie parasitaire provoquée par un trypanosome
Ne doit pas être confondu avec Trypanosomiase animale africaine.
| Causes | Trypanosoma brucei, Trypanosoma gambiense (d) ou Trypanosoma brucei rhodesiense (d) |
|---|---|
| Transmission | Transmission vectorielle (d) |
| Incubation min | 7 j |
| Incubation max | 22 j |
| Symptômes | Signe de Winterbottom (en), fièvre périodique (d), céphalée, malaise (en), anémie, arthralgie, trouble du sommeil, étourdissement, foyer d'infection primaire (d), tachycardie, tuméfaction, cachexie et sopor (en) |
| Médicament | (RS)-éflornithine, Nifurtimox, suramine, pentamidine et Mélarsoprol |
|---|---|
| Spécialité | Infectiologie |
| CIM-10 | B56 |
|---|---|
| CIM-9 | 086.5 |
| DiseasesDB | 29277 13400 |
| MedlinePlus | 001362 |
| eMedicine | 228613 |
| MeSH | D014353 |
| Patient UK | African-trypanosomiasis |
La trypanosomiase humaine africaine, couramment appelée maladie du sommeil, est une forme de trypanosomiase, une maladie parasitaire provoquée par un trypanosome, qui est transmis par la piqûre de la mouche tsé-tsé. Deux sous-espèces de Trypanosoma bruceiengendrent des pathologies différentes : Trypanosoma brucei ssp. gambiense (Afrique de l'Ouest) et Trypanosoma brucei ssp. rhodensiense (Afrique de l'Est). La maladie du sommeil fait partie des 20 maladies tropicales négligées listées par l'OMS. Le nagana est la trypanosomiase provoquée par les Trypanosoma brucei chez les mammifères non humains.
La maladie est endémique dans certaines régions de l’Afrique subsaharienne, couvrant environ 36 pays et menaçant 60 millions de personnes. Entre 2017 et 2022, l'OMS estime que moins de 1 000 individus sont infectés par an.
Trois épidémies majeures se sont produites ces cent dernières années, une en 1896-1906 (qui aurait tué environ un million de personnes dans le bassin du Congo) et les deux autres en 1920 et 1970.
Mode de transmission
Cette maladie se transmet surtout par la piqûre par une mouche tsé-tsé infectée. Elle peut aussi être transmise par d'autres insectes hématophages, bien que ce soit plus rare. Elle se transmet aussi de la mère à l'enfant en traversant la barrière placentaire pour infecter le fœtus. Elle est alors un facteur de risque de mort périnatale. Des infections accidentelles dans les laboratoires existe, en cas de mauvaise manipulation du sang d'une personne infectée. Avoir des rapports sexuels non protégés avec une personne atteinte pourrait la transmettre mais les cas avérés sont anecdotiques.
Symptômes

Lors du premier stade, la maladie se manifeste par des symptômes peu spécifiques, dont la fièvre intermittente, des céphalées, la fatigue, l'arthralgie, l'adénopathie et des démangeaisons. L'adénopathie postérieure cervicale, appelée le signe de Winterbottom (en) est parfois observé. Alors que le parasite envahit de nouveaux organes, des symptômes supplémentaires apparaissent, dont l'anémie hémolytique, une hépatomégalie avec un fonctionnement du foie altéré, une splénomégalie, des troubles du système endocrinien, une péricardite et l'arrêt cardiorespiratoire ainsi que des troubles ophtalmologiques. Les symptômes sont différents chez les patients qui ne viennent pas d'une zone où la maladie du sommeil est endémique, avec des diarrhées et l'ictère. Un trypanome, c'est-à-dire une tuméfaction au niveau du point d'inoculation, est observé dans un cas sur cinq chez les patients atteints de la forme rhodésienne de la maladie.
Une fois que le parasite atteint le système nerveux central, la maladie entre dans son second stade, avec des symptômes plus évidents : une irritabilité, fatigue, des changements de comportement, des troubles de la vision dont la diplopie, une perte de coordination, des mouvements involontaires, des tremblements, une difficulté à s'exprimer et une perturbation du rythme circadien provoquant des somnolences et des insomnies. Les patients sont ensuite atteints d'incontinence urinaire, des convulsions, un état de conscience altérés, et généralement, le coma puis la mort,.
La durée de la maladie varie selon le parasite en cause. L'évolution est plus rapide dans le cas du Trypanosomia rhodesiense (sur quelques semaines à quelques mois). Elle peut atteindre plusieurs années dans le cas du Trypanosomia gambiense.
Une atteinte cardiaque peut se voir dans la forme gambienne, essentiellement à type d'anomalie sur l'électrocardiogramme sans conséquence. Cette atteinte reste au second plan, contrairement à la forme américaine de la trypanosomiase (maladie de Chagas). La forme gambienne peut être également totalement asymptomatique.
Distribution géographique et épidémiologique

La maladie se rencontre sous deux formes, selon le parasite en cause, Trypanosoma brucei gambiense ou Trypanosoma brucei rhodesiense.
En 2023, Trypanosoma brucei gambiense se trouve dans 24 pays d'Afrique de l'ouest et d'Afrique centrale. Il est responsable de 92 % des cas de trypanosomiase humaine africaine. Trypanosoma brucei rhodesiense se trouve dans 13 pays différents d'Afrique de l'est et du sud et est responsable des 8 % des cas restants.
Entre 2018 et 2022, l'OMS estime que le nombre de cas de trypanosomiase humaine africaine est en dessous de 1 000 par an. Entre 2003 et 2023, le nombre de nouveaux cas à chuté de 97 %.
En 2011, un rapport du CDC prévoit qu'au rythme du réchauffement climatique actuel, certaines régions tempérées pourraient devenir des zones à risque de contamination ; si en 2011 75 millions de personnes vivent dans des zones à risque, ils évaluent qu'en 2090, ce sont 40 à 77 millions d'individus en plus qui seront exposés au risque de transmission de la maladie.
Les humains sont le réservoir principal pour Trypanosoma brucei gambiense, mais les réservoirs principaux pour Trypanosoma brucei rhodesiense sont les animaux sauvages et domestiques. La trypanosomiase animale provoquée par les Trypanosoma brucei s'appelle le Nagana.
C'est une maladie vectorielle provoquée par la piqûre de la mouche tsé-tsé et peut-être d'autres mouches hématophages.
Cycle parasitaire
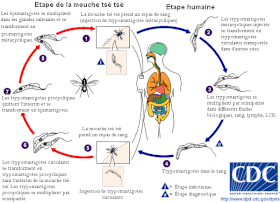
La mouche tsé-tsé est grande, brune et furtive. La piqûre est ressentie comme une aiguille chaude enfoncée dans la chair. Pendant un repas de sang sur le mammifère hôte, une mouche tsé-tsé infectée (du genre Glossina) injecte les trypomastigotes métacycliques dans le tissu cutané. Les parasites entrent dans le système lymphatique et passent dans la circulation sanguine (1). À l'intérieur de l’hôte, ils se transforment en trypomastigotes circulants dans le sang (2) et sont transportés à d'autres emplacements dans tout le corps, atteignent d'autres fluides biologiques (par exemple, lymphe, liquide cérébrospinal), et continuent de se répliquer par scissiparité (3). Le cycle parasitaire du Trypanosome africain est représenté par des étapes extracellulaires. Une mouche tsé-tsé s’infecte par des trypomastigotes circulants en prenant un repas de sang sur un mammifère infecté hôte (4)(5). Dans l’intestin de la mouche, les parasites se transforment en trypomastigotes procycliques, se multiplient par scissiparité (6), quittent l’intestin, et se transforment en épimastigotes (7). Les épimastigotes atteignent les glandes salivaires de la mouche et continuent leur multiplication par scissiparité (8). Le cycle dans la mouche dure approximativement 3 semaines.
Diagnostic de laboratoire
Le diagnostic repose sur la mise en évidence des trypanosomes par l'examen au microscope du fluide d’un chancre, du liquide de ponction d’un ganglion, de sang, de moelle osseuse, ou, aux dernières étapes de l'infection, du liquide cérébrospinal prélevé par ponction lombaire. Les trypanosomes mobiles sont recherchés sur une préparation humide et en outre une préparation est fixée et colorée avec la méthode de Giemsa. Des techniques de concentration peuvent être utilisées avant l'examen au microscope. Pour des échantillons de sang, la centrifugation est utilisée, pour d'autres échantillons, tels que le liquide cérébrospinal, les techniques de concentration comprennent la centrifugation suivie de l'examen du sédiment. L'isolement du parasite par l'inoculation au rat ou à la souris est une méthode sensible, mais son utilisation est limitée au T.B. rhodesiense. La détection d'anticorps a une sensibilité et une spécificité qui sont trop variables pour en tirer des conclusions cliniques. En outre, dans les infections avec le T.B. rhodesiense, la séroconversion se produit après le début des symptômes cliniques et présente donc un intérêt limité.
Trois tests sérologiques semblables sont disponibles pour la détection du parasite gambien : le micro-CATT, le wb-CATT, et le wb-LATEX. Le premier utilise le sang coagulé tandis que les autres utilisent des échantillons de sang entier. Ces tests consistent à faire réagir une goutte de sang sur un réactif sur carte. Ils sont simples à mettre en œuvre et constituent un moyen de dépistage efficace. La sérologie est, par contre, peu utile dans les formes rhodésiennes, le diagnostic parasitologique devant être privilégié et étant plus facile, du fait d'une plus grande concentration en parasites.
Dans les formes neurologiques, la ponction lombaire montre, outre le parasite, une augmentation du taux de protéines ainsi que la présence de globules blancs.
Traitement
Pour T. b. gambiense
Le traitement recommandé par l'OMS pour le premier stade de la maladie est la pentamidine en intramusculaire. Le fexinidazole est aussi utilisé. Pour le second stade de la maladie, elle recommande plutôt l'éflornithine intraveineuse, généralement accompagnée de nifurtimox.
Pour T. b. rhodesiense
Le traitement recommandé par l'OMS pour le premier stade de la maladie est la suramine en intraveineuse, à surveiller à cause des risques d'allergie. Pour le second stade, elle recommande le mélarsoprol.
Suivi
Tous les patients devraient être suivis pendant deux années avec des ponctions lombaires semestrielles pour détecter les rechutes.
Histoire du traitement
Dès le début du XXe siècle, l'Institut Pasteur de Paris entame des démarches afin de comprendre le développement de la maladie mortelle. Pour cela, le centre de recherche envoie des spécialistes médicaux au sein des colonies françaises afin d'effectuer une évaluation de la maladie. Le biologiste Émile Roubaud, faisant partie de ces déploiements, mène ses recherches sur le territoire colonial français. Le scientifique effectue notamment des recherches sur la cause de transmission, soit les glossines, plus connus sous le nom de mouche tsé-tsé.
Dans le rapport de la mision d'étude de la maladie du sommeil du Congo français 1906-1908, les médecins tentent de comprendre le développement de la maladie dès les premiers symptômes. Ils débutent donc par effectuer des travaux sur le sang des victimes.
En 1910, l’année même de la découverte de Bruce, est introduit le premier médicament actif contre la maladie du sommeil, le Salvarsan (arsphénamine), mis au point par Paul Ehrlich et Sahachiro Hata. Cependant, l’emploi de ce dérivé de l’arsenic présente des risques graves, dont la cécité. Jointe à une toxicité qui le rend peu maniable, l’efficacité du Salvarsan incite à poursuivre les recherches en direction des dérivés de l’arsenic, et d'autres molécules seront obtenues par dérivation de l'acide aminophénolarsinieux : la tryparsamide (it) et le mélarsen, acides arsiniques, à noyau d'arsenic pentavalent ; l'arséno-phénylglycine, le melarsen-oxyde et le melarsoprol, oxydes d'acides arsiniques, à noyau trivalent.
Il faut pourtant attendre jusqu’en 1919 pour qu’aboutissent les travaux de Walter Jacobs et Michael Heidelberger, qui permettront à Wade Brown et Louise Pearce d’introduire la tryparsamide. Dès lors, trois trypanocides apparus au cours des années 1920, la suramine (non-arsenical), l’orsanine et la tryparsamide, sont employés dans de vastes campagnes de dépistage et de traitement de masse. La suramine (Bayer 205), synthétisée en 1917, mais dont la formule, tenue secrète, n'est élucidée par Ernest Fourneau qu'en 1924 à l'Institut Pasteur, est introduite dès 1920. Elle est utilisée au premier stade de la maladie ou en cas d'arséno-résistance. Son administration par voie intraveineuse et à des doses élevées en limite l’emploi. Cependant, et malgré son importante toxicité, elle est encore en usage en 2001 dans la phase lymphatico-sanguine. La tryparsamide (it), dérivée de l'atoxyl, est introduite en 1921 et commercialisée en 1930 sous le nom de Tryponarsil. C’est le premier médicament actif sur la phase cérébrospinale. Cependant, même réduite par une posologie progressive, sa toxicité oculaire touche 2 % des malades traités au cours de la campagne menée par Jean Laigret en République du Congo au milieu des années 1920, et 4,4 % de ceux traités par Eugène Jamot au Cameroun à la même époque. Et chez les patients administrés à un stade avancé, le taux de létalité iatrogène s’élève à 6,6 %. Dans l'ouvrage Essaie de traitement de la maladie du sommeil, au Cameroun, par le Bayer 205 rédigée par Jamot lui-même explique : " [n]ous nous basions, en l'absence de données exactes, sur l'âge que nous étions obligés d'évaluer approximativement d'après l'aspect général. C'est ainsi qu'un garçon de 12 ans, bien développé, a reçu 3 grammes en tout, comme un adulte et n'en a été, en aucune façon, incommodé." Les doses administrées sont donc parfois trop concentrées pour l'âge ou pour le sexe du malade, la cause de l'aveuglement de plusieurs camerounais. Au total, environ 700 camerounais sont atteints de cécité à la suite d'une vaccination. L'orsanine sodique (Fourneau 270) est employée à partir de 1925 et pendant une quinzaine d'années,,, soit seule chez les patients « en période douteuse », soit en association avec la tryparsamide chez les malades au stade second.
Dès le début des années 1930, au Congo belge, apparaissent les premiers cas d’arséno-résistance et, à partir de 1934, la tryparsamide est associée à d'autres molécules, dont la suramine et l'orsanine sodique.
L’orsanine est abandonnée à la découverte, en 1939, de la pentamidine, molécule très efficace dans la première phase de la maladie, couramment employée en Afrique occidentale comme agent prophylactique, et qui permet pendant les années 1950 une diminution des taux d'infection si importante qu'on[Qui ?] croit possible l'éradication de la maladie. La suramine quant à elle, généralement associée à la tryparsamide, reste le médicament le plus employé dans le traitement de la maladie du sommeil jusqu’à la fin des années 1960, progressivement remplacée à partir de 1949 par le mélarsoprol, mis au point par Friedheim et qui présente une toxicité moins élevée que tous les arsenicaux employés jusqu’alors.
L’éflornithine enfin (difluoromethylornithine ou DFMO), le traitement le plus moderne, a été mise au point dans les années 1970 par Albert Sjoerdsmanot et elle a fait l’objet d’essais cliniques dans les années 1980. La molécule a été autorisée aux États-Unis par la Food and Drug Administration en 1990, mais Aventis, le laboratoire pharmaceutique responsable de sa fabrication, a cessé la production en 1999. En 2001, cependant, Aventis, en association avec Médecins sans frontières et l'Organisation mondiale de la santé, a signé un accord à long terme pour fabriquer et distribuer le médicament. Son efficacité est démontrée, sa tolérance est meilleure que celle du mélarsoprol. Il existe cependant, des rechutes sous ce traitement, dans un peu moins de 10 % de cas, mais le plus souvent mortelles. Le fexinidazole pourrait constituer une alternative à ce traitement.
Des traitements combinés pourraient réduire ce risque de rechute, parmi lesquels l'association eflornithine - nifurtimox semble particulièrement prometteuse.
Le Megazol, molécule biologiquement active avec une activité trypanocide, a fait l'objet il y a quelques années d'études scientifiques. En effet cette molécule, active sous forme de pilule (voie orale) permet d'éliminer 100 % du parasite en deux jours (tests in vitro et in vivo chez le chimpanzé et le cochon). Cette molécule est cependant suspectée d'être cancérigène et son développement a été arrêté.
Perspectives et voies de recherche
Le génome du parasite a été décodé et plusieurs protéines ont été identifiées comme cibles potentielles pour un traitement médicamenteux. Le décodage de l'ADN a également permis de comprendre pourquoi la production d'un vaccin pour cette maladie a été si difficile. T brucei a plus de 800 gènes qui fabriquent des protéines qu’il utilise pour éviter la détection par le système immunitaire. (Berriman, et autres. , 2005)
Une équipe de recherche internationale travaillant en République démocratique du Congo, au Soudan et en Angola impliquant Immtech international et l’université de la Caroline du Nord à Chapel Hill a mené les essais cliniques en phase I et commencé un essai en phase III en 2005 pour tester l'efficacité du premier traitement par voie orale de la maladie de sommeil, connu pour le moment sous le nom de « DB289 »,.
Des résultats récents indiquent que le parasite ne peut pas survivre dans la circulation sanguine sans son flagelle. Cette découverte donne aux chercheurs un nouvel angle d’attaque pour éliminer le parasite.
Des chercheurs ont trouvé un mécanisme immunitaire qu'ils pensent utiliser pour créer de nouveaux traitements. Une protéine Hpr (haptoglobinrelated protein) découverte en 2006 et liée à des lipides du système sanguin peut capturer l'hémoglobine et la transporter vers le corps gras auxquels elles sont liées, qui contient une toxine fatale au trypanosome. Ce mécanisme pourrait être une solution immunitaire utilisant la dépendance des trypanosomes à l'hémoglobine. Lorsque cette dernière a préalablement été capturée par une protéine Hpr, les trypanosomes s'y fixent aussi à la particule graisseuse qui empoisonne alors le parasite.
En 2022, le développement de l'acoziborole laisse espérer une maitrise de la maladie. Le traitement, qui consiste en une seule prise orale du médicament, fonctionne pour les deux stades de la maladie, ce qui évite de devoir réaliser des ponctions lombaires pour identifier à quel stade se trouve le patient. Cette facilité d'accès au traitement permet d'envisager une éradication de la transmission de la maladie. Une étude publiée en novembre 2022 indique une efficacité de 95%. Mais elle a été réalisée sans groupe de contrôle. Une autre étude avec un groupe recevant un placebo est lancée. Le Monde signale aussi une étude comportant 1 200 personnes lancée en 2022 pour vérifier l'innocuité de l'acoziborole.
Prévention et contrôle
Il n'existe pas de vaccin ni de prévention médicamenteuse. La prévention et le contrôle se focalisent, là où c’est possible, sur l'extirpation de l'hôte parasite, la mouche tsé-tsé. Deux stratégies ont été employées alternativement dans les tentatives pour réduire les trypanosomiases africaines. L'une des tactiques est principalement médicale ou vétérinaire et vise directement la maladie en utilisant la prophylaxie, le traitement, et la surveillance pour réduire le nombre d'organismes porteurs de la maladie. La deuxième stratégie est généralement entomologique et prévoit de perturber le cycle de transmission en réduisant le nombre de mouches.
Il existe des exemples de réduction de la maladie du sommeil par l'utilisation de techniques de stérilisation des insectes. La surveillance active régulière, impliquant la détection et le traitement des cas, en plus du contrôle des mouches de tsé-tsé, est l'épine dorsale de la stratégie pour le contrôle de la maladie du sommeil. Le dépistage systématique dans les communautés où des foyers ont été identifiés est la meilleure approche, car le dépistage au cas par cas n'est pas possible en pratique dans les zones de forte endémie. Le dépistage systématique peut se faire sous forme de cliniques mobiles ou de centres fixes de dépistages où les équipes voyagent quotidiennement dans les foyers. La nature de la maladie de gambiense est telle que les patients ne cherchent pas à se faire soigner assez tôt parce que les symptômes à cette phase ne sont pas évidents ou assez sérieux pour justifier une consultation médicale, en raison de l'éloignement des quelques secteurs affectés. En outre, le diagnostic de la maladie est difficile et la plupart des personnels sanitaires ne sont pas capable de la détecter. Le dépistage systématique permet à la maladie débutante d'être détectée et traitée avant que la maladie progresse, et diminue le réservoir humain.
Pour le voyageur, le port de vêtements couvrants ainsi que de répulsifs contre la mouche responsable est conseillé.
Histoire et épidémiologie
En Afrique, la présence de la maladie du sommeil est attestée depuis le XIVe siècle.
Ce n'est pourtant qu'au début du XXe siècle, en 1901 et 1903, que Sir David Bruce découvre et confirme l’agent parasitaire de cette affection, auquel il laisse son nom : le trypanosome de Bruce (Trypanosoma brucei), et en 1910 qu'il identifie avec précision son insecte vecteur, la mouche Glossina palpalis
Il y a eu trois épidémies graves en Afrique au cours du dernier siècle. La première, entre 1896 et 1906, atteint surtout l’Ouganda et le bassin du Congo.
Une épidémie majeure a lieu après le début de la colonisation au passage du XXe siècle, tuant probablement environ un million de personnes dans le bassin du Congo, contribuant à dépeupler les pays du bassin d'Afrique ; il est d'ailleurs probable que les déplacements accrus et souvent forcés dans ce bassin, la promiscuité entre enfants rassemblés dans les écoles, entre les porteurs de tribus et horizons différentes, volontaires ou recrutés de force. Une Assistance médicale indigène et des groupes sanitaires mobiles sont mis en place par l'administration coloniale pour toutes ses colonies, dont au Maroc, et en Algérie, en Afrique-Occidentale française dont au Cameroun, rapidement confiée aux médecins militaires.
Une deuxième épidémie sévit à partir de 1920 dans plusieurs pays africains. Elle est arrêtée par des équipes mobiles qui examinent systématiquement des millions de personnes en danger. La maladie ayant presque disparu entre 1960 et 1965, le dépistage et la surveillance se relâchent après le départ des autorités coloniales et, en 1970, éclate la troisième grande épidémie.
Depuis, la maladie n'a cessé de progresser sous forme endémique dans plusieurs foyers.
Divers
De 1951 à 1953, alors que d'importants progrès sont faits par la pharmacologie et dans la connaissance des psychoses, le professeur Pierre Gallais, responsable du service de psychiatrie de l'hôpital Lévy à Marseille, expérimente une méthode thérapeutique inspirée de la malariathérapie, qu'il nomme trypanothérapie, et fait des essais pharmacologiques directement chez 12 patients durant deux ans, estimant que « la phase nerveuse de la maladie pourrait être un moment salutaire pour les patients psychotiques et schizophrènes, en échec thérapeutique, accueillis dans son service »
La molécule sécrétée par le parasite responsable des retentissements symptomatiques sur l'état de veille est le tryptophol.
Notes et références
Annexes
Bibliographie
- Gaëlle Ollivier et Dominique Legros, « Historique de la trypanosomiase humaine africaine », Tropical Medecine International Health, vol. 6, no 11, , p. 855-863 (lire en ligne)
- (en) M.P. Barrett et al., « The trypanosomiases », Lancet, vol. 362, no 9394, , p. 1469-80 (PMID 14602444, lire en ligne)
- (en) M. Berriman et al., « The genome of the African trypanosome Trypanosoma brucei », Science, vol. 309, no 5733, , p. 416–22 (PMID 16020726, lire en ligne)
Articles connexes
- Mouche tsé-tsé
- Liste des maladies infectieuses
- Maladie de Chagas, autre maladie humaine provoquée par le Trypanosome
- DNDi (Drugs for Neglected Diseases Initiative)
- Épidémie de maladie du sommeil dans le bassin du Congo
Liens externes
- Doctors Without Borders/Medecins Sans Frontieres Sleeping sickness information page
- Institut de recherche pour le développement
- OMS "Trypanosomiase humaine africaine (maladie du sommeil)" dernière mise à jour , http://www.who.int/mediacentre/factsheets/fs259/fr/
This article uses material from the Wikipedia Français article Maladie du sommeil, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Le contenu est disponible sous licence CC BY-SA 4.0 sauf mention contraire. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Français (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.