Yếu Tố Hoại Tử Khối U Alpha
Yếu tố hoại tử khối u là các chất thuộc nhóm xitôkin được tiết ra bởi đại thực bào trong cơ thể, có khả năng tiêu huỷ nhiều tế bào của một số loại khối u.
Tên này dịch từ nguyên gốc tiếng Anh: "Tumor Necrosis Factors" (viết tắt là TNF) dùng để chỉ một loại prôtêin đóng vai trò tín hiệu tế bào liên quan đến viêm toàn thân và tạo nên phản ứng giai đoạn cấp tính. Hai chất đầu tiên của họ TNF đã được xác định là: TNF anpha (yếu tố hoại tử khối u alpha viết tắt TNFa, cũng gọi là cachexin hoặc cachectin) và TNF bêta (còn được gọi là Lymphotoxin-alpha) một loại xitôkin bị ức chế bởi interleukin10. Các TNF liên quan đến ung thư và đã được sử dụng để điều trị có hiệu quả một số bệnh ung thư.
TNF được sản xuất chủ yếu bởi các đại thực bào được kích hoạt, mặc dù nó có thể được sản xuất bởi nhiều loại tế bào khác như tế bào lympho CD4 +, tế bào NK, bạch cầu trung tính, tế bào mast, bạch cầu ái toan và tế bào thần kinh. TNFα là một thành viên của siêu họ TNF, bao gồm các protein xuyên màng khác nhau với miền TNF tương đồng.
Vai trò chính của TNF là trong việc điều hòa các tế bào miễn dịch. TNF, là một pyrogen nội sinh, có thể gây sốt, chết tế bào apoptotic, suy nhược, viêm và ức chế sự hình thành khối u và sao chép virus và đáp ứng với nhiễm trùng huyết thông qua các tế bào sản xuất IL1 & IL6. Rối loạn sản xuất TNF có liên quan đến nhiều loại bệnh ở người bao gồm bệnh Alzheimer, ung thư, trầm cảm lớn, bệnh vẩy nến và bệnh viêm ruột (IBD). Mặc dù còn nhiều tranh cãi, các nghiên cứu về trầm cảm và IBD hiện đang được liên kết với mức độ tăng của TNFα. TNF tái tổ hợp được sử dụng như một chất kích thích miễn dịch dưới INN tasonermin. TNF có thể được sản xuất ngoài tử cung trong bối cảnh ác tính và tương tự hormone tuyến cận giáp cả trong việc gây tăng calci máu thứ phát và trong các bệnh ung thư có sản xuất quá mức có liên quan.
Khám phá Yếu Tố Hoại Tử Khối U Alpha
Lý thuyết về phản ứng chống ung thư của hệ thống miễn dịch in vivo đã được công nhận bởi bác sĩ William B. Coley. Năm 1968, Gale A Granger từ Đại học California, Irvine, đã báo cáo một yếu tố gây độc tế bào được sản xuất bởi các tế bào lympho và đặt tên là lymphotoxin (LT). Tín dụng cho khám phá này được chia sẻ bởi Nancy H. Ruddle từ Đại học Yale, người đã báo cáo hoạt động tương tự trong một loạt các bài báo trở lại được xuất bản trong cùng tháng. Sau đó, vào năm 1975 Lloyd J. Old từ Trung tâm Ung thư Tưởng niệm Sloan-Kettering, New York, đã báo cáo một yếu tố gây độc tế bào khác do đại thực bào sản xuất và đặt tên là yếu tố hoại tử khối u (TNF). Cả hai yếu tố này đã được mô tả dựa trên khả năng của họ để giết chuột fibrosarcoma tế bào L-929. Những khái niệm này đã được mở rộng sang bệnh hệ thống vào năm 1981, khi Ian A. Clark, từ Đại học Quốc gia Úc, hợp tác với Elizabeth Carswell trong nhóm Old, làm việc với dữ liệu thời kỳ tiền giải trình tự, lý do rằng sản xuất quá nhiều TNF gây ra bệnh sốt rét và nội độc tố ngộ độc.
Các cDNA mã hóa LT và TNF đã được nhân bản vào năm 1984 và được tiết lộ là tương tự nhau. Sự ràng buộc của TNF với thụ thể của nó và sự dịch chuyển của nó bằng LT đã xác nhận sự tương đồng chức năng giữa hai yếu tố. Sự tương đồng tuần tự và chức năng của TNF và LT đã dẫn đến việc đổi tên TNF thành TNFα (bài viết này) và LT là TNFβ. Năm 1985, Bruce A. Beutler và Anthony Cerami đã phát hiện ra rằng cacheectin (một loại hormone gây ra chứng sợ hãi) thực sự là TNF. Sau đó, họ xác định TNF là chất trung gian gây ngộ độc nội độc tố gây chết người. Kevin J. Tracey và Cerami đã phát hiện ra vai trò trung gian chính của TNF trong sốc nhiễm trùng gây chết người và xác định tác dụng điều trị của kháng thể kháng TNF đơn dòng. Gần đây, nghiên cứu trong Phòng thí nghiệm của Mark Mattson đã chỉ ra rằng TNF có thể ngăn ngừa tử vong / apoptosis của các tế bào thần kinh bằng một cơ chế liên quan đến việc kích hoạt yếu tố phiên mã NF-kappaB, tạo ra biểu hiện của Mn-SOD và Bcl-2.[cần dẫn nguồn]
Gen
Gen TNF của người (TNFA) đã được nhân bản vào năm 1985. Nó ánh xạ tới nhiễm sắc thể 6p 21.3, kéo dài khoảng 3 kilobase và chứa 4 exon. Exon cuối cùng có sự tương đồng với lymphotoxin alpha (LTA, còn được gọi là TNF-). 3 'UTR của TNFa chứa phần tử giàu AU (IS).
Kết cấu Yếu Tố Hoại Tử Khối U Alpha
TNF chủ yếu được sản xuất dưới dạng protein xuyên màng loại II dài 233 amino acid được sắp xếp trong các homotrim ổn định. Từ dạng tích hợp màng này, cytokine hòa tan đồng nhất (sTNF) được giải phóng thông qua sự phân tách protein bởi enzyme chuyển đổi TNF alpha của metallicoprotease (TACE, còn được gọi là ADAM17). STNF trimeric 51 kDa hòa tan có xu hướng phân ly ở nồng độ dưới phạm vi nano, do đó mất hoạt tính sinh học. Dạng TNFa được tiết ra của con người có hình dạng kim tự tháp hình tam giác, và nặng khoảng 17 kDa. Cả hai dạng tiết và màng liên kết đều hoạt động về mặt sinh học, mặc dù các chức năng cụ thể của từng loại đang gây tranh cãi. Nhưng, cả hai hình thức có hoạt động sinh học chồng chéo và khác biệt.
Chuột nhà chung TNFa và TNF của con người có cấu trúc khác nhau. Các 17- kilodalton (kDa) protomers TNF (185-amino acid-dài) được tạo thành từ hai tờ β-pleated phản song song với chuỗi β phản song song, tạo thành một 'roll thạch' β-cấu trúc, đặc trưng cho gia đình TNF, mà còn tìm thấy trong protein capsid của virus.
Tín hiệu tế bào Yếu Tố Hoại Tử Khối U Alpha
TNF có thể liên kết hai thụ thể, TNFR1 (thụ thể TNF loại 1; CD120a; p55 / 60) và TNFR2 (thụ thể TNF loại 2; CD120b; p75 / 80). TNFR1 là 55-kDa và TNFR2 là 75-kDa. TNFR1 được biểu hiện ở hầu hết các mô và có thể được kích hoạt hoàn toàn bằng cả hai dạng TNF gắn màng và hòa tan trong màng, trong khi TNFR2 thường được tìm thấy trong các tế bào của hệ thống miễn dịch và phản ứng với dạng đồng nhất của màng tế bào TNF. Vì hầu hết các thông tin liên quan đến tín hiệu TNF có nguồn gốc từ TNFR1, vai trò của TNFR2 có thể bị đánh giá thấp.
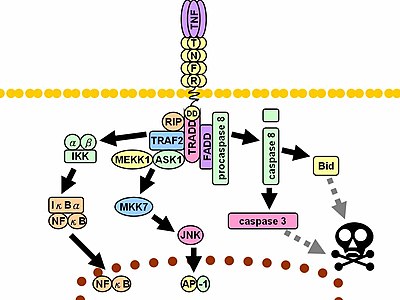
Khi tiếp xúc với phối tử của chúng, các thụ thể TNF cũng tạo thành các tông đơ, các đầu của chúng khớp với các rãnh được hình thành giữa các đơn phân TNF. Sự gắn kết này gây ra một sự thay đổi về hình dạng xảy ra trong thụ thể, dẫn đến sự phân ly của protein ức chế SODD từ miền chết nội bào. Sự phân ly này cho phép protein bộ điều hợp TradD liên kết với miền chết, đóng vai trò là nền tảng cho liên kết protein tiếp theo. Theo ràng buộc TradD, ba con đường có thể được bắt đầu.
- Kích hoạt NF- B: TradD tuyển dụng TRAF2 và RIP. TRAF2 lần lượt tuyển dụng protein kinase đa thành phần IKK, cho phép RIP serine-threonine kinase để kích hoạt nó. Một protein ức chế, IκBa, thường liên kết với NF-κB và ức chế sự chuyển vị của nó, bị phosphoryl hóa bởi IKK và sau đó bị thoái hóa, giải phóng ra NF-B. NF-B là một yếu tố phiên mã dị thể chuyển vào nhân và làm trung gian cho quá trình phiên mã của một loạt các protein liên quan đến sự sống và tăng sinh của tế bào, phản ứng viêm và các yếu tố chống apoptotic.
- Kích hoạt các con đường MAPK: Trong ba tầng chính của MAPK, TNF tạo ra sự kích hoạt mạnh mẽ của nhóm JNK liên quan đến căng thẳng, gợi lên phản ứng vừa phải của p38-MAPK và chịu trách nhiệm kích hoạt tối thiểu ERK cổ điển. TRAF2 / Rac kích hoạt các kinase ngược dòng của JNK của MLK2 / MLK3, TAK1, MEKK1 và ASK1 (trực tiếp hoặc thông qua GCKs và Trx, tương ứng). SRC- Vav- Trục Rac kích hoạt MLK2 / MLK3 và các kinase phosphoryl MKK7, sau đó kích hoạt JNK. JNK chuyển vào nhân và kích hoạt các yếu tố phiên mã như c-Jun và ATF2. Các JNK con đường được tham gia vào việc biệt hóa tế bào, tăng sinh, và nói chung là ủng hộ apoptosis.
- Cảm ứng báo hiệu cái chết: Giống như tất cả các thành viên có chứa miền chết của siêu họ TNFR, TNFR1 có liên quan đến tín hiệu tử vong. Tuy nhiên, cái chết tế bào do TNF chỉ đóng một vai trò nhỏ so với các chức năng áp đảo của nó trong quá trình viêm. Khả năng gây tử vong của nó rất yếu so với các thành viên khác trong gia đình (như Fas) và thường bị che giấu bởi các tác dụng chống apoptotic của NF-B. Tuy nhiên, TradD liên kết FADD, sau đó tuyển dụng protease cysteine caspase-8. Một nồng độ cao của caspase -8 gây ra sự kích hoạt autoproteolytic của nó và sự phân cắt tiếp theo của các caspase effector, dẫn đến apoptosis tế bào.
Các hiệu ứng vô số và thường xung đột được trung gian bởi các con đường trên cho thấy sự tồn tại của liên kết chéo. Ví dụ, NF- B tăng cường phiên mã C-FLIP, Bcl-2 và cIAP1 / cIAP2, các protein ức chế gây nhiễu tín hiệu tử vong. Mặt khác, các tầng được kích hoạt sẽ tách một số thành phần của con đường NF-κB, bao gồm RIP, IKK và các tiểu đơn vị của chính NF-B. Các yếu tố khác, chẳng hạn như loại tế bào, kích thích đồng thời của các cytokine khác hoặc lượng các loại oxy phản ứng (ROS) có thể thay đổi sự cân bằng có lợi cho con đường này hay con đường khác. Tín hiệu phức tạp như vậy đảm bảo rằng, bất cứ khi nào TNF được giải phóng, các tế bào khác nhau với các chức năng và điều kiện rất đa dạng đều có thể phản ứng thích hợp với tình trạng viêm.
Trong mô hình động vật TNFa chọn lọc giết chết các tế bào T tự trị.
Enzyme quy định Yếu Tố Hoại Tử Khối U Alpha
Protein này có thể sử dụng mô hình morpheein của quy định allosteric.
Sinh lý Yếu Tố Hoại Tử Khối U Alpha
TNF được cho là được sản xuất chủ yếu bởi các đại thực bào, nhưng nó cũng được sản xuất bởi nhiều loại tế bào bao gồm tế bào bạch huyết, tế bào mast, tế bào nội mô, tế bào cơ tim, mô mỡ, nguyên bào sợi và tế bào thần kinh. Một lượng lớn TNF được giải phóng để đáp ứng với lipopolysacarit, các sản phẩm vi khuẩn khác và Interleukin-1 (IL-1). Trong da, các tế bào mast dường như là nguồn chủ yếu của TNF được hình thành trước, có thể được giải phóng khi kích thích viêm (ví dụ, LPS).
Nó có một số hành động trên các hệ thống cơ quan khác nhau, thường là cùng với IL-1 và Interleukin-6 (IL-6):
- Trên vùng dưới đồi:
- Kích thích trục hạ đồi-tuyến yên-thượng thận bằng cách kích thích giải phóng hormone giải phóng corticotropin (CRH)
- Ức chế sự thèm ăn
- Sốt
- Trên gan: kích thích phản ứng giai đoạn cấp tính, dẫn đến sự gia tăng protein phản ứng C và một số chất trung gian khác. Nó cũng gây ra kháng insulin bằng cách thúc đẩy quá trình phosphoryl hóa serine của chất nền thụ thể insulin-1 (IRS-1), làm suy yếu tín hiệu insulin
- Nó là một chất hóa học mạnh cho bạch cầu trung tính, và thúc đẩy sự biểu hiện của các phân tử kết dính trên các tế bào nội mô, giúp bạch cầu trung tính di chuyển.
- Trên đại thực bào: kích thích thực bào và sản xuất chất oxy hóa IL-1 và lipid viêm Prostaglandin E2 (PGE 2)
- Trên các mô khác: tăng kháng insulin. TNF phosphorylates dư lượng serine thụ thể insulin, ngăn chặn sự truyền tín hiệu.
- Về chuyển hóa và lượng thức ăn: điều chỉnh nhận thức vị đắng.
Sự gia tăng nồng độ TNF cục bộ sẽ làm cho các dấu hiệu viêm của tim xảy ra: nóng, sưng, đỏ, đau và mất chức năng.
Trong khi nồng độ cao của TNF gây ra các triệu chứng giống như sốc, việc tiếp xúc kéo dài với nồng độ TNF thấp có thể dẫn đến chứng đau lưng, một hội chứng lãng phí. Điều này có thể được tìm thấy, ví dụ, ở bệnh nhân ung thư.
Nói và cộng sự cho thấy TNFa gây ra sự ức chế phụ thuộc IL-10 đối với sự mở rộng và hoạt động của tế bào T CD4 bằng cách điều chỉnh tăng mức PD-1 trên các tế bào đơn nhân dẫn đến sản xuất IL-10 bởi bạch cầu đơn nhân sau khi gắn PD-1 bởi PD-L.
Nghiên cứu gần đây của Pedersen et al. chỉ ra rằng sự gia tăng TNFa trong đáp ứng với nhiễm trùng huyết bị ức chế do sản xuất myokine do tập thể dục. Để nghiên cứu liệu tập thể dục cấp tính có gây ra phản ứng chống viêm thực sự hay không, một mô hình 'viêm cấp thấp' đã được thành lập trong đó một liều thấp E.coli endotoxin được dùng cho những người tình nguyện khỏe mạnh, những người được chọn ngẫu nhiên để nghỉ ngơi hoặc tập thể dục trước đó quản lý nội độc tố. Trong các đối tượng nghỉ ngơi, endotoxin gây ra sự gia tăng gấp 2 đến 3 lần mức độ lưu hành của TNFα. Ngược lại, khi các đối tượng thực hiện 3 giờ đi xe đạp và nhận được bolus nội độc tố trong 2,5 giờ, phản ứng TNFα hoàn toàn bị cùn. Nghiên cứu này cung cấp một số bằng chứng cho thấy tập thể dục cấp tính có thể ức chế sản xuất TNF.
Dược lý Yếu Tố Hoại Tử Khối U Alpha
TNF thúc đẩy phản ứng viêm, do đó, gây ra nhiều vấn đề lâm sàng liên quan đến rối loạn tự miễn dịch như viêm khớp dạng thấp, viêm cột sống dính khớp, bệnh viêm ruột, bệnh vẩy nến, viêm hidradeniva và bệnh hen suyễn. Những rối loạn này đôi khi được điều trị bằng cách sử dụng chất ức chế TNF. Sự ức chế này có thể đạt được với một kháng thể đơn dòng như infliximab (Remicade) liên kết trực tiếp đến TNFα, adalimumab (Humira), certolizumab pegol (Cimzia) hoặc với một decoy lưu hành thụ protein phản ứng tổng hợp như etanercept (Enbrel) mà liên kết với TNFα với hơn ái lực hơn TNFR.
Mặt khác, một số bệnh nhân được điều trị bằng thuốc ức chế TNF phát triển bệnh nặng hơn hoặc khởi phát tự miễn dịch mới. TNF dường như cũng có một khía cạnh ức chế miễn dịch. Một lời giải thích cho một cơ chế có thể là quan sát này rằng TNF có tác động tích cực đến các tế bào T điều tiết (Tress), do liên kết với thụ thể yếu tố hoại tử khối u 2 (TNFR2).
Liệu pháp chống TNF chỉ cho thấy tác dụng khiêm tốn trong điều trị ung thư. Điều trị ung thư biểu mô tế bào thận bằng Infliximab dẫn đến ổn định bệnh kéo dài ở một số bệnh nhân. Etanercept đã được thử nghiệm để điều trị bệnh nhân ung thư vú và ung thư buồng trứng cho thấy sự ổn định bệnh kéo dài ở một số bệnh nhân thông qua điều hòa giảm IL-6 và CCL2. Mặt khác, việc bổ sung infliximab hoặc etanercept vào gemcitabine để điều trị bệnh nhân ung thư tuyến tụy tiến triển không liên quan đến sự khác biệt về hiệu quả khi so sánh với giả dược.
Tương tác Yếu Tố Hoại Tử Khối U Alpha
TNFα đã được chứng minh là tương tác với TNFRSF1A.
Danh pháp Yếu Tố Hoại Tử Khối U Alpha
Một số bài báo gần đây đã lập luận rằng TNFα đơn giản nên được gọi là TNF, vì LTα không còn được gọi là TNFβ.
Tham khảo
Liên kết ngoài
This article uses material from the Wikipedia Tiếng Việt article Yếu tố hoại tử khối u alpha, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Nội dung được phát hành theo CC BY-SA 4.0, ngoại trừ khi có ghi chú khác. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Tiếng Việt (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.