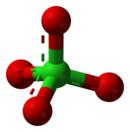
Perchlorat
Muối perchlorat là tên của các hợp chất hóa học chứa ion perchlorat ClO−4.
Đa số muối perchlorat được sản xuất thương mại. Muối perchlorat đang sử dụng chủ yếu làm thuốc phóng, nhằm khai thác đặc điểm oxy hóa mạnh của nó. Sự ô nhiễm perchlorat trong môi trường đã được nghiên cứu rộng rãi vì nó có tác dụng đến sức khỏe con người. Nghiên cứu cho thấy perchlorat có liên quan đến ảnh hưởng tiêu cực trên tuyến giáp.
| Perchlorat | |||
|---|---|---|---|
| |||
 Skeletal model of perchlorate showing various dimensions | |||
| Tên hệ thống | Perchlorate | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| DrugBank | DB03138 | ||
| MeSH | |||
| ChEBI | |||
| ChEMBL | |||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| Tham chiếu Gmelin | 2136 | ||
| Thuộc tính | |||
| Công thức phân tử | ClO− 4 | ||
| Khối lượng mol | 99.451 g mol−1 | ||
| Điểm nóng chảy | |||
| Điểm sôi | |||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Hầu hết các muối perchlorat là các chất rắn không màu, hòa tan trong nước. Bốn perchlorat là sản phẩm thương mại chính: amoni perchlorat (NH4ClO4), axit perchloric (HClO4), kali perchlorat (KClO4), và natri perchlorat (NaClO4). Perchlorat là anion được tạo thành từ sự phân ly của axit perchloric và muối của nó khi chúng hòa tan trong nước. Nhiều muối perchlorat tan trong dung môi không phải nước.
Sản xuất ở đâu và bằng cách nào
Muối perchlorat được sản xuất trong công nghiệp bằng cách oxy hóa dung dịch natri clorat bằng cách điện phân. Phương pháp này được sử dụng để điều chế natri perchlorat. Ứng dụng chính của muối này là để làm nhiên liệu tên lửa. Phản ứng của axit perchloric với các base, như amoni hydroxide cho muối amoni perchlorat. Amoni perchlorat do có giá trị cao có thể được sản xuất bằng điện hóa.
Thật ngạc nhiên, muối perchlorat có thể được tạo ra do sét đánh với sự có mặt của muối chloride. Muối perchlorat đã được phát hiện trong các mẫu mưa và tuyết ở Lubbock, Texas và Florida.
Tham khảo
| HClO4 | He | |||||||||||||||||
| LiClO4 | Be(ClO4)2 | B(ClO 4)− 4 B(ClO4)3 | ROClO3 | N(ClO4)3 NH 4ClO 4 NOClO4 | H 3OClO 4 | FClO4 | Ne | |||||||||||
| NaClO4 | Mg(ClO4)2 | Al(ClO4)3 Al(ClO 4)− 4 Al(ClO 4)2− 5 Al(ClO 4)3− 6 | Si | P | S | ClO− 4 ClOClO3 Cl 2O 7 | Ar | |||||||||||
| KClO4 | Ca(ClO4)2 | Sc(ClO4)3 | Ti(ClO4)4 | VO(ClO4)3 VO2(ClO4) | Cr(ClO4)3 | Mn(ClO4)2 | Fe(ClO4)2 Fe(ClO4)3 | Co(ClO4)2, Co(ClO4)3 | Ni(ClO4)2 | Cu(ClO4)2 | Zn(ClO4)2 | Ga(ClO4)3 | Ge | As | Se | Br | Kr | |
| RbClO4 | Sr(ClO4)2 | Y(ClO4)3 | Zr(ClO4)4 | Nb(ClO4)5 | Mo | Tc | Ru | Rh(ClO4)3 | Pd(ClO4)2 | AgClO4 | Cd(ClO4)2 | In(ClO4)3 | Sn(ClO4)4 | Sb | TeO(ClO4)2 | I | Xe | |
| CsClO4 | Ba(ClO4)2 | Lu(ClO4)3 | Hf(ClO4)4 | Ta(ClO4)5 TaO(ClO4)3 TaO2ClO4 | W | Re | Os | Ir | Pt | Au | Hg2(ClO4)2, Hg(ClO4)2 | Tl(ClO4), Tl(ClO4)3 | Pb(ClO4)2 | Bi(ClO4)3 | Po | At | Rn | |
| FrClO4 | Ra | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | ||||||||||||||||||
| La | Ce(ClO4)x | Pr(ClO4)3 | Nd(ClO4)3 | Pm | Sm(ClO4)3 | Eu(ClO4)3 | Gd(ClO4)3 | Tb(ClO4)3 | Dy(ClO4)3 | Ho(ClO4)3 | Er(ClO4)3 | Tm(ClO4)3 | Yb(ClO4)3 | |||||
| Ac | Th(ClO4)4 | Pa | UO2(ClO4)2 | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
This article uses material from the Wikipedia Tiếng Việt article Perchlorat, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Nội dung được phát hành theo CC BY-SA 4.0, ngoại trừ khi có ghi chú khác. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Tiếng Việt (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.