熱力學
熱力學 - 搜索结果 - 维基百科,自由的百科全书
在维基百科上已有名为“熱力學”的页面
 理量(像溫度、內能、熵、壓強等),描述各物理量之間的關係。热力学描述數量非常多的微觀粒子的平均行為,其定律可以用統計力學推導而得。 熱力學可以總結為四條定律: 熱力學第零定律定義了温度這一物理量,指出了相互接觸的两个系統,熱流的方向。 熱力學第一定律指出内能這一物理量的存在,並且與系統整體運動的動能…
理量(像溫度、內能、熵、壓強等),描述各物理量之間的關係。热力学描述數量非常多的微觀粒子的平均行為,其定律可以用統計力學推導而得。 熱力學可以總結為四條定律: 熱力學第零定律定義了温度這一物理量,指出了相互接觸的两个系統,熱流的方向。 熱力學第一定律指出内能這一物理量的存在,並且與系統整體運動的動能… 热力学平衡,简称热平衡,指一个热力学系统在没有外界影响的条件下,系统各部分的宏观属性(如物质的量、能量、体积等)在长时间内不发生任何变化的状态。 熱平衡是熱力學中的一個公理性概念,也是基本實驗定律,其重要意義在於它是科學定義溫度概念的基礎,是用溫度計測量溫度的依據。 在熱力學中,溫度、內能、熵是三個基本的狀態函數:…
热力学平衡,简称热平衡,指一个热力学系统在没有外界影响的条件下,系统各部分的宏观属性(如物质的量、能量、体积等)在长时间内不发生任何变化的状态。 熱平衡是熱力學中的一個公理性概念,也是基本實驗定律,其重要意義在於它是科學定義溫度概念的基礎,是用溫度計測量溫度的依據。 在熱力學中,溫度、內能、熵是三個基本的狀態函數:… 非平衡態熱力學是熱力學的一門分支,研究時變熱力學系統、不可逆轉變和開始系統。非平衡態熱力學,和平衡態熱力學(英语:Equilibrium thermodynamics)相對,是研究在非零合力、流動及產生熵,但沒有時間變動的隱定態中最成功的一門學科。早期所發現的非平衡態系統為BZ化學振盪器。 平衡態熱力學…
非平衡態熱力學是熱力學的一門分支,研究時變熱力學系統、不可逆轉變和開始系統。非平衡態熱力學,和平衡態熱力學(英语:Equilibrium thermodynamics)相對,是研究在非零合力、流動及產生熵,但沒有時間變動的隱定態中最成功的一門學科。早期所發現的非平衡態系統為BZ化學振盪器。 平衡態熱力學… 熱力學系統的體積是在描述熱力學狀態時,重要的外延性質。比容是對應的內含性質,是單位質量的體積。體積為一狀態函數,和其他熱力學性質(如壓力、溫度)之間有相互關係。例如理想氣體的體積就可以依理想氣體定律,用壓力及溫度來表示。 一系統的體積可能與分析系統所用的控制體積重合,但也可能不重合。 熱力學…
熱力學系統的體積是在描述熱力學狀態時,重要的外延性質。比容是對應的內含性質,是單位質量的體積。體積為一狀態函數,和其他熱力學性質(如壓力、溫度)之間有相互關係。例如理想氣體的體積就可以依理想氣體定律,用壓力及溫度來表示。 一系統的體積可能與分析系統所用的控制體積重合,但也可能不重合。 熱力學…- 在古典熱力學中,熵是關於一熱力學系統之自發變化方向或變化結果的狀態參數,於十九世紀中葉由德國物理學家魯道夫·克勞修斯提出,取自希臘文τρoπή ,意為「轉化(transformation)」,用於說明內能是否能轉化為熱或功。熵指出有些熱力學過程雖不違反能量守恆定律但仍然不可行。熵的定義建立了熱力學…
 Q+\delta W\,} 根據熱力學第二定律,可知下式在可逆過程中成立: d S = δ Q / T {\displaystyle dS=\delta Q/T\,} 因此: δ Q = T d S {\displaystyle \delta Q=TdS\,} 用此式代入熱力學第一定律的表示式中,可得 d…
Q+\delta W\,} 根據熱力學第二定律,可知下式在可逆過程中成立: d S = δ Q / T {\displaystyle dS=\delta Q/T\,} 因此: δ Q = T d S {\displaystyle \delta Q=TdS\,} 用此式代入熱力學第一定律的表示式中,可得 d… 熱力學第一定律(英語:First Law of Thermodynamics)是熱力學的四條基本定律之一,能量守恒定律對非孤立系統的擴展。此時能量可以以功W或熱量Q的形式傳入或傳出系統。即: Δ E i n t = Q − W {\displaystyle \qquad \mathrm {\Delta…
熱力學第一定律(英語:First Law of Thermodynamics)是熱力學的四條基本定律之一,能量守恒定律對非孤立系統的擴展。此時能量可以以功W或熱量Q的形式傳入或傳出系統。即: Δ E i n t = Q − W {\displaystyle \qquad \mathrm {\Delta… 熱力學第零定律(英語:Zeroth Law of Thermodynamics),又稱熱平衡定律,是熱力學的四條基本定律之一,是一個關於互相接觸的物體於熱平衡時的描述,並為溫度提供了理論基礎。最常用的定律表述是: 換句話說,第零定律是指:在一個數學二元關係之中,熱平衡是遞移的。…
熱力學第零定律(英語:Zeroth Law of Thermodynamics),又稱熱平衡定律,是熱力學的四條基本定律之一,是一個關於互相接觸的物體於熱平衡時的描述,並為溫度提供了理論基礎。最常用的定律表述是: 換句話說,第零定律是指:在一個數學二元關係之中,熱平衡是遞移的。… 熱力學方程(英語:thermodynamic equation)是以數學架構描述於實驗室或生產製程中測得的熱力學物理量。熱力學是基於一些基礎假設,即熱力學定律。…
熱力學方程(英語:thermodynamic equation)是以數學架構描述於實驗室或生產製程中測得的熱力學物理量。熱力學是基於一些基礎假設,即熱力學定律。…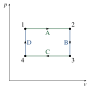 熱力學圖是科學家及工程師用來表示物體(多半是流體)熱力學狀態及其變化的圖。例如T-s圖(溫度熵圖)就可以說明流體在壓縮機中的溫度及熵的變化。 以下是一些常見的熱力學圖: 壓力體積圖(英语:Pressure volume diagram) 溫度熵圖 焓熵圖(英语:Enthalpy–entropy chart)…
熱力學圖是科學家及工程師用來表示物體(多半是流體)熱力學狀態及其變化的圖。例如T-s圖(溫度熵圖)就可以說明流體在壓縮機中的溫度及熵的變化。 以下是一些常見的熱力學圖: 壓力體積圖(英语:Pressure volume diagram) 溫度熵圖 焓熵圖(英语:Enthalpy–entropy chart)… 熱力學狀態(英語:Thermodynamic state)是指一組描述熱力學系統的狀態。個別的參數一般會稱為狀態變數、狀態參數或是熱力學變數。只要一熱力學系統中有足夠多的已知狀態,其他的狀態就已被確定,而所需要的狀態數量視系統複雜程度而定。 例如一封閉簡單系統,其中有二公升的氧氣,壓力為一大氣壓,…
熱力學狀態(英語:Thermodynamic state)是指一組描述熱力學系統的狀態。個別的參數一般會稱為狀態變數、狀態參數或是熱力學變數。只要一熱力學系統中有足夠多的已知狀態,其他的狀態就已被確定,而所需要的狀態數量視系統複雜程度而定。 例如一封閉簡單系統,其中有二公升的氧氣,壓力為一大氣壓,…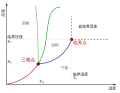 在熱力學中,臨界点是可使一物質以液態存在的最高溫度或以氣態存在的最高壓力,當物質的溫度、壓力超過此界線——即臨界温度及臨界壓力——會相變成同時擁有液態及氣態特徵的流體:超臨界流體。 临界温度下的p-V等温线上,在临界点处的一阶、二阶导数均为零,即: (∂p∂V)T=(∂2p∂V2)T=0{\displaystyle…
在熱力學中,臨界点是可使一物質以液態存在的最高溫度或以氣態存在的最高壓力,當物質的溫度、壓力超過此界線——即臨界温度及臨界壓力——會相變成同時擁有液態及氣態特徵的流體:超臨界流體。 临界温度下的p-V等温线上,在临界点处的一阶、二阶导数均为零,即: (∂p∂V)T=(∂2p∂V2)T=0{\displaystyle… TC為低溫熱源的絕對溫度 TH為高溫熱源的絕對溫度 上式的熱效率是指熱機產生的功和高溫熱源提供能量的比值。 上述定律其實是熱力學第二定律的結果。不過當初在推導此定律時是以熱質說為基礎,且以此定律為基礎建立熱力學第二定律。 此定理可用以下的方式,針對不可逆熱機及可逆熱機的情形進行證明 假設一不可逆熱機,其熱源為 T 1…
TC為低溫熱源的絕對溫度 TH為高溫熱源的絕對溫度 上式的熱效率是指熱機產生的功和高溫熱源提供能量的比值。 上述定律其實是熱力學第二定律的結果。不過當初在推導此定律時是以熱質說為基礎,且以此定律為基礎建立熱力學第二定律。 此定理可用以下的方式,針對不可逆熱機及可逆熱機的情形進行證明 假設一不可逆熱機,其熱源為 T 1… 化學熱力學(英語:Chemical thermodynamics)是在熱力學定律範疇之下,研究化學反應以及系統狀態之間熱和功的交互關係。化學熱力學不僅包含實驗測定不同的熱力學性質,還應用數學分析來探討化學問題及自發過程。 化學熱力學的建構是基於前兩個熱力學定律,由熱力學…
化學熱力學(英語:Chemical thermodynamics)是在熱力學定律範疇之下,研究化學反應以及系統狀態之間熱和功的交互關係。化學熱力學不僅包含實驗測定不同的熱力學性質,還應用數學分析來探討化學問題及自發過程。 化學熱力學的建構是基於前兩個熱力學定律,由熱力學… 热力学第二定律(英語:second law of thermodynamics)是热力学的四条基本定律之一,表述热力学过程的不可逆性——孤立系统自發地朝著熱力學平衡方向──最大熵狀態──演化,同样地,第二类永动机永不可能实现。 這一定律的歷史可追溯至尼古拉·卡诺对于热机效率的研究,及其于1824年提…
热力学第二定律(英語:second law of thermodynamics)是热力学的四条基本定律之一,表述热力学过程的不可逆性——孤立系统自發地朝著熱力學平衡方向──最大熵狀態──演化,同样地,第二类永动机永不可能实现。 這一定律的歷史可追溯至尼古拉·卡诺对于热机效率的研究,及其于1824年提…- 大氣熱力學是一門研究熱功轉換,在地球大氣層內以氣候的方式表現的學問。大氣熱力學運用熱力學定律去描述、解釋一些大氣中的物理現象,例如潮濕空氣的特性、雲的形成、大氣邊界層、大氣中的鉛直不穩定性等。大氣熱力學常使用熱力學圖去預測風暴的形成。大氣熱力學是雲物理學和大量天氣模型中對流參數化的基石,常被用於對流平衡等氣候模型。…
 在平衡熱力學(英语:Equilibrium thermodynamics)中, 态函数(英語:state function)又称狀態函數、热力学函数(thermodynamic function),是描述系统热力学状态的宏观物理性质的函数。处于平衡状态的热力学…
在平衡熱力學(英语:Equilibrium thermodynamics)中, 态函数(英語:state function)又称狀態函數、热力学函数(thermodynamic function),是描述系统热力学状态的宏观物理性质的函数。处于平衡状态的热力学… 大多數開頭有「比」的性質都是以單位質量為基準的,不過有時會使用其他的基準,例如單位莫耳。 无量纲量 熱力學物質資料庫(英语:Thermodynamic databases for pure substances) 熱力學狀態 Aylward, Gordon; Findlay, Tristan, SI Chemical…
大多數開頭有「比」的性質都是以單位質量為基準的,不過有時會使用其他的基準,例如單位莫耳。 无量纲量 熱力學物質資料庫(英语:Thermodynamic databases for pure substances) 熱力學狀態 Aylward, Gordon; Findlay, Tristan, SI Chemical… 热力学第三定律(the third law of thermodynamics)是热力学四条基本定律之一,它描述的是热力学系统的熵在温度趋近于绝对零度时將趋于定值,而对于完整晶体而言,这个定值为零。由於这個定律是由瓦尔特·能斯特歸納并發表,因此又常被称为能斯特定理或能斯特假定。1923年,吉爾伯特…
热力学第三定律(the third law of thermodynamics)是热力学四条基本定律之一,它描述的是热力学系统的熵在温度趋近于绝对零度时將趋于定值,而对于完整晶体而言,这个定值为零。由於这個定律是由瓦尔特·能斯特歸納并發表,因此又常被称为能斯特定理或能斯特假定。1923年,吉爾伯特… 黑洞热力学,或称作黑洞力学,是发展于1970年代将热力学的基本定律应用到广义相对论领域中黑洞研究而产生的理论。虽然至今人们还不能清晰地理解阐述这一理论,黑洞热力学的存在强烈地暗示了广义相对论、热力学和量子理论彼此之间深刻而基础的联系。尽管它看上去只是从热力学…
黑洞热力学,或称作黑洞力学,是发展于1970年代将热力学的基本定律应用到广义相对论领域中黑洞研究而产生的理论。虽然至今人们还不能清晰地理解阐述这一理论,黑洞热力学的存在强烈地暗示了广义相对论、热力学和量子理论彼此之间深刻而基础的联系。尽管它看上去只是从热力学…
- 國際音標 (高雄):/ziɛt̚⁴⁻³² liɪk̚⁴⁻³² hak̚⁴/ 熱力學 研究熱現象中物態轉變和能量轉換規律的學科。 翻譯 熱(ねつ)力(りき)學(がく) • (netsurikigaku) 熱力学的舊字體形式 熱力學 (yeoryeokhak) (韓文 열역학) 열역학 (yeoryeokhak)的漢字
- 10⁻⁷ N,则每根导线中的电流为 1 A。 [ CIPM (1946),决议 2。第 9 届 CGPM (1948) 批准] 开尔文 热力学温度开尔文是水三相点热力学温度的 1/273.16, [第 13 届 CGPM (1967),决议 4] 摩尔 摩尔是一系统的物质的量,该系统中所包含的基本单元数与
- 在物質能量轉換過程不探討個別分子特性的科學,稱之為古典熱力學(classical thermodynamics); 在物質能量轉換過程探討個別分子特性的科學,則稱之為統計熱力學(statistical thermodynamics)。 热力学第零定律(又稱熱平衡定律):只要A和B同時與C處於熱平衡,則A和B處於熱平衡狀態。
- 南师大 无机化学教研室. 无机化学(上册)第四版. 高等教育出版社. pp 427. 附表8 在298.15 K和100 kPa时一些单质和化合物的热力学函数 注:此法可以得到纯度较高的硫,并可用于有机反应 说明:①倒入时应缓慢,否则产生块状硫或连在一起的硫。②倒入的速度越慢越好,为分离较小的球状硫,可用纱网等工具进行过滤。




