化學反應
化學反應 - 搜索结果 - 维基百科,自由的百科全书
在维基百科上已有名为“化學反應”的页面
- 裂分開形成兩個以上的小分子,或是分子內部的原子重組。為了形成變化,化學反應通常和化學鍵的形成與斷裂有關。特別注意化學反應不會以任何方式改變原子核,而仅限於在原子外的電子雲交互作用。雖然核變形後可能會引發化學反應,但是核反應與化學反應無關,因為核反應會改變反應的原子,變成另一種原子,根據質量守恆,反…
 engineering)。 化學反應 化學動力學 化學反應器 林爱光(1999):《化学工程基础》,第277頁,中國大陸:清华大学出版社。 郭鍇、唐小恒(2007):《化學反應工程》,第1頁,北京市:化學工業出版社。 H·Scott Fogler(2005):《化學反應工程》,第I頁,中國大陸:化學工業出版社。…
engineering)。 化學反應 化學動力學 化學反應器 林爱光(1999):《化学工程基础》,第277頁,中國大陸:清华大学出版社。 郭鍇、唐小恒(2007):《化學反應工程》,第1頁,北京市:化學工業出版社。 H·Scott Fogler(2005):《化學反應工程》,第I頁,中國大陸:化學工業出版社。…- 反应速率(英語:Rate of reaction)是在化學反應中,反應物轉變成生成物的速度。不同反應的速率有所不同。例如鐵的生銹(氧化)過程的需時以年來計算;在火中燃燒纖維素,卻只需要數秒鐘的時間。對於大部分的反應,反應速率隨時間而減少。 反應速率可以用這種方式來表達: r = lim Δ t → 0…
- 化學反應模型(英語:chemical reaction model)將物理知識轉化為數學公式,可用於化學工程中實際問題的計算模擬。計算機模擬為研究各種條件下的化學過程提供了靈活性。化學反應的建模涉及求解描述每個組成成份的對流、擴散和反應源的守恆方程。 ∂(ρYi)∂t+∇⋅(ρv→Yi)=−∇⋅J→i+Ri{\displaystyle…
 反應器的外觀 反應器的內部剖視圖 化學反應器(英語:chemical reactor)是化工生產或實驗上進行化學反應的裝置,簡稱反應器,在工業上亦有工業反應器的別稱。 反應器主要功能是控制反應過程中的各種條件參數,例如壓力(P)、溫度(T)、體積(V)、滯留時間(τ{\displaystyle \tau…
反應器的外觀 反應器的內部剖視圖 化學反應器(英語:chemical reactor)是化工生產或實驗上進行化學反應的裝置,簡稱反應器,在工業上亦有工業反應器的別稱。 反應器主要功能是控制反應過程中的各種條件參數,例如壓力(P)、溫度(T)、體積(V)、滯留時間(τ{\displaystyle \tau…- 化学平衡(英語:Chemical equilibrium)是指在宏观条件的可逆反应中,化学反应正逆反应速率相等,且反应物濃度和生成物浓度不再改變的状态。 化学平衡也是化学热力学的主要研究內容。 當一個化學反應達到化學平衡後,需要外部變因恆定才能保持此平衡狀態。如果外部變因有所改變,此平衡狀態將被打…
- equation)又称化学反应式、化学反应方程式,是用化学式来描述各种物质之间的不同化学反应的式子。 化学方程式反映化学反应中“质”和“量”两方面,分别表示反应前后物质的种类与反应时各物质之间量的关系。而在书写化学方程式要遵守两个原则:一是必须依据客观事实,绝不能凭空臆想、臆造事实上不存在的物质和化学反应…
- (Chichibabin reaction(英语:Chichibabin reaction)) 吡啶用氨基鈉處理時,發生氨基化作用生成2-氨基吡啶的化學反應。 Chichibabin吡啶合成 (Chichibabin pyridine synthesis(英语:Chichibabin pyridine…
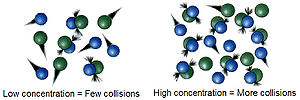 化学动力学也称反应动力学、化學反應動力學,是物理化学的一个分支,研究化学反应的反应速率及反应机理。它的主要研究领域包括:分子反应动力学、催化动力学、基元反应动力学、宏观动力学、表观动力学等,也可依不同化学分支分类为有机反应动力学及无机反应动力学。化学动力学往往是化工生产过程中的决定性因素。…
化学动力学也称反应动力学、化學反應動力學,是物理化学的一个分支,研究化学反应的反应速率及反应机理。它的主要研究领域包括:分子反应动力学、催化动力学、基元反应动力学、宏观动力学、表观动力学等,也可依不同化学分支分类为有机反应动力学及无机反应动力学。化学动力学往往是化工生产过程中的决定性因素。…- 速率控制步驟 (分类化學反應)(RDS)),是一個化學詞彙,用以表達在化學反應中,反應速率最慢的一個步驟。認識一個化學反應當中最慢的一個步驟的重要性在於能夠有效率地改善整個化學反應的速度,從而達致更高的产率等。一個常用的比喻就是一條狹窄的水管——無論水流有多快,也無法改變水的流量。速率控制步驟就是影響整個化學反應速率的那條水管。 舉個簡單例子,…
- 催化剂 (分类化学反应)催化劑(catalyst)舊稱觸媒,是能通過提供另一活化能較低的反應途徑而加快化學反應速率,而本身的質量、組成和化學性質在參加化學反應前後保持不變的物質。例如二氧化錳可以作為過氧化氫(雙氧水的成分)分解的催化劑;又如在生物體系中,酶和具有催化活性的RNA,均為一種催化劑。催化剂不能改变热力学平衡,只能影响反应过程达到平衡的速度。…
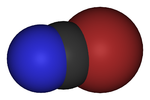 溴化氰含劇毒而且性質活潑,其易发生聚合,产生三聚氰溴 (页面存档备份,存于互联网档案馆)。与氫氧化鈉發生化學反應生成氰酸鈉,與氨和胺發生化學反應生成氨基氰,與醇發生化學反應生成三聚氰酸酯。溴化氰遇水易发生水解。 3BrCN → (CNBr)₃ BrCN + 2 NaOH → NaOCN +…
溴化氰含劇毒而且性質活潑,其易发生聚合,产生三聚氰溴 (页面存档备份,存于互联网档案馆)。与氫氧化鈉發生化學反應生成氰酸鈉,與氨和胺發生化學反應生成氨基氰,與醇發生化學反應生成三聚氰酸酯。溴化氰遇水易发生水解。 3BrCN → (CNBr)₃ BrCN + 2 NaOH → NaOCN +… 化學能 (分类化學反應)化學能是內能的一種,指一些需要經由化學反應釋放出來的能量。例如煤的能量是由燃燒(與氧反應)釋放出來的,貯存於煤裏面的能量即稱為化學能。電池裡的化學物質,是藉著化學變化而產生電能。 生物裡呼吸作用、光合作用產生之能量,也是化學能。 由於化學能是化學反應時產生的,因此是一種隱蔽的能量,不能直接用來做功,…
化學能 (分类化學反應)化學能是內能的一種,指一些需要經由化學反應釋放出來的能量。例如煤的能量是由燃燒(與氧反應)釋放出來的,貯存於煤裏面的能量即稱為化學能。電池裡的化學物質,是藉著化學變化而產生電能。 生物裡呼吸作用、光合作用產生之能量,也是化學能。 由於化學能是化學反應時產生的,因此是一種隱蔽的能量,不能直接用來做功,… 化學反應的守恆必須符合物理守恆定律,反應前後應符合: 質量守恒定律:一個化學反應發生,物質的總質量不會有任何變化。 能量守恒定律:化學反應所產生的能量總和不變,只是能量形式依照反應模式而變化。引出三个重要概念:平衡,热力学,动力学。 電荷守恆定律:化學反應前後的電荷數應守恆。 阿伏伽德罗定律…
化學反應的守恆必須符合物理守恆定律,反應前後應符合: 質量守恒定律:一個化學反應發生,物質的總質量不會有任何變化。 能量守恒定律:化學反應所產生的能量總和不變,只是能量形式依照反應模式而變化。引出三个重要概念:平衡,热力学,动力学。 電荷守恆定律:化學反應前後的電荷數應守恆。 阿伏伽德罗定律… Zewail,又译泽韦尔、扎威尔,1946年2月26日—2016年8月2日),埃及化學家,飛秒化學專家。他研究的技術能將研究化學反應的時間尺度縮減至飛秒,透過攝影將化學反應中每個微細變化忠實地紀錄。 艾哈迈德·兹韦勒1946年2月25日生于埃及达曼胡尔,在Disuq长大。他在亞歷山大大學取得学士學…
Zewail,又译泽韦尔、扎威尔,1946年2月26日—2016年8月2日),埃及化學家,飛秒化學專家。他研究的技術能將研究化學反應的時間尺度縮減至飛秒,透過攝影將化學反應中每個微細變化忠實地紀錄。 艾哈迈德·兹韦勒1946年2月25日生于埃及达曼胡尔,在Disuq长大。他在亞歷山大大學取得学士學… 化學反應中,反應前化學成分的質量是等於反應後分子的總質量。 因此,在孤立系統中的任何化學反應和低能量熱力學過程期間,反應物或起始材料的總質量必須等於產物的質量。質量守恆的概念在化學,力學和流體動力學等許多領域得到了廣泛的應用。歷史上,米哈伊爾·羅蒙諾索夫和安托萬·拉瓦錫分别獨立發現了化學反應…
化學反應中,反應前化學成分的質量是等於反應後分子的總質量。 因此,在孤立系統中的任何化學反應和低能量熱力學過程期間,反應物或起始材料的總質量必須等於產物的質量。質量守恆的概念在化學,力學和流體動力學等許多領域得到了廣泛的應用。歷史上,米哈伊爾·羅蒙諾索夫和安托萬·拉瓦錫分别獨立發現了化學反應…- 产物 (化学) (分类化学反应)产物(product)又称生成物,是化学反应所得到的物质。 根据反应速率的不同,产物生成的速度的可以从纳秒到世纪不等。 在「H++H2O->H3O+」中,H3O+是這個化學反應的產物。 存档副本. [2023-07-15]. (原始内容存档于2023-07-16). 反应物 底物 过渡态 中间体 P…
 其中最有名的一篇報告是《非均相物質間的平衡》。在這些報告中,吉布斯證明了熱力學第一、第二定律如何以圖形及數學方法來測量,不僅可確定化學反應中兩邊的熱平衡,還可得知化學反應的發生的趨勢或者反應行進的方向。吉布斯收集了其他熱力學相關研究人員的著作,如克勞修斯跟尼古拉·卡諾的論文,提供了第一個在研究熱力學基礎理論上的整合架構。…
其中最有名的一篇報告是《非均相物質間的平衡》。在這些報告中,吉布斯證明了熱力學第一、第二定律如何以圖形及數學方法來測量,不僅可確定化學反應中兩邊的熱平衡,還可得知化學反應的發生的趨勢或者反應行進的方向。吉布斯收集了其他熱力學相關研究人員的著作,如克勞修斯跟尼古拉·卡諾的論文,提供了第一個在研究熱力學基礎理論上的整合架構。…- 收率 (分类化學反應)收率(yield 或percent yield)或稱作反應收率、也稱產率,一般用於化學及工業生產,是指在化學反應或相關的化學工業生產中,投入单位数量原料获得的实际生产的产品产量与理论计算的产品产量的比值。同樣的一個化學反應在不同的氣壓、溫度下會有不同的收率。一般而言,收率在90%以上是很高的收率,75%以上是不…
- 基元反应 (分类化学反应)reaction)或稱基本反應,顾名思义,即最简单的化学反应步骤,是一个或多个化学物种直接作用,一步(单一过渡态)转化为反应产物的过程;或是說,將化學反應過程盡可能分為若干簡單反應步驟(如分解、取代、結合等)時,其“各反應步驟”稱為基元反應。“基元”的意思是“基本单元”,是最小独立不可分的个体单元。 微观上看所有化学反应…
- 漢語維基百科有一篇文章關於: 化學反應/化学反应 維基百科 简体:化 学 反 应 繁体:化 學 反 應 汉语拼音:huà xúe fǎn yìng 翻譯 本词条全部或部分内容来自cc-by-sa-3.0许可协议的CC-CEDICT项目。
- 化学反应的实质是旧化学键的断裂和新化学键的生成。化学键的断裂会吸收能量,而化学键的形成会放出能量,故化学反应一定伴随着能量的变化。 物质中含有的化学能,伴随着化学反应的发生,会转化为光能(如物质燃烧时发光)、电能(如原电池)、内能(如物质燃烧时发热)等。
- 這個列表記載了關於鎢的化學反應方程式。 WO3 + 3H2 → W + 3H2O 高温反应。 2WO3 + 3C→ 2W + 3CO2 WO3 + 2NaOH + H2O→ Na2WO4·2H2O CuO+WO3 →800oC CuWO4{\displaystyle \mathrm {CuO+WO_{3}\
- (六)用作分離流程中的載體; (七)核級用途。 三、“化學反應”是指通過分子鍵斷裂並形成新的分子鍵,或通過改變分子內原子的空間排列而形成具有新結構的分子的過程(包括生化過程)。就本定義而言,下列過程不視為化學反應: (一)溶解於水或其他溶劑; (二)去除溶劑,包括作為溶劑的水; (三)添加或去除結晶水。
- 诺贝尔化学奖的总奖金为100万美元。美国科学家阿诺德获奖,是因为她在1993年实现首次酶的定向进化,通过自然选择的原理催生一种加速化学反应的新的蛋白质。 乔治·史密斯的贡献是开发出一种被称作噬菌体展示的技术,这种病毒吞噬菌体以产生新的蛋白质。 英国的科学家格里格·温特使用噬菌体展示技
- 维基百科中的相关条目: 李遠哲 李遠哲(英语:Yuan-Tseh Lee,1936年11月19日—),臺灣知名化學家,新竹市人。1986年,因首先以分子角度來研究化學反應的動力學而與達德利·赫施巴赫及約翰·波拉尼共獲諾貝爾化學獎,是第一位獲得諾貝爾獎的臺灣人。1994年1月15日,返國出任中華民國中央研究院院長至2









