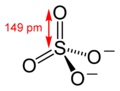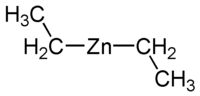Zinc Enlaces externos
Resultados de la búsqueda para «Zinc Enlaces externos», la enciclopedia libre
Si consideras que este artículo debería existir, conoces nuestros pilares, dispones de fuentes fiables y sabes indicarlas como referencias, puedes crearlo, opcionalmente usando nuestro asistente.
 electroquímica o pila húmeda Leclanché.[1] Está formada por un recipiente externo de zinc que sirve como contenedor y terminal o polo negativo (ánodo) en cuyo…
electroquímica o pila húmeda Leclanché.[1] Está formada por un recipiente externo de zinc que sirve como contenedor y terminal o polo negativo (ánodo) en cuyo…- Asturiana de Zinc, S. A. (AZSA) es una empresa tradicionalmente asturiana, actualmente propiedad de la multinacional Glencore. Sus principales actividades…
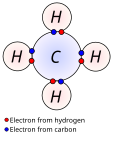 Estos electrones son los que presentan la facilidad de formar enlaces.[3] Estos enlaces pueden darse de diferente manera, ya sea por intercambio de estos…
Estos electrones son los que presentan la facilidad de formar enlaces.[3] Estos enlaces pueden darse de diferente manera, ya sea por intercambio de estos… Fosfodiesterasa (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)nucleasas son enzimas hidrolasas (EC 3.1.4) que catalizan la ruptura de los enlaces fosfodiéster,[1] como por ejemplo los que se establecen en los ácidos…
Fosfodiesterasa (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)nucleasas son enzimas hidrolasas (EC 3.1.4) que catalizan la ruptura de los enlaces fosfodiéster,[1] como por ejemplo los que se establecen en los ácidos… El cloruro de zinc es un compuesto químico cuya fórmula es ZnCl2. Se conocen nueve formas cristalinas diferentes de cloruro de zinc, incoloras o blancas…
El cloruro de zinc es un compuesto químico cuya fórmula es ZnCl2. Se conocen nueve formas cristalinas diferentes de cloruro de zinc, incoloras o blancas… Pila Leclanché (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)despolarizador de dióxido de manganeso, y un ánodo (terminal negativa) de zinc.[1] La pila Leclanché era esencialmente una versión independiente de una…
Pila Leclanché (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)despolarizador de dióxido de manganeso, y un ánodo (terminal negativa) de zinc.[1] La pila Leclanché era esencialmente una versión independiente de una…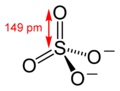 Sulfato (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)descripción de los enlaces en términos modernos fue realizada por Gilbert Lewis es su trabajo seminal de 1916 donde describió los enlaces en función de octetos…
Sulfato (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)descripción de los enlaces en términos modernos fue realizada por Gilbert Lewis es su trabajo seminal de 1916 donde describió los enlaces en función de octetos…- implica la interrupción de: Enlaces no covalentes dipolo-dipolo entre cadenas laterales polares de aminoácidos. Enlaces dipolo inducidos por fuerzas…
 Elementos del grupo 12 (sección Zinc)[1] es un grupo de elementos químicos de la tabla periódica que incluye el zinc (Zn), el cadmio (Cd) y el mercurio (Hg).[2] Varios experimentos sobre átomos…
Elementos del grupo 12 (sección Zinc)[1] es un grupo de elementos químicos de la tabla periódica que incluye el zinc (Zn), el cadmio (Cd) y el mercurio (Hg).[2] Varios experimentos sobre átomos… Indio (elemento) (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)galio, pero más parecido al zinc (de hecho, la principal fuente de obtención de este metal es a partir de los minerales de zinc). Su principal aplicación…
Indio (elemento) (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)galio, pero más parecido al zinc (de hecho, la principal fuente de obtención de este metal es a partir de los minerales de zinc). Su principal aplicación… aleaciones a base de hierro, aunque recientemente también se ha investigado el zinc[4]. Actualmente se ha desarrollado el uso de metales absorbibles como implantes…
aleaciones a base de hierro, aunque recientemente también se ha investigado el zinc[4]. Actualmente se ha desarrollado el uso de metales absorbibles como implantes…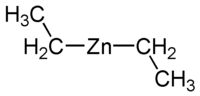 Compuesto de organozinc (categoría Compuestos de zinc)Los compuestos de organocinc son compuestos químicos que contienen enlaces químicos entre átomos de carbono y de cinc. La química de organocinc es la…
Compuesto de organozinc (categoría Compuestos de zinc)Los compuestos de organocinc son compuestos químicos que contienen enlaces químicos entre átomos de carbono y de cinc. La química de organocinc es la… Latón (categoría Wikipedia:Artículos con enlaces externos rotos)auricalco[1] o azófar[2] es una aleación de cobre y zinc. Las proporciones de cobre y zinc pueden variar para crear una variedad de latones con propiedades…
Latón (categoría Wikipedia:Artículos con enlaces externos rotos)auricalco[1] o azófar[2] es una aleación de cobre y zinc. Las proporciones de cobre y zinc pueden variar para crear una variedad de latones con propiedades… Pila alcalina (categoría Wikipedia:Artículos con enlaces externos rotos)pilas eléctricas que obtienen su energía de la reacción química entre el zinc, actuando como ánodo, y el dióxido de manganeso (MnO2), como cátodo, y empleando…
Pila alcalina (categoría Wikipedia:Artículos con enlaces externos rotos)pilas eléctricas que obtienen su energía de la reacción química entre el zinc, actuando como ánodo, y el dióxido de manganeso (MnO2), como cátodo, y empleando…- por los cabellos formando una capa protectora. El sebo protege de daños externos la estructura proteínica del cabello, pero tiene un coste asociado: el…
 Protección catódica (categoría Wikipedia:Artículos con enlaces externos rotos)protección catódica. Si la capa de zinc está rayada o dañada a nivel local y el acero está expuesto, cerca de recubrimiento de zinc forma una pila galvánica con…
Protección catódica (categoría Wikipedia:Artículos con enlaces externos rotos)protección catódica. Si la capa de zinc está rayada o dañada a nivel local y el acero está expuesto, cerca de recubrimiento de zinc forma una pila galvánica con… Elemento representativo (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)son generalmente considerados como metales de transición, sin embargo, el zinc (Zn), el cadmio (Cd), y el mercurio (Hg) comparten algunas propiedades de…
Elemento representativo (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)son generalmente considerados como metales de transición, sin embargo, el zinc (Zn), el cadmio (Cd), y el mercurio (Hg) comparten algunas propiedades de… Aneurisma (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)exceso de ingesta de zinc puede conducir a la deficiencia de cobre (hypocupremia). Esta deficiencia se debe a que el exceso de zinc en el cuerpo provoca…
Aneurisma (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)exceso de ingesta de zinc puede conducir a la deficiencia de cobre (hypocupremia). Esta deficiencia se debe a que el exceso de zinc en el cuerpo provoca… Corrosión galvánica (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)se generaliza cuando el recubrimiento de zinc de protección se rompe y el acero subyacente es atacado. El zinc es atacado preferentemente porque es menos…
Corrosión galvánica (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)se generaliza cuando el recubrimiento de zinc de protección se rompe y el acero subyacente es atacado. El zinc es atacado preferentemente porque es menos… Alessandro Volta (categoría Wikipedia:Artículos con enlaces externos rotos)H+ y SO2− 4. El zinc metálico, que se encuentra más arriba en la electroquímica que el cobre y el hidrógeno, se oxida a cationes de zinc (Zn2+) y crea electrones…
Alessandro Volta (categoría Wikipedia:Artículos con enlaces externos rotos)H+ y SO2− 4. El zinc metálico, que se encuentra más arriba en la electroquímica que el cobre y el hidrógeno, se oxida a cationes de zinc (Zn2+) y crea electrones…
- potencia inducida por tetracloruro de carbono-fibrosis hepática en ratas Enlaces externos [1]Ficha de seguridad diclorometano INSHT [2]Ficha de seguridad cloroformo
- incrementos de 25.9%, 6.9% y 3.2%, respectivamente; en el oro, el cobre, el zinc y el azufre se observaron moderadas disminuciones. La construcción continúa