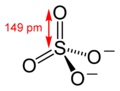Número Π Enlaces externos
Resultados de la búsqueda para «Número Π Enlaces externos», la enciclopedia libre
Si consideras que este artículo debería existir, conoces nuestros pilares, dispones de fuentes fiables y sabes indicarlas como referencias, puedes crearlo, opcionalmente usando nuestro asistente.
 El número π (pi) es la relación entre la longitud de una circunferencia y su diámetro en geometría euclidiana.[1] Es un número irracional[2] y una de…
El número π (pi) es la relación entre la longitud de una circunferencia y su diámetro en geometría euclidiana.[1] Es un número irracional[2] y una de…- Enlace (química) (redirección desde Enlaces químicos)aglomerados, se ha postulado la existencia de enlaces de cuatro centros y dos electrones. En ciertos sistemas conjugados π (pi), como el benceno y otros compuestos…
 Aromaticidad (sección Enlaces dobles del benceno)enlaces dobles en una configuración y, entre flechas, las demás configuraciones como oportunidades adicionales tengan los electrones de los enlaces dobles…
Aromaticidad (sección Enlaces dobles del benceno)enlaces dobles en una configuración y, entre flechas, las demás configuraciones como oportunidades adicionales tengan los electrones de los enlaces dobles… Piled Higher and Deeper (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)personaje y su autor, Jorge Cham. El número π/2 aparece frecuentemente en el cómic. Sitio oficial. Los siguiente enlaces externos fueron verificados el 18 de octubre…
Piled Higher and Deeper (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)personaje y su autor, Jorge Cham. El número π/2 aparece frecuentemente en el cómic. Sitio oficial. Los siguiente enlaces externos fueron verificados el 18 de octubre…- cuenta que el número entero Rn es necesariamente un número primo, dado que: π(x)−π(x/2){\displaystyle \pi (x)-\pi (x/2)} y, por lo tanto, π(x){\displaystyle…
- seis electrones π deslocalizados residen en un espacio mayor que existe por encima y por debajo del plano del anillo. Todos los enlaces carbono-carbono…
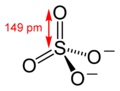 Sulfato (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)proponer que los canónicos de resonancia más significativos tenían dos enlaces π que utilizaban orbitales d. Su razonamiento era que la carga del azufre…
Sulfato (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)proponer que los canónicos de resonancia más significativos tenían dos enlaces π que utilizaban orbitales d. Su razonamiento era que la carga del azufre…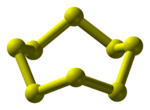 Catenación (categoría Wikipedia:Artículos con enlaces externos rotos)cadena larga, vía una serie de enlaces covalentes. La catenación se da más fácilmente en el carbono, que forma enlaces covalentes con otros átomos de…
Catenación (categoría Wikipedia:Artículos con enlaces externos rotos)cadena larga, vía una serie de enlaces covalentes. La catenación se da más fácilmente en el carbono, que forma enlaces covalentes con otros átomos de… BODIPY (sección Síntesis y extensión del sistema π)los electrones- π. Un sistema conjugado está basado en una alteración de los enlaces sencillos y dobles carbono-carbono. Los enlaces sencillos están conformados…
BODIPY (sección Síntesis y extensión del sistema π)los electrones- π. Un sistema conjugado está basado en una alteración de los enlaces sencillos y dobles carbono-carbono. Los enlaces sencillos están conformados…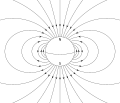 cero porque los dos enlaces C − Cl están en lados opuestos de C = C y se cancelan (y los dos momentos de enlace para los enlaces C − H mucho menos polares…
cero porque los dos enlaces C − Cl están en lados opuestos de C = C y se cancelan (y los dos momentos de enlace para los enlaces C − H mucho menos polares… orbitales de enlaces que tienen una energía inferior a la de los orbitales atómicos que los forman y, por tanto, favorecen los enlaces químicos que mantienen…
orbitales de enlaces que tienen una energía inferior a la de los orbitales atómicos que los forman y, por tanto, favorecen los enlaces químicos que mantienen… Decágono (categoría Polígonos por el número de lados)miden 144º o 4π/5{\displaystyle 4\pi /5} rad. Cada ángulo externo del decágono regular mide 36º o π/5{\displaystyle \pi /5} rad. P=n⋅t=10 t{\displaystyle…
Decágono (categoría Polígonos por el número de lados)miden 144º o 4π/5{\displaystyle 4\pi /5} rad. Cada ángulo externo del decágono regular mide 36º o π/5{\displaystyle \pi /5} rad. P=n⋅t=10 t{\displaystyle…- Inducción asimétrica (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)Pitzer) involucrando enlaces parciales (en los estados de transición) representa una fracción sustancial de la tensión entre enlaces completamente formados…
 Tensión mecánica (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)las tensiones mecánicas si se imagina un corte mediante un plano imaginario π que divida el cuerpo en dos partes. Para que cada parte estuviera en equilibrio…
Tensión mecánica (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)las tensiones mecánicas si se imagina un corte mediante un plano imaginario π que divida el cuerpo en dos partes. Para que cada parte estuviera en equilibrio…- y Hartree. [11] Los átomos forman a menudo enlaces entre ellos, dando lugar a moléculas. Estos enlaces deforman la nube de electrones de los átomos…
- que pretende proteger a la Tierra de la llegada de un asteroide llamado "π". El plan consiste en desplegar un grupo de nuevos supermisiles, llamados…
 Función zeta de Riemann (categoría Wikipedia:Artículos con enlaces externos rotos)donde B2k son los números de Bernoulli. De esta fórmula se obtiene que: ζ(2) = π²/6, ξ(4) = π4/90, ξ(6) = π6/945 etc. Para números impares no se conoce…
Función zeta de Riemann (categoría Wikipedia:Artículos con enlaces externos rotos)donde B2k son los números de Bernoulli. De esta fórmula se obtiene que: ζ(2) = π²/6, ξ(4) = π4/90, ξ(6) = π6/945 etc. Para números impares no se conoce… forman enlaces favorables. Si bien estos pueden ser frágiles, son bastante fuertes cuando se forma una gran red de estos enlaces. La capa más externa de cada…
forman enlaces favorables. Si bien estos pueden ser frágiles, son bastante fuertes cuando se forma una gran red de estos enlaces. La capa más externa de cada…- Kaón (categoría Wikipedia:Páginas con enlaces mágicos de ISBN)(leptónico, ratio de ramificación (RR) ~ 63%) π+π0{\displaystyle \pi ^{+}\pi ^{0}} (hadrónico, RR ~ 21%) π+π+π−{\displaystyle \pi ^{+}\pi ^{+}\pi ^{-}} (hadrónico…
- interacciones dipolo-dipolo, interacciones π, interacciones catión-π, apilamiento, química donante-aceptor y enlaces de halógeno. Además, el efecto hidrofóbico…
- número exagerado de decimales. Calculemos: x = A 3 = 100 π 3 {\displaystyle x={\sqrt[{3}]{A}}={\sqrt[{3}]{100\pi }}} Como comienzo, evaluamos 100 π {\displaystyle
- forma más de un enlace covalente, estos enlaces forman entre sí ángulos bien definidos. Por lo tanto los enlaces covalentes son dirigidos, además de saturables