Alkoholok: Egy vagy több, szén atomhoz kapcsolódó hidroxil csoportot tartalmazó szerves vegyületek
Az alkoholok egy vagy több hidroxilcsoportot (-OH) tartalmazó szerves vegyületek.
Az alkoholokban a hidroxilcsoport telített szénhidrogénhez kapcsolódik. Általános képletük: R-OH.

- Ez a szócikk a vegyületcsoportról szól. A közbeszédben az „alkohol” szó általában az etanolra utal, vagy az etanolt tartalmazó alkoholos italokra.
Az alkohol elnevezés az arab al-kuḥl (الكحل) szóból származik, eredeti jelentése finom antimon-szulfid por. Ezt használták az egyiptomi nők szemöldökfestésre, és a jó minőségű festékben nem voltak kitapintható szemcsék. Később a szó átvitt értelemben a „nem tapintható” jelentést kapta. Ilyenek az alkoholt tartalmazó italok, amelyekben nem lehet kitapintani a „lényeget”. Az alkohol vegyületeket sokféle néven nevezték magyar nyelven. A legrégibb magyar neve az égett bor volt, amely egyik nyersanyagára, a borra mutatott, de nevezték még boralék, borláng, borlél, borlelke, borer, borspiritus, borszesz néven is. Később a bor és szesz szavak összeforrtak, és alkohol értelmet kaptak. Az alcohol vini (a bor párlata) kifejezést a 16. században Paracelsus alkotta meg és abból állandósult az alkohol szó mai jelentése.
Szerkezete
Az alkoholok nevénél néha látható egy szám, valahogy így: 2-butanol. Ez a szám azt jelenti, hogy hányadik szénatomhoz kapcsolódik a hidroxilcsoport. az alkohol szerkezet lehet R-OH, R2-OH, végül pedig R3-OH.
Nevezéktan, típusok
Az alkoholok neve
Szabályos nevüket a megfelelő szénhidrogénlánc nevének végéhez illesztett -ol végződéssel képezzük. Három-, vagy több szénatomos alkoholoknál az -ol végződés előtt fel kell tüntetni annak a szénatomnak a számát, melyhez a hidroxilcsoport kapcsolódik. Így a CH3-CH(OH)-CH2-CH3 vegyület szabályos neve butan-2-ol. Egyes alkoholoknak csoportfunkciós és triviális neve is használatos.
Rendűség, értékűség
Az alkoholok rendűsége annak a szénatomnak a rendűségét adja meg, amelyikhez a hidroxilcsoport kapcsolódik. A rendűség megmutatja, hogy a hidroxilcsoporthoz kapcsolódó szénatom hány olyan kötést alakít ki, melyekkel másik szénatomhoz kapcsolódik. Az elsőrendű alkoholokban a hidroxilcsoporthoz kapcsolódó szénatom 1 másik szénatomhoz kapcsolódik. A másodrendűekben ugyanez a szénatom 2 másik szénatomhoz kapcsolódik, vagy egyhez, kétszeres kötéssel. Az alkoholok legfeljebb harmadrendűek lehetnek.
| Elsőrendű (primer) alkohol | Másodrendű (szekunder) alkohol | Harmadrendű (tercier) alkohol |
 |  | 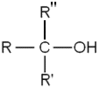 |
Az alkoholok értékűségét a bennük található hidroxilcsoportok száma határozza meg.
Típusok és képviselőik

- A nyílt láncú alkoholok (alkil-alkoholok, vagy alifás alkoholok) a leggyakoribb értelemben vett alkoholok. Ezek hidroxilcsoportja nem mutat savas jelleget, oldatuk semleges. Az alifás alkoholok közé tartozik a legismertebb alkohol, az etanol. Igen mérgező a metanol, más néven faszesz.
- Gyűrűs, de nem aromás alkoholok.
- A fenolok (aromás alkoholok, aril-alkoholok) az alkoholoktól különálló vegyületcsoportot alkotnak. A hidroxilcsoport közvetlenül aromás gyűrűhöz kapcsolódik, és savas jelleget mutat.
Fizikai tulajdonságok
A kis szénatomszámú egyértékű alkoholok színtelen, jellegzetes szagú folyadékok. A magasabb szénatomszámú alkoholok szilárdak. Olvadás- és forráspontjuk a megfelelő szénhidrogénekénél, aldehidekénél és ketonokénál magasabb, mivel a legerősebb intermolekuláris (másodrendű) kölcsönhatás, hidrogénkötés kialakítására képesek. A karbonsavakénál viszont alacsonyabb forrás-, ill. olvadásponttal rendelkeznek, mivel előbbiekkel szemben molekulánként csak 1 db hidrogénkötést tudnak létrehozni.
A kis szénatomszámú alkoholok poláris jellegük miatt jól elegyednek a vízzel, ez az alapja a különböző alkoholos italok készítésének. Magasabb szénatomszám esetén vízben nem oldódnak. Az összes alkohol jól oldódik etanolban és éterben.
A tiszta alkoholok, ill. azok tiszta vizes oldata nem vezetik az áramot, mivel az alkoholok vízben nem disszociálnak.
Az alkoholok általában annyi hidrogénkötést tudnak kialakítani, amennyi értékűek (pl. glicerin 3 hidrogénkötés, eritrit 4 hidrogénkötés)
Kémiai tulajdonságok
Az alkoholok vizes oldata első közelítésben semleges, így az alkoholok a Brönsted-féle savelmélet alapján nem számítanak sem savnak, sem bázisnak. Második közelítésben az alkohol vízben igen csekély mértékben disszociál, ez azonban a pH-t jelentősen nem befolyásolja.
Alkáli- és alkáliföldfémekkel redoxireakcióba lépnek, hidrogén képződése közben:
- 2 R-OH + 2 Na = 2 R-O- + 2 Na+ + H2
A képződő R-O- iont alkoholátionnak nevezzük.
Cseppfolyós alkoholokban szilárd kálium- vagy nátrium-hidroxidot oldva kálium- és nátrium-alkoholát képződik.
- R-OH + NaOH = R-ONa + H2O
Alkoholokat melegítve kb. 130 °C-on az alkoholnak megfelelő szimmetrikus éter és víz képződik:
- 2 R-OH = R-O-R + H2O
Magasabb hőmérsékleten, kb. 160 °C-on vízkilépéssel az alkohol láncának megfelelő alkén keletkezik:
- R-CH2-CH2-OH = R-CH═CH2 + H2O
Az alkoholok enyhe oxidáció hatásra (pl. forró réz-oxid) megfelelő oxovegyületté (a primer alkoholok aldehiddé, a szekunderek ketonná) alakulnak át:
- R-CH2OH + CuO = R-CH═O + Cu + H2O
Erősebb oxidációs hatásra megfelelő karbonsav, vagy szén-dioxid keletkezik.
Karbonsavakkal vízkilépéssel észtereket képeznek:
- R1-OH + R2-COOH ⇌ R2-COO-R1 + H2O
Előállítás
Az alkoholok előállíthatók telítetlen szénhidrogének vízaddíciójával, ill. alkoholátok vízben való oldásával:
- CH2═CH2 + H2O = CH3-CH2-OH
- R-ONa + H2O = R-OH + NaOH
Előfordulás, felhasználás
A természetben számos alkohol megtalálható az erjedő növényi anyagokban. Kötött állapotban a különböző gyümölcsök, viaszok, illóolajok tartalmazzák őket észtereik formájában. Az etil-alkoholt italok készítésére használják. A metanolt szerves oldószerként alkalmazzák.
Jegyzetek
Kapcsolódó szócikkek
- Az alkohol hatása az emberi szervezetre
- Az alkohol hatása az emberi szervezet hőveszteségének pótlására
- Alkoholfogyasztás
This article uses material from the Wikipedia Magyar article Alkoholok, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). A lap szövege CC BY-SA 4.0 alatt érhető el, ha nincs külön jelölve. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Magyar (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.