Αλκοόλες
Στη Χημεία, όμως, με την ονομασία «αλκοόλη» αναφέρεται οποιαδήποτε οργανική ένωση που περιέχει ένα ή περισσότερα υδροξύλια ή υδροξυομάδες (-OH), συνδεμένα με άτομο άνθρακα και μόνο εφόσον το υδροξύλιο είναι η κύρια χαρακτηριστική ομάδα της ένωσης.
Έτσι, για παράδειγμα το γαλακτικό οξύ (CH3CH(OH)COOH), που περιέχει υδροξύλιο, δεν θεωρείται αλκοόλη, αλλά καρβονικό οξύ (και πιο συγκεκριμένα υδροξυοξύ), διότι η κύρια χαρακτηριστική του ομάδα είναι το καρβοξύλιο (-COOH).


- *Το ουσιαστικό αλκοόλη στην καθομιλούμενη είναι συνώνυμο της αιθυλικής αλκοόλης, το κοινό οινόπνευμα. Για άλλες χρήσεις του όρου δείτε Αλκοόλη (αποσαφήνιση).
Ως χαρακτηριστική ομάδα, το υδροξύλιο έπεται για χαρακτηρισμό ως κύρια χαρακτηριστική ομάδα του καρβοξυλίου (-COOH), των άλλων όξινων ομάδων, όπως της σουλφοξυομάδας (-SO3H), του νιτριλίου (-CN), του καρβονυλίου (>CO) και αντίστοιχων ομάδων που περιέχουν άλλα στοιχεία και πολλαπλούς δεσμούς ταυτόχρονα. Προηγείται όμως όλων των υπόλοιπων χαρακτηριστικών ομάδων.
Ταξινόμηση
Το πρώτο κριτήριο ταξινόμησης των αλκοολών είναι η τυχόν παρουσία και δευτερευόντων χαρακτηριστικών ομάδων. Έτσι έχουμε π.χ. τις αμιναλκοόλες, αν έχουμε και αμινομάδες (-ΝΗ2, >NH, >N-), κ.τ.λ..
Το δεύτερο κριτήριο ταξινόμησης των αλκοολών είναι η τυχόν παρουσία περισσότερων της μιας ομάδας υδροξυλίου. Έτσι έχουμε π.χ. τις διόλες, τριόλες, κ.τ.λ..
Ειδικότερα στις αλκανόλες, δηλαδή άκυκλες κορεσμένες μονοσθενείς αλκοόλες, χωρίς καμμιά άλλη χαρακτηριστική ομάδα, διακρίνουμε τρεις υποκατηγορίες, ανάλογα με τον αριθμό των αλκυλίων που συνδέονται στο άτομο άνθρακα που φέρει το υδροξύλιο:
- Πρωτοταγείς αλκοόλες: Περιέχουν ένα (1) αλκύλιο και δύο (2) άτομα υδρογόνου στο άτομο του άνθρακα που συνδέεται με το υδροξύλιο. Κατ' εξαίρεση, συμπεριλαμβάνεται σ' αυτές και η μεθανόλη, που περιέχει τρία (3) άτομα υδρογόνου στο μοναδικό της άτομο άνθρακα. Χαρακτηριστική ιδιότητα αυτών είναι η ικανότητα να οξειδώνονται σε αλδεΰδες και κατόπιν σε καρβοξυλικά οξέα.
- Δευτεροταγείς αλκοόλες: Περιέχουν δύο αλκύλια και ένα (1) άτομο υδρογόνου στο άτομο του άνθρακα που συνδέεται με το υδροξύλιο. Χαρακτηριστική ιδιότητα αυτών είναι η ικανότητα να οξειδώνονται σε κετόνες.
- Τριτοταγείς αλκοόλες: Περιέχουν τρία (3) αλκύλια και κανένα (0) άτομο υδρογόνου στο άτομο του άνθρακα που συνδέεται με το υδροξύλιο. Χαρακτηριστική ιδιότητα αυτών είναι η ικανότητα να μην οξειδώνονται, παρά μόνο κάτω από πολύ έντονες οξειδωτικές συνθήκες, οπότε και διασπάται η ανθρακική αλυσίδα τους.
- Η παρουσία άλλων υδροξυομάδων ή και άλλων χαρακτηριστικών ομάδων συχνά τροποποιεί αλλά συνήθως δεν αναιρεί την παραπάνω κατηγοριοποίηση και τις χαρακτηριστικές της ιδιότητες.
- Σε διόλες (πολυόλες, γενικά), αν συνυπάρχουν πρωτοταγή και δευτεροταγή υδροξύλια, τα δευτεροταγή οξειδώνονται (συνήθως) ταχύτερα και επομένως είναι συνήθως απομονώσιμες οι υδροξυκετόνες, που παράγονται ως προϊόντα μερικής οξείδωσης πολυολών.
Ονοματολογία
Η ονομασία «αλκοόλη» προέρχεται από την αραβική λέξη «αλ κουνούλ» ή «αλ κου(χ)λ» (al-Kunul ή Al-Kuhl), με αρχική σημασία «λεπτή σκόνη» και που κατέληξε να σημαίνει άρωμα. Πολύ αργότερα η λέξη χρησιμοποιήθηκε για τα οινοπνεύματα ως "alcool vini" με τελική κατάληξη τις αλκοόλες.
Για την ονοματολογία των αλκοολών αναπτύχθηκε ένα σύνθετο σύστημα βασισμένο κυρίως στον όρο «καρβυνόλη», που είναι συνώνυμος του (πιο σύγχρονου) όρου μεθανόλη, και που πρωτοδημιουργήθηκε τον 19ο αιώνα από τον Γερμανό χημικό Χέρμαν Κόλμπε. Έτσι όλες οι αλκοόλες φέρονται με κατάληξη -όλη.
Έτσι η ονομασία κάθε αλκοόλης προέρχεται από την ονομασία του κύριου υδρογονάνθρακα (που κυριαρχεί στην αλυσίδα του μορίου της) όπου η κατάληξη «-ιο», αντικαθίσταται με την «-όλη», π.χ. μεθάνιο → μεθανόλη (ή καρβυνόλη), αιθάνιο → αιθανόλη, προπάνιο → προπανόλη, βουτένιο → βουτενόλη, κ.τ.λ..
Αν υπάρχουν ισομερή θέσης ως προς τη θέση του υδροξυλίου, τότε της ονομασίας προηγείται ένας αριθμός που δηλώνει τον αύξοντα αριθμό του ατόμου άνθρακα της κύριας ανθρακικής αλυσίδας (της πολυπλοκότερης που φέρει την υδροξυλομάδα) στον οποίο συνδέεται η υδροξυλομάδα. Π.χ. 1-βουτανόλη, 2-βουτανόλη, κ.τ.λ..
Η τυχόν παρουσία περισσότερων της μιας υδροξυομάδων σημειώνεται με ένα πρόθεμα -δι-, -τρι-, κ.τ.λ. μεταξύ του ονόματος του αντίστοιχου υδρογονάνθρακα και της κατάληξης -όλη. Π.χ. αιθανοδιόλη, προπανοτριόλη, κ.τ.λ.. Αν είναι αναγκαίο προτίθενται και οι αντίστοιχοι αριθμοί θέσης των υδροξυομάδων. Π.χ. 1,3-βουτανοδιόλη.
Αν συνυπάρχουν πολλαπλοί δεσμοί, τότε οι αριθμοί θέσης αυτών προτίθενται στο όνομα της αλκοόλης, ενώ ο αριθμός θέσης των υδροξυλίων σημειώνεται ενδιάμεσα στο όνομα της αλκοόλης. Π.χ. 2-προπεν-1-όλη.
Αν συνυπάρχουν δευτερεύουσες χαρακτηριστικές ομάδες, αυτές μπάίνουν ως προθέματα μπροστά από το κυρίως όνομα της αλκοόλης, με τους αριθμούς θέσης τους, αν είναι απαραίτητο. Π.χ. 2-αμιναιθανόλη.
Τέλος, αν οι διακλαδώσεις είναι πολύπλοκες, μπορεί για λόγους απλούστευσης της ονομασίας κάποιες υδροξυομάδες ή υδροξυλαλκυλομάδες (HOCxHy-), να τεθούν μπροστά και αυτές ως υποκαταστάτες.
Αλκοόλες με εμπειρικές ονομασίες
- Μεθανόλη ή ξυλόπνευμα ή μεθυλική αλκοόλη ή καρβυνόλη: CH3OH ή MeOH
- Αιθανόλη ή αλκοόλη, ή οινόπνευμα ή αιθυλική αλκοόλη: CH3CH2OH ή EtOH
- Αιθενόλη ή βινυλική αλκοόλη: CH2=CHOH ή ViOH
- 2-προπεν-1-όλη ή αλλυλική αλκοόλη: CH2=CHCH2OH ή ViCH2OH
- 2-προπιν-1-όλη ή προπαργυλική αλκοόλη: HC≡CCH2OH
- 1,2-αιθανοδιόλη ή αιθυλενογλυκόλη ή γλυκόλη: HOCH2CH2OH
- 1,2,3-προπανοτριόλη ή γλυκερόλη ή γλυκερίνη: HOCH2CH(OH)CH2OH
- 1,2,3,4-βουτανοτετραόλη ή ερυθριτόλη ή ερυθρίτης: HOCH2CH(OH)CH(OH)CH2OH
- 2,3-διμεθυλό-2,3-βουτανοδιόλη ή πινακόλη: (CH3)2C(OH)C(OH)(CH3)2
- Μεθοξυαιθανόλη ή μεθυλοκελλοσόλβη: CH3OCH2CH2OH ή MeOCH2CH2OH
- Φαινόλη: PhOH
- Βενζυλική αλκοόλη: PhCH2OH
- Κρεσόλες: CH3C6H4OH.
Παραγωγή
Βιομηχανικές μέθοδοι
- Μερικές αλκοόλες απομονώνονται ως προϊόντα ή παραπροϊόντα ζυμώσεων.
- Με υδρόλυση (δείτε παρακάτω) αλκενίων, που συνήθως είναι προϊόντα πυρόλυσης αργού πετρελαίου ή φυσικού αερίου.
- Με καταλυτική οξείδωση αλκανίων, που συνήθως είναι προϊόντα διύλισης του αργού πετρελαίου.
- Η γλυκερίνη είναι προϊόν υδρόλυσης των τριγλυκεριδίων, δηλαδή των κυριότερων λιπών.
Εργαστηριακές ή εναλλακτικές μέθοδοι
Με οργανομαγνησιακές ενώσεις
1. Οι πρωτοταγείς αλκοόλες παράγονται με επίδραση μεθανάλης σε αλκυλομαγνησιοαλογονίδια:

2. Οι δευτεροταγείς αλκοόλες παράγονται με επίδραση αλδεΰδης σε αλκυλομαγνησιοαλογονίδια:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
3. Οι τριτοταγείς αλκοόλες παράγονται με επίδραση κετόνης σε αλκυλομαγνησιοαλογονίδια:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
Με αναγωγή καρβονυλικών ενώσεων ή καρβονικών οξέων
1. Οι πρωτοταγείς αλκοόλες παράγονται με αναγωγή των αντίστοιχων αλδεϋδών ή καρβονικών οξέων:
- α. Από αλδεύδες

- β. Από καρβονικά οξέα

ή
2. Οι δευτεροταγείς αλκοόλες παράγονται με αναγωγή των αντίστοιχων κετονών

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
3. Οι τριτοταγείς αλκοόλες δεν παράγονται μ' αυτήν τη μέθοδο.
4. Με χρήση μεταλλικού νατρίου σε κετόνες παίρνουμε:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
Με υδρόλυση αλογονοπαραγώγων
1. Με αραιό διάλυμα NaOH, όταν η δομή του αλογονοπαραγώγου δεν επιτρέπει την απόσπαση υδραλογόνου προς παραγωγή αλκενίων. Π.χ.:

2. Αν υπάρχει μεγάλη πιθανότητα απόσπασης προτιμάται το AgOH, δηλαδή υδατικό εναιώρημα Ag2O:

3. Με υδατικό διάλυμα αλάτων καρβονικών οξέων:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
Από αλκένια
1. Με επίδραση θειικού οξέος και μετά με νερό (ενυδάτωση):

- Η αντίδραση ακολουθεί τον κανόνα Markownikow, δηλαδή το υδροξύλιο ενώνεται με το πιο ηλεκτροθετικό, συνήθως με το πιο υποκατατεστημένο άτομο άνθρακα. Π.χ.:

2. Με επίδραση βορανίου και μετά με υπεροξείδιο του υδρογόνου:

- Η αντίδραση φαίνεται εδώ ακολουθεί τον κανόνα αντί-Markownikow, δηλαδή το υδροξύλιο ενώνεται με το λιγότερο ηλεκτροθετικό, συνήθως με το λιγότερο υποκατατεστημένο άτομο άνθρακα. Π.χ.:

3. Με επίδραση αραιού διαλύματος υπερμαγγανικού κσλίου ή μίγματος υπεροξειδίου του υδρογόνου και καρβονικού οξέος. Παραγωγή διόλης τύπου -1,2:

ή
Από κυκλοπροπάνια
- Το κυκλοπροπάνιο και τα υποκατεστημένα παράγωγά του (κυκλοπροπάνια) δείνουν ανυιδράσεις κυκλοπροσθήκης. Για λόγους απλότητας παρακάτω θα χρησιμοποιήσουμε ως παράδειγμα κυκλοπροπανίων το μεθυλοκυκλοπροπάνιο:
1. Με επίδραση θειικού οξέος και μετά με νερό (ενυδάτωση):
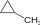

- Η αντίδραση ακολουθεί τον κανόνα Markownikow, δηλαδή το υδροξύλιο ενώνεται με το πιο ηλεκτροθετικό, συνήθως με το πιο υποκατατεστημένο άτομο άνθρακα.
2. Με επίδραση βορανίου και μετά με υπεροξείδιο του υδρογόνου:
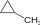


- Η αντίδραση φαίνεται εδώ ακολουθεί τον κανόνα αντί-Markownikow, δηλαδή το υδροξύλιο ενώνεται με το λιγότερο ηλεκτροθετικό, συνήθως με το λιγότερο υποκατατεστημένο άτομο άνθρακα.
3. Με επίδραση αραιού διαλύματος υπερμαγγανικού καλίου ή μίγματος υπεροξειδίου του υδρογόνου και καρβονικού οξέος. Παραγωγή διόλης τύπου -1,3:
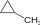

ή
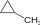

Με υδρόλυση εστέρων

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
Με επίδραση νιτρώδους οξέος σε πρωτοταγείς αμίνες

- Επειδή το νιτρώδες οξύ δε διατηρείται εύκολα, συνήθως παράγεται επί τόπου:

Από άλλες αλκοόλες
1. Με ανοικοδόμηση της ανθρακικής αλυσίδας:

- Από εδώ και πέρα διακρίνουμε δυο μεθόδους:
- α.

- Από εδώ και πέρα διακρίνουμε δυο υπομεθόδους:
- α1.

- α2.

- β.

 +
+ 
2. Με αποικοδόμηση της ανθρακικής αλυσίδας:



- Επειδή το υποβρωμιούχο νάτριο δε διατηρείται εύκολα, συνήθως παράγεται επί τόπου:

Αντιδράσεις αλκοολών
Όξινος χαρακτήρας
- Οι αλκοόλες δείνουν μερικές αντιδράσεις που είναι χαρακτηριστικές για τα οξέα, όπως ο σχηματισμός αλκοολικών αλάτων. Η σχετική τους οξύτητα είναι: H2Ο > ROH > RC≡CH > NH3 > RH
1. Αντιδρούν με αλκάλια:

2. Αντιδρούν με νατραμίδιο:

3. Αντιδρούν με άλατα 1-αλκινίων:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
4. Αντιδρούν με αλκυλομαγνησιοαλογονίδια:

Βασικός χαρακτήρας
- Οι αλκοόλες αντιδρούν και με διάφορα οξέα και όξινα άλατα. Δεν σχηματίζουν όμως άλατα μαζί τους, όπως οι βάσεις. Τα αποτελέσματα των αντδράσεων αυτών ποικίλλουν:
1. Πυρηνόφιλη υποκατάσταση με υδραλογόνα:
- α. Με υδροϊώδιο, χωρίς βοήθεια:

- β. Με το υδροχλώριο ή υδροβρώμιο, με καταλύτη:

2. Αφυδάτωση με θειικό οξύ:
- α. Ενδομοριακή προς αλκένια:

- β. Διαμοριακή προς αιθέρες:

3. Εστεροποίηση με καρβονικά και άλλα οξέα:
- α. Με καρβονικά οξέα:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
- β. Με ανόργανα οξέα, όπως π.χ. το φωσφορικό οξύ:

4. Με όξινα άλατα, όπως τα χλωριωτικά-βρωμιωτικά μέσα:
- α. Με θειονυλοχλωρίδιο (SOCl2):

- β. Με πενταχλωριούχο φωσφόρο (PCl5):

- γ. Με τριχλωριούχο φωσφόρο (PCl3):

- δ. Με τριβρωμιούχο φωσφόρο (PBr3):

5. Πινακολική μετάθεση:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
- Πραγματοποιείται από τις πινακόλες, δηλαδή τις τριτοταγείς και ως προς τα δυο άτομα άνθρακα που φέρουν υδροξυομάδες 1,2-διόλες.
Οξείδωση
1. Οι πρωτοταγείς αλκοόλες μόνο, με υπερμαγγανικό κάλιο, προς καρβονικά οξέα:

2. Οι πρωτοταγείς αλκοόλες μόνο, με διχρωμικό κάλιο, προς αλδεΰδες:

3. Οι δευτεροταγείς αλκοόλες μόνο, με διχρωμικό κάλιο, προς κετόνες:

- Όπου τα R δεν είναι υποχρεωτικά τα ίδια.
- Οι τριτοταγείς αλκοόλες οξειδώνονται μόνο με πολύ δραστικές συνθήκες, οπότε διασπάται η ανθρακική τους αλυσίδα.
4. Οι 1,2-διόλες με HIO4. Π.χ.:

- Οι τριτοταγείς έστω και ως προς το ένα άτομο άνθρακα που φέρει υδροξυομάδα δίνουν κετόνες αντί αλδεΰδες.
Πηγές
- Λεξικό Βιολογίας Collins, σελ. 42, Εκδόσεις Ι. Φλώρος, Αθήνα
- Λεξικό των Επιστημών Neil Ardley σ. 37, εκδ. ΕΡΕΥΝΗΤΕΣ Αθήνα
- Εγκυκλοπαίδεια Πάπυρος Λαρούς Μπριτάννικα τ. 7ος, σσ. 7-8
- Γ. Βάρβογλη, Ν. Αλεξάνδρου: Οργανική Χημεία, Αθήνα 1972
- Α. Βάρβογλη: Χημεία Οργανικών Ενώσεων, παρατηρητής, Θεσσαλονίκη 1991
- SCHAUM'S OUTLINE SERIES, ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ, μετφ. Α. Βάρβογλη, 1999
- Ν.Α. Πετάση: Ασκήσεις και προβλήματα Οργανικής Χημείας, 1982
- Δημήτριου Ν. Νικολαΐδη: Ειδικά μαθήματα Οργανικής Χημείας, Θεσσαλονίκη 1983
Αναφορές και σημειώσεις
Πλήρως μετουσιωμένη αιθυλική αλκοόλη, καύσιμη ύλη για τζάκια https://www.e-biofire.gr/plhrofories-vioaithanoli.html
This article uses material from the Wikipedia Ελληνικά article Αλκοόλες, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Το περιεχόμενο είναι διαθέσιμο υπό CC BY-SA 4.0 εκτός αν αναφέρεται διαφορετικά. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Ελληνικά (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.