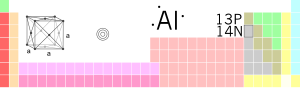
Aluminio
L'aluminio ye un elemento quimico de simbolo Al y numero atomico 13.
| Iste articlo ye en proceso de cambio enta la ortografía oficial de Biquipedia (la Ortografía de l'aragonés de l'Academia Aragonesa d'a Luenga). Puez aduyar a completar este proceso revisando l'articlo, fendo-ie los cambios ortograficos necesarios y sacando dimpués ista plantilla. |
| Aluminio | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||
| Información cheneral | |||||||||||||||||||||||||
| Nombre, simbolo, numero | Aluminio, Al, 13 | ||||||||||||||||||||||||
| Serie quimica | Metals d'o bloque p | ||||||||||||||||||||||||
| Grupo, periodo, bloque | 13, 3, p | ||||||||||||||||||||||||
| Color | Griso | ||||||||||||||||||||||||
| Peso atomico | 26.9815386(13) g·mol−1 | ||||||||||||||||||||||||
| Configuración electronica | [Ne] 3s2 3p1 | ||||||||||||||||||||||||
| Electrons por capa | 2, 8, 3 | ||||||||||||||||||||||||
| Propiedaz fisicas | |||||||||||||||||||||||||
| Fase | Solido | ||||||||||||||||||||||||
| Densidat (a t.a.) | 2.70 g·cm−3 | ||||||||||||||||||||||||
| Densidat en liquido en o p.f. | 2.375 g·cm−3 | ||||||||||||||||||||||||
| Punto de fusión | 933.47 K (660.32 °C, 1220.58 °F) | ||||||||||||||||||||||||
| Punto d'ebullición | 2792 K (2519 °C, 4566 °F) | ||||||||||||||||||||||||
| Entalpía de fusión | 10.71 kJ·mol−1 | ||||||||||||||||||||||||
| Entalpía de vaporización | 294.0 kJ·mol−1 | ||||||||||||||||||||||||
| Calor especifica | (25 °C) 24.200 J·mol−1·K−1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Propiedaz atomicas | |||||||||||||||||||||||||
| Estructura cristalina | Cubica centrata en as caras 0.40494 nm | ||||||||||||||||||||||||
| Estatos d'oxidación | 3, 2, 1 (Oxido anfoterico) | ||||||||||||||||||||||||
| Electronegatividat | 1.61 (escala de Pauling) | ||||||||||||||||||||||||
| Enerchías d'ionización (mas) | 1ª: 577.5 kJ·mol−1 | ||||||||||||||||||||||||
| 2ª: 1816.7 kJ·mol−1 | |||||||||||||||||||||||||
| 3ª: 2744.8 kJ·mol−1 | |||||||||||||||||||||||||
| Radio atomico | 125 pm | ||||||||||||||||||||||||
| Radio atomico (calc.) | 118 pm | ||||||||||||||||||||||||
| Radio covalent | 118 pm | ||||||||||||||||||||||||
| Atra información | |||||||||||||||||||||||||
| Ordenación magnetica | Paramagnetico | ||||||||||||||||||||||||
| Resistividat electrica | (20 °C) 26.50 nΩ·m | ||||||||||||||||||||||||
| Conductividat termal | (300 K) 237 W·m−1·K−1 | ||||||||||||||||||||||||
| Dilatación | (25 °C) 23.1 µm·m−1·K−1 | ||||||||||||||||||||||||
| Velocidat d'o sonito | (t.a.) 5000 m·s−1 | ||||||||||||||||||||||||
| Modulo d'elasticidat | 70 GPa | ||||||||||||||||||||||||
| Mod. elast. transversal | 26 GPa | ||||||||||||||||||||||||
| Modulo de compresión | 76 GPa | ||||||||||||||||||||||||
| Coeficient de Poisson | 0.35 | ||||||||||||||||||||||||
| Dureza Mohs | 2.75 | ||||||||||||||||||||||||
| Dureza Vickers | 167 MPa | ||||||||||||||||||||||||
| Dureza Brinell | 245 MPa | ||||||||||||||||||||||||
| Numero CAS | 7429-90-5 | ||||||||||||||||||||||||
| Isotopos mas estables | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Ye l'elemento metalico mas abundante en crosta terrestre, con un 8,13 % d'abundancia. O primer fisico en aillar-lo estió o cientifico danés Hans Christian Oersted.
Debito a que ye lichero, a la suya conductividat electrica, resistencia a la corrosión y baixo punto de fusión fan que sía un material ideyal ta muitas aplicacions, especialment l'aeronautica; manimenos, a gran cantidat d'enerchía que s'aprecisa ta la obtención d'o metal a partir d'os oxidos dificulta a suya mayor utilización; encara que se puet compensar en parti por o baixo coste en reciclar-lo, a suya larga vita útil y a estabilidat d'o suyo pre.
O primer lingote fabricato en Espanya estió en l'anyo 1927 en a interpresa Aluminio Español S.A., en a localidat aragonesa de Samianigo.
Etimolochía
En o sieglo XIX con o desarrollo d'a fisica y quimica s'identificó l'elemento present en l'alum y o britanico Sir Humprey Davy proposó a denominación d'aluminium en l'anyo 1809.
Caracteristicas chenerals

L'aluminio ye un metal lichero, tovo pero resistent y d'aspecto griso archent. A suya densidat ye alto u baixo un tercio d'a de l'acero u de l'arambre, ye muit maleable y dúctil y apto ta estar mecanizato y ta a fundición . A causa d'a suya alta calor d'oxidación se forma a escape, en presencia d'aire, una fina capa superficial d'oxido d'aluminio (Al2O3) impermeable y adherent que atura o proceso d'oxidación proporcionant-le resistencia a la corrosión y durabilidat. Ista capa protectora, puet estar enamplata por electrolisi en presencia d'oxalatos.
L'aluminio, tien caracteristicas anfotericas, ye decir que se disuelve en acidos, formando sals d'aluminio y en bases fuertes, formando aluminatos con l'anión [Al(OH)4]-, liberando hidrocheno.
O prencipal y cuasi unico estato d'oxidación de l'aluminio ye o +III, como ye d'asperar por a confeguración electronica que presenta, con tres electrons en a capa de valencia.
Producción

A extracción de l'aluminio se fa dende o mineral dito bauxita, que recibe o suyo nombre d'o nombre en francés d'a localidat occitana de Baus (Les Baux en francés), que ye o puesto a on se fació a suya primera extracción. Actualment os prencipales chacimientos d'iste mineral se trobal en os países d'a mar Caribe, Australia, Brasil y Africa en estar en ixos lugars a on a extracción de l'aluminio dende a bauxita se fa con mas facilidat. A bauxita ye un mineral rico en aluminio, d'entre un 20% y un 30% d'a suya masa, frente a o 10% u 20% que tienen os silicatos aluminicos d'archilas y carbons. Ye un aglomerato de cuantos compuestos que contién caolinita, cuarz, oxidos de fierro y titania, y a on l'aluminio se i presenta en cuantas formas hidroxidas como a gibbsita Al (OH)3, a boehmita AlOOH y o diasporo AlOOH.
A obtención de l' aluminio se fa en dos fases: aa extracción de l'alumina dende a bauxita (proceso Bayer) y a extracción de l'aluminio dende ista zaguera por electrolisi. Cuatre toneladas de bauxita producen dos toneladas d'alumina y, en zagueras, nomás que una d'aluminio. O proceso Bayer prencipia con o triturato d'a bauxita y con o suyo lavato con una solución calient d'hidroxido de sodio a alta presión y temperatura. A sosa disuelve os compuestos de l'aluminio, que en trobar-se en un meyo muit basico, s'hidratan:
- Al(OH)3 + OH- + Na* → Al(OH)4- + Na*
- AlO(OH)2 + OH- + H2O + Na* → Al(OH)4- + Na*
Os materiales no aluminicos se deseparan por decantación. A solución caustica de l'aluminio se refreda dimpués ta recristalizar o hidroxido y deseparar-lo d'a sosa, que se recupera ta poder tornar a fer-la servir. Ta rematar, se calcina o hidroxido d'aluminio a temperaturas amanatas a 1000 °C, ta formar l'alumina.
- 2 Al(OH)3 → Al2O3 + 3 H2O
L'oxido de aluminio que s'ha obteniu d'ixa maneta tién un punto de fusión muit alto (2000 °C) que fa imposible someter-lo a un proceso d'electrolisi. Ta evitar-lo, se disuelve en un banyo de criolita, obtenindo asinas una mezcla eutectica con un punto de fusión de 900 °C. Contino se fa a electrolisis, en sumerchindo en a cuba uns electrodos de carbono (tanto l'ánodo como o cátodo), preparatos en horizontal. Ta cada tonelada d'aluminio cal entre 17 y 20 MWh d'enerchía, y consume en o proceso 460 kg de carbonio, que ye asinas entre un 25% y un 30% d'o pre final d'o producto, cosa que fa que l'aluminio sía asinas uno d'os metals mas caros d'obtener. De feito, se son buscando procesos alternativos menos costosos que o proceso electrolítico. L'aluminio obtenito tién una pureza de entre o 99,5% y o 99,9%, estando as impurezas mas que mas de fierro y silicio principalmente. Dende as cubas pasa a o furno, a on se purifica por meyo de l'adición d'un fundent u se fa l'aliación con atros metals ta obtener materials con propiedaz especificas. Dimpués se vierte en moldes u s'en fan lingoz u chapas.
Tabla de produccions por continent
| Anyo | Africa | America d'o Norte | America d'o Sud | Asia | Europa y Rusia | Oceanía | Total |
|---|---|---|---|---|---|---|---|
| 1973 | 249 | 5.039 | 229 | 1.439 | 2.757 | 324 | 10.037 |
| 1978 | 336 | 5.409 | 413 | 1.126 | 3.730 | 414 | 11 428 |
| 1982 | 501 | 4.343 | 795 | 1.103 | 3.306 | 548 | 10.496 |
| 1987 | 573 | 4.889 | 1.486 | 927 | 3.462 | 1.273 | 12.604 |
| 1992 | 617 | 6.016 | 1.949 | 1.379 | 3.319 | 1.483 | 14.763 |
| 1997 | 1.106 | 5.930 | 2.116 | 1.910 | 6.613 | 1.804 | 19.479 |
| 2003 | 1.428 | 5.945 | 2.275 | 2.457 | 8.064 | 2.198 | 21.935 |
| 2004 | 1.711 | 5.110 | 2.356 | 2.735 | 8.433 | 2.246 | 22.591 |
| Producción d'aluminio en millons de toneladas. Fuent: International Aluminium Association. | |||||||
Aplicacions

En l'antigüedat se feba servir o compuesto d'aluminio dito alum en tintorería y medicina.
Ya sía considerando a cantidat u a valura d'o metal emplegato, l'uso de l'aluminio sobrepuya a o de cualsiquier atro fueras de l'acero, y ye un material important en a-saber-las actividaz economicas. L'aluminio puro ye tovo y fráchil, pero as suyas aliacions con chicotas cantidaz d'arambre, manganés, silicio, magnesio y atros elementos presentan una gran variedat de caracteristicas adecuatas a las mas diversas aplicacions. Istas chicotas aliacions constituyen o component prencipal de muitos components d'os avions y codetes, en que o peso ye un factor critico.
Cuan s'evapora aluminio en o vueito, forma un revestimento que reflecta tanto a luz visible com a infrarroya. Amás a capa d'oxido que se forma impide o deterioramiento d'o recubrimiento, por ista razón s'ha emplegato ta revestir os mirallos de telescopios, en substitución de l'archent.
Dada a suya gran reactividat quimica, finament polvorizato s'usa como combustible solido de codetes; en bels explosivos, como anodo de sacrificio y en procesos d'aluminotermia ta a obtención de metals.
Atros usos de l'aluminio metalico son:
- Transporte, como material estructural en avions, automóbils, tanques, superestructuras de vaixiellos, blindaches, etc.
- Embalache; papel d'aluminio, tetrabriks, etc.
- Construcción; finestras, puertas, bastidas estructurals, etc.
- Biens de consumo; aines de cocina, ferramientas, etc.
- Transmisión electrica. Encara que a suya conductividat electrica ye nomás d'o 60% de la d'o coure a suya mayor lichereza permite una mayor deseparación entre as torres d'alta tensión, disminuindo os costes d'a infraestructura.
- Recipients criochenicos (dica -200 °C), ya que no presenta temperatura de transición de dúctil a fráchil como l'acero, y la tenacidat de l'aluminio contina estando buena a baixas temperaturas.
- Material de calderería; radiadors,...
Tamién s'emplegan compuestos d'aluminio en:
- As sals d'aluminio d'os acidos grasos (p.eix. o estearato d'aluminio) fan parti d'o napalm.
- Os hidruros complexos d'aluminio son reductors útils en sintesi organica.
- Os haluros d'aluminio tienen caracteristicas d'acido de Lewis y son emplegatos como tals, como catalizadors y como reactivos auxiliars.
- Os aluminosilicatos son un tipo important de mineral. Fan parti d'as archilas y son a base de muitas ceramicas.
- Adhibir aditivos d'oxido d'aluminio u aluminosilicatos a vidres, fa variar as propiedaz termicas, mecanicas y opticas d'istos.
- O corindón (Al2O3) ye emplegato como abrasivo. Bellas variants d'iste, como o rubí y o zafir s'emplegan en choyería como piedras preciosas.
aliacions d'aluminio:
- Duraluminio
Toxicidat
Iste metal ha estato considerato mientres muitos anyos como innocuo ta os sers humans. Debito a ista suposición s'han fabricato de forma masiva ainas d'aluminio ta cocinar alimentos, envases ta alimentos, y papel d'aluminio ta o embalache d'alimentos frescos. Manimenos, o suyo impacto sobre os sistemas biolochicos ha estato obchecto de muita controversia en as decadas pasatas y una profusa investigación ha contrimostrato que puet producir efectos adversos en plantas, animals acuaticos y sers humans.
A exposición a l'aluminio por un regular no ye perchudiciosa, pero a exposición a altos nivels puet causar serios problemas ta la salut. A exposición a l'aluminio se produce prencipalment cuan:
- Se consumen merecinas que contienen altos nivels d'aluminio.
- S'inhala polvo d'aluminio que sía en a zona de treballo.
- Se vive a on se quita u procesa aluminio.
- Se colocan vacunas que contienen aluminio.
Cualsiquier persona se puet intoxicar con aluminio u os suyos derivatos, pero bellas personas son mas propensas a desembolicar toxicidat por l'aluminio.
Vinclos externos
 Se veigan as imáchens de Commons sobre Aluminio.
Se veigan as imáchens de Commons sobre Aluminio.- (es) Pres historicos de l'aluminio, seguntes o FMI.
- (es) Historia d'a industria de l'aluminio.
Referencias
This article uses material from the Wikipedia Aragonés article Aluminio, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). O texto ye disponible baixo a Creative Commons Attribution/Share-Alike License; puede que sigan d'aplicación atros termins. Se veiga as Condicions d'uso ta más detalles. Wikipedia ye una marca rechistrada d'a Wiki Du học, una organización sin animo de lucro. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Aragonés (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.