Linalool: Gruppe von organischen Stereoisomeren, Naturstoffe, Duftstoffe
Linalool ist eine organisch-chemische Verbindung aus der Stoffgruppe der acyclischen Monoterpen-Alkohole.
Linalool ist ein Naturstoff mit frischem, maiglöckchenähnlichem Geruch.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
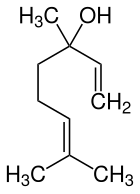 | |||||||||||||||||||
| Vereinfachte Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Linalool | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C10H18O | ||||||||||||||||||
| Kurzbeschreibung | farblose, nach Maiglöckchen riechende Flüssigkeit | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 154,25 g·mol−1 | ||||||||||||||||||
| Aggregatzustand | flüssig | ||||||||||||||||||
| Dichte | 0,86 g·cm−3 (20 °C) | ||||||||||||||||||
| Schmelzpunkt | <−74 °C | ||||||||||||||||||
| Siedepunkt | 198–200 °C [(S)-(+)-Linalool] | ||||||||||||||||||
| Dampfdruck |
| ||||||||||||||||||
| Löslichkeit | schlecht in Wasser (1,59 g·l−1 bei 20 °C) | ||||||||||||||||||
| Brechungsindex | 1,4616 (20 °C) | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Isomere
Die Substanz hat ein stereogenes Zentrum am Kohlenstoffatom der Position 3 und tritt somit in Form zweier Enantiomere auf: Licareol [(R)-(−)-Linalool] und Coriandrol [(S)-(+)-Linalool]. Es ist isomer zu Nerol/Geraniol wie auch zu Pinanol, Borneol, Myrcenol und Dihydrocarveol.
| Isomere von Linalool | ||
| Name | (S)-(+)-Linalool | (R)-(−)-Linalool |
| Andere Namen | Coriandrol | Licareol |
| Strukturformel |  |  |
| CAS-Nummer | 126-90-9 | 126-91-0 |
| 78-70-6 (unspez.) | ||
| EG-Nummer | 204-810-7 | 204-811-2 |
| 201-134-4 (unspez.) | ||
| ECHA-Infocard | 100.004.374 | 100.004.375 |
| 100.001.032 (unspez.) | ||
| PubChem | 67179 | 443158 |
| 6549 (unspez.) | ||
| Wikidata | Q27105233 | Q27105200 |
| Q410932 (unspez.) | ||
Vorkommen
Linalool ist Bestandteil vieler ätherischer Öle und kommt dort oft als Hauptbestandteil vor. So enthält das Shuiöl aus dem Kampherbaum 80–85 %, das Korianderöl 60–70 % Linalool. Es kommt im Sternanis, Anis-Duftnessel, Bay, Hopfen, Muskat, Ingwer, Bohnenkraut, Zimt, Basilikum, Echtem Lorbeer, Pfefferminze, Acker-Minze, Majoran, Thymian, Oregano, schwarzen Pfeffer, Safran, Hanf und anderen Gewürzpflanzen vor.
- Kampher
- Koriander
- Sternanis
- Anis-Duftnessel
- Hopfen
- Muskatnuss
Auch als Ester (Linalylacetat) und als Linalooloxid findet es sich in vielen ätherischen Ölen. Linalool gehört auch zu den Aromen im Wein. Mit einem Geruchsschwellenwert von 0,025 Milligramm pro Liter ist es eine wichtige Komponente des Muskateller-Bouquets.
Gewinnung und Darstellung
Nach Schätzungen wurden im Jahr 2000 weltweit etwa 12.000 Tonnen Linalool industriell hergestellt. Die natürliche Produktion übertrifft die industrielle aber um ein Vielfaches.
Zur Synthese wird Methylheptenon ethinyliert. Das entstehende Dehydrolinalool wird durch eine partielle Hydrierung zum Linalool reduziert. Diese Synthese gelang erstmals Leopold Ruzicka und Virgilio Fornasir 1919.

Eine zweite mögliche Syntheseroute geht vom α-Pinen aus. Dieses wird zum cis-Pinan hydriert und an der Luft zu cis- bzw. trans-Pinanhydroperoxid oxidiert. Das Hydroperoxid wird reduktiv zum Gemisch aus cis- oder trans-Pinanol aufgearbeitet, das destillativ getrennt werden kann. Bei Temperaturen von über 500 °C wird cis-Pinanol dann zum Coriandrol und trans-Pinanol zum Licareol isomerisiert.

Eigenschaften
Linalool ist eine klare, farblose Flüssigkeit. Coriandrol riecht seifig-korianderartig, Licareol holzig-lavendelartig. Der Geruch des Racemats wird als angenehmer, leicht erfrischender, blumig-holziger/herber Geruch beschrieben. Linalool ist brennbar, der Flammpunkt der Flüssigkeit liegt bei 78 °C, die Zündtemperatur bei 235 °C und die Explosionsgrenzen liegen zwischen 0,9 % (untere Explosionsgrenze) und 5,2 % (obere Explosionsgrenze). Der Brechungsindex der Flüssigkeit liegt bei 20 °C zwischen 1,46 und 1,4675.
Reaktionen
Linalool kann mit Wasserstoff an Katalysatoren zu Tetrahydrolinalool hydriert werden:

Im sauren Milieu isomerisiert Linalool zum Geraniol. Analog erfolgt die Isomerisierung zum Nerol bzw. Terpineol.

Linalool reagiert wie alle Alkohole mit Säuren zu Carbonsäureestern. So kann Linalool z. B. mit Essigsäure zu Linalylacetat verestert werden.

Verwendung
Als ein Bestandteil ätherischer Öle wie auch als Reinstoff findet Linalool als Geruchs- und Geschmackstoff Verwendung. Es ist seit 1954 ein duftgebender Bestandteil des tschechischen Rasierwassers Pitralon F – voda po holení, das bis heute in unveränderter Zusammensetzung produziert wird.
Es ist ein Zwischenprodukt bei der Synthese von Vitamin E.
Gefahrenhinweise
Linalool wirkt reizend auf Haut und Augen, es ruft Rötungen und Schmerzen hervor. Linalool kann oral oder inhalativ aufgenommen werden. Es ist schwach wassergefährdend (WGK 1). Die LD50 für Ratten bei oraler Aufnahme liegt bei 2.790 mg/kg, bei dermaler Resorption bei 5.610 mg/kg. Linalool hat sich in vielen Tests als nicht erbgutverändernd erwiesen. Auch eine karzinogene Wirkung konnte bis heute nicht nachgewiesen werden. Chronische Aufnahme führt zur Schädigung der Leber.
Linalool gehört zu den Prohaptenen, Substanzen, deren Oxidationsprodukte an der Luft (Linalooloxid) bzw. Reaktionsprodukte auf der Haut allergieauslösend sind. In einer europaweiten Studie erwiesen sich 1,3 Prozent der Patienten als sensibel auf oxidiertes Linalool.
Weblinks
- OECD: Screening Information Dataset (SIDS) Initial Assessment Report (SIAR) für 1,6-Octadien-3-ol, 3,7-dimethyl-
- Eintrag zu Linalool in der Consumer Product Information Database
Einzelnachweise
This article uses material from the Wikipedia Deutsch article Linalool, which is released under the Creative Commons Attribution-ShareAlike 3.0 license ("CC BY-SA 3.0"); additional terms may apply (view authors). Abrufstatistik · Autoren Der Inhalt ist verfügbar unter CC BY-SA 4.0, sofern nicht anders angegeben. Images, videos and audio are available under their respective licenses.
®Wikipedia is a registered trademark of the Wiki Foundation, Inc. Wiki Deutsch (DUHOCTRUNGQUOC.VN) is an independent company and has no affiliation with Wiki Foundation.






